
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
![]()
![]() 江苏省泰州中学2018届高三3月月度检测(二模模拟)
江苏省泰州中学2018届高三3月月度检测(二模模拟)
化学
本试卷分第I卷(选择题) 和第II卷(非选择题) 两部分,共120分,考试用时100分钟。
相对原子质量S 32 O 16 C 12 Mn 55 C1 35.5 Fe 56 Cu 64 Mg 24 Ca 40 Na 23
I卷 (选择题)
单项选择题: 本题包括10小题,每小题2分,共计20分。每小题只有一个选项符合题意。
1.化学与人类生产、生活,社会可持续发展密切相关。下列说法正确的是
A.蔬菜表面洒少许福尔马林,可保鲜和消毒
B.推广使用可降解塑料及布质购物袋,以减少“自色污染”
C.绿色食品就是不使用化肥农药,不含任何化学物质的食品
D.推广使用煤液化技术可减少二氧化碳温窒气体的排放
2.下列有关化学用语表示正确的是
A.重氢原子: ![]() B.NH4Br的电子式:
B.NH4Br的电子式:![]()
C.NaHSO3的电离方程式:NaHSO3=Na++H++SO32-
D.邻羟基苯甲酸的结构简式:![]()
3.下列有关物质性质与用途具有对应关系的是
A.二氧化硅为酸性氧化物,可用于制造光导纤维
B.明矾溶于水能形成胶体,可用于自来水的杀菌消毒
C.浓硫酸具有脱水性,可用于干燥H2、SO2等
D.Zn具有还原性和导电性,可用作锌锰干电池的负极材料
4.用下列实验装置和方法进行相应实验,能达到实验目的的是
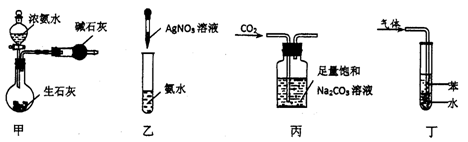
A.用图甲装置制取干燥的氨气 B.用图乙装置配制银氨溶液
C.用图丙装置除去CO2中含有的少量HCl D.用图丁装置吸收NH3,并防止倒吸
5.己知W、X、Y、Z为短周期元素,原子序数依次增大。W、Z同主族,X、Y、Z同周期,其中只有X为金属元素。下列说法一定正确的是
A.W的含氧酸的酸性比Z的含氧酸的酸性强
B.原子半径:X>Y>Z>W
C.W的气态氢化物的稳定性小于Y的气态氢化物的稳定性
D.若W与X原子序数差为5,则形成化合物的化学式为X3W2
6.下列指定反应的离子方程式正确的是
A.向氢氧化钡溶液中加入硫酸氢钠至溶液为中性: Ba2++20H-+2H++SO42-=BaS04↓+2H2O
B.电解氯化镁溶液: 2Cl-+2H20![]() H2↑+ Cl2↑+20H-
H2↑+ Cl2↑+20H-
C.氯气与水反应: Cl2+H20==2H++Cl-+ClO-
D.向碳酸氢铵溶液中加入足量石灰水: Ca2++HCO3-+OH-=CaCO3↓+H2O
7.下列物质的转化在给定条件下不能实现的是
A.NH3![]() O2
O2![]() HNO3 B.浓HCl
HNO3 B.浓HCl![]() Cl2
Cl2![]() 漂白粉
漂白粉
C.Al2O3![]() AlCl3(aq)
AlCl3(aq)![]() 无水AlCl3
无水AlCl3
D.淀粉![]() 葡萄糖
葡萄糖![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO
8.通过以下反应可获得新型能源二甲醚(CH3OCH3)。下列说法不正确的是
①C(s)+H20(g)=CO(g) H2(g) △H1=akJ/mol
②CO(g)+H2O(g)=CO2(g)+H2(g) △H2=bkJ/mol
③CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H3=ckJ/mol
④2CH3OH(g)=CH3OCH3(g)+H2O(g) △H4=dkJ/mol
A.反应①、②为反应③提供原料气,且a>0
B.反应③也是CO2资源化利用的方法之一
C.反应CH3OH(g)=1/2CH3OCH3(g)+1/2H2O(g) △H=-(2b+2c+d)kJ/mol
D.反应2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g)的△H=(2b+2c+d)kJ/mol
9.常温下,在下列给定条件的溶液中,一定能大量共存的离子组是
A.Kw/c(H+)=0.1mol/L的溶液:Na+、K+、SiO32-、NO3-
B.加入铝粉生成H2的溶液; K+、Mg2+、SO42-、HCO3-
C.c(Fe3+)=0.1mol/L的溶液: NO3-、A13+、Cl-、CO32-
D.能使pH试纸呈红色的溶液:Na+、NH4+、Fe2+、NO3-
10.下列装置图或曲线图与对应的叙述相符的是
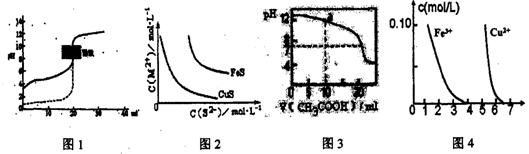
A.如图1所示,用0.1mol/LNaOH溶液分别滴定相同物质的量浓度、相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线
B.某温度下FeS、CuS的沉定溶解平衡曲线如图2所示,纵坐标c(M2+)代表Fe2+或Cu2+的浓度,横坐标c(S2-)代表S2-浓度。在物质的量浓度相等的Fe2+和Cu2+的溶液中滴加硫化钠溶液,首先沉淀的离子为Fe2+
C.如围3所示,用0.1mol/LCH3COOH溶液滴定20mL0.1mol/LNaOH溶液的滴定曲线,当pH=7时:c(Na+)=(CH3COO-)>c(OH-)=c(H+)
D.据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在5.5左右
不定项选择题:本题包括5小题,每小题4分,共计20分。每小题只有一个或两个选项符合题意。若正确答案只包括一个选项。多选时,该小题得0分;若正确答案包括两个选项,只选一个且正确的得2分,逸两个且都正确的得漪分,但只要选错一个,该小题就得0分。
11.已知常温下CH3COOH和NH3·H2O的电离平衡常数分别为Ka、Kb。若在常温下向0.1mol/L的醋酸溶液中逐滴加入相同浓度的氨水直至完全过量,则下列说法正确的是
A.加入氨水的过程中,溶液的导电性一直不断增强
B.CH3COONH4在水溶液中的水解平衡常数Kb=Kw/(Ka+Kb)
C.若Ka≈Kb,当加入等体积的氨水时,溶液基本呈中性
D.该等式在滴加过程中始终成立c(CH3C0O-)+c(CH3COOH)=c(NH4+)+c(NH3·H20)
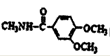
12.丹参素能明显抑制血小板的聚集,其结构如图所示,下列说法错误的是
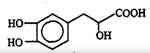
A.丹参素的分子式为C9H10O5
B.丹参素能发生缩聚、消去、氧化反应
C.1mol丹参素最多可以和4molH2发生加成反应
D.丹参素分子中含有手性碳原子
13.根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向硅酸钠溶液中滴加盐酸 | 有白色胶状沉淀生成 | 非金属性:Cl>Si |
| B | 向溶液X中加入稀盐酸,并将产生的无色无味气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中一定含有CO32-或HCO3- |
| C | 向1mL0.1mol/L MgSO4溶液中,滴入2滴0.1mol/L1NaOH溶液,再滴入2滴0.1mol/LCuSO4溶液 | 起初生成的白色沉淀逐渐变为蓝色沉淀 | Ksp[Cu(OH)2] |
| D | 向鸡蛋白溶液中滴入HgCl2溶液 | 有白色抗淀 | 蛋白质发生盐析 |
14.25℃,c(HCN)+c(CN-)=0.1mol/L的一组HCN和NaCN的混合溶液,溶液中c(HCN)、c(CN-)与pH的关系如图所示。下列有关离子浓度关系叙述正确的是
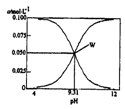
A.将0.1mol/L的HCN溶液和0.1mol/LNaCN溶液等体积混合(忽略溶液体积变化): c(Na+)>c(HCN)>c(CN-)>c(OH-)>c(H+)
B.W点表示溶液中: c(Na+)+c(H+)=c(HCN)
C.pH=8的溶液中: c(Na+)+c(H+)+c(HCN)=0.1mol/L +c(OH-)
D.将0.3mol/LHCN溶液和0.2mol/LNaOH溶液混合
15.一定温度下,在3个体积均为1.0L的恒容密闭容器中反应2SO2(g)+02(g) 2SO3(g)达到平衡。下列说法正确的是
| 容器 | 温度/K | 物质的起始浓度/mol/L | 物质的平衡浓度/mol/L | SO2或SO3平衡转化率 | ||
| c(SO2) | c(O2) | c(SO3) | ||||
| I | 723 | 0.2 | 0.1 | 0 | 0.16 | a1 |
| II | 723 | 0.4 | 0.2 | 0 | a2 | |
| III | 823 | 0 | 0 | 0.2 | a3 | |
A.达到平衡时,a1+a3>1
B.达到平衡时,容器中的压强: PII>PI>PIII
C.达到平衡时,容器III中的逆反应速率比容器I中的大
D.若起始时,向容器I中充入0.16molSO2、0.04molO2和0.16molSO3,则此时反应向逆反应方向进行
II卷 非选择题
16.(12分) 酸浸法制取硫酸锕的流程示意图如下
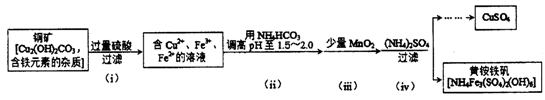
①若用CuSO4进行化学镀铜,应选用__________(填“氧化剂”或“还原剂”) 与之反应。
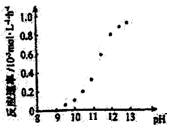
②某化学镀铜的反应速率随镀液pH变化如右图所示。该镀铜过程中,镀液pH控制在12.5左右。据图中信息,给出使反应停止的方法:________________。
17.(15分) 阿塞那平用于治疗精神分裂症,可通过以下方法合成(部分反应条件略去):
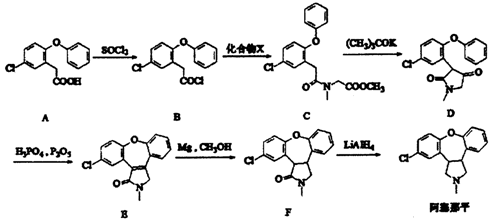
 的合成路线流程图(无机试剂任用)。
的合成路线流程图(无机试剂任用)。18.(12分)某研究小组用黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备ClO2气体,再用水吸收该气体可得C1O2溶液。在此过程中需要控制适宜的温度,若温度不当,副反应增加,影响生成ClO2气体的纯度,且会影响ClO2的吸收率,具体情况如图所示。
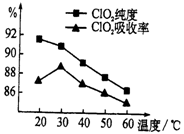
l4H++Cr2O72-+6Fe2+=2Cr3++6Fe3++7H2O
试计算ClO2的“产率”(写出计算过程)。
19.(15分)NiSO4•6H20是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废液(除含镍外,还含有Cu、Fe、Cr等杂质)为原料获得。工艺流程如下图:
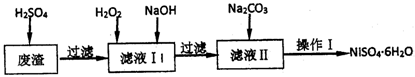
已知: 25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如下表所示。
| Fe(OH)2 | Fe(OH)3 | Cr(OH)3 | Ni(OH)2 | |
| Ksp | 8.0×10-16 | 4.0×10-38 | 6.0×10-31 | 6.5×10-18 |
| 完全沉淀pH | ≥9.6 | ≥3.2 | ≥5.6 | ≥8.4 |
注:NiCO3是一种不溶于水易溶于强酸的沉淀。
请回答下列问题:
①_______________________; ②_______________________;
③蒸发浓缩、冷却结晶,过滤得NiSO4•6H2O晶体
④用少量乙醇洗涤NiSO4•6H2O晶体并晾干。
20.(14分)为保护环境,应减少二氧化硫、氮氧化物和二氧化碳等物质的排放量。
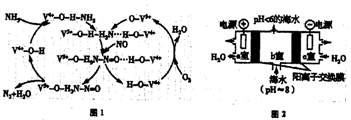
①a室的电极反应式为__________。
②b室中提取CO2的反应的离子方程式为____________。
③b室排出的海水(pH<6)不可直接排回大海,需用该装置中产生的物质对b室排出的海水进行处理,合格后才能排回大海。处理的方法是_________。
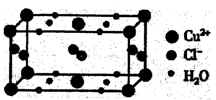
21.(12分)将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出深蓝色的晶体[Cu(NH3)4]SO4•H2O。
17.(15分)
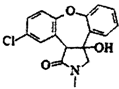 (3分)
(3分)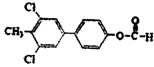 (3分)
(3分)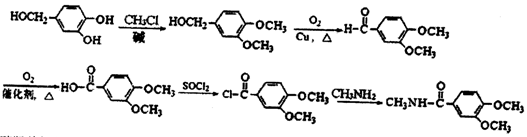 (5分)
(5分)(醇羟基氧化可写为一步)
18.(12分) (1)30℃(2分) 水浴加热(2分)(或水浴控制恒温等合理答案均可)
(2)15ClO3-+FeS2+14H+=15ClO2+Fe3++7H2O+2SO42-(2分)
(3)56.25%(6分)
19.(15分)
②向沉淀中滴加稀H2SO4,直至恰好完全溶解。(2分)
20.(14分)
②H++HCO3-=H2O+CO2↑;
③用c室排出的碱性溶液将从b室排出的酸性海水调节至接近正常海水的pH。
21.(12分)