湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
![]() 高四第二学期第1次考试化学试题
高四第二学期第1次考试化学试题
一、单选题
1.下列实验的现象所得到的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向溶有SO2的BaCl2溶液中通入气体X | 产生白色沉淀 | X一定是Cl2 |
| B | 向NaClO和NaOH的混合溶液中加入 H2O2浓溶液 | 产生大量气泡 | 碱性条件下,H2O2被ClO-氧化成O2 |
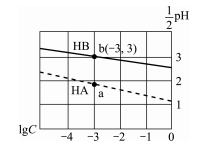
| C | 等体积PH=3的HA和HB两溶液分别与足量的锌反应 | HA放出的H2多 | 酸性:HA>HB |
| D | 将铜片和铁片导线连接插入浓硝酸中 | 铁片表面有气泡产生 | 金属活动性:Cu>Fe |
2.已知: 常温下,(1) Ka1(H2CO3)=4.3×10-7, Ka2(H2CO3)=5.6×10-11;(2)H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是
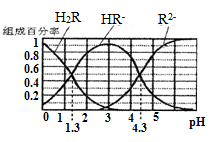
3.某溶液中除H+、OH—外,还有大量的Mg2+、Fe3+、Cl-,且这三种离子的物质的量之比为1:1:6,下列有关该溶液的判断正确的是
4.下列有关实验装置进行的相应实验,能达到目的的是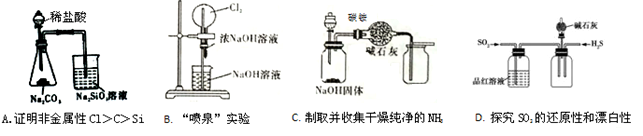
5.能证明乙酸是弱酸的实验事实是
6.用电解法可制取有广泛用途的Na2FeO4:Fe+2H2O+ 2NaOH![]() Na2FeO4+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeOH42-,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。下列说法不正确的是
Na2FeO4+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeOH42-,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。下列说法不正确的是
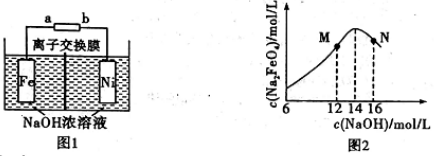
7.室温下,1mol·L-l的某二元酸H2A溶液中,存在的HA-、A2-的物质的量分数随pH变化的关系如图所示,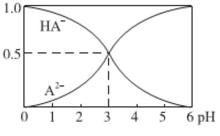
下列说法不正确的是
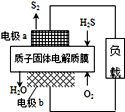
8.已知:2H2S(g)+O2(g) = S2(s)+2H2O(l) △H= -632 kJ•mol-1,如图为质子膜H2S燃料电池的示意图。下列说法正确的是
9.分子式为C6H12Cl2的有机物,分子中只含有一个甲基的结构有(不考虑立体异构)
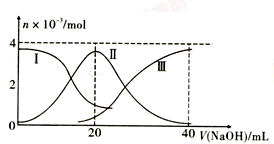
10.常温下,向20mL0.2 mol·L-1H2A溶液中滴加0.2 mol·L-1NaOH溶液。有关微粒的物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是
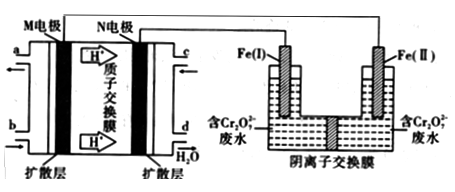
11.用甲醇燃料电池作电源,用铁作电极电解含Cr2O72-的酸性废水,利用生成的Fe2+可将Cr2O72-转化成Cr(OH)3沉淀而除去,装置如图。下列说法正确的是
12.下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向包有Na2O2粉末的脱脂棉滴2滴水 | 脱脂棉燃烧 | Na2O2与水反应放热 |
| B | Fe(NO3)2样品中加入稀硫酸,再滴加KSCN溶液 | 溶液变为血红色 | Fe(NO3)2样品已经变质 |
| C | 向FeCl3溶液中加入Mg(OH)2悬浊液,振荡 | 沉淀由白色变为红褐色 | Fe(OH)3的溶度积小于Mg(OH)2 |
| D | 向蔗糖溶液中加入稀硫酸,加热几分钟后加入新制Cu(OH)2悬浊液,加热煮沸 | 无红色沉淀生成 | 蔗糖没有发生水解反应生成葡萄糖 |
13.前20号元素W、X、Y、Z原子序数依次递增,W原子最外层电子数是次外层的3倍,X的简单离子半径在同周期中最小。W、Z的质子数之和等于X、Y的质子数之和,X、Y、Z的最外层电子数之和等于W的核外电子数。下列说法错误的是
14.化合物a、b的结构简式如图所示,下列说法正确的是
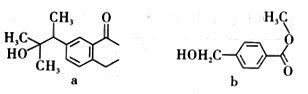
C. a、b均能发生还原反应、取代反应、消去反应 D. b分子发生加成反应最多消耗4mol H2
15.设NA为阿伏加德罗常数的值,下列说法正确的是
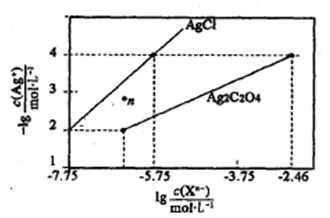
16.常温下,用AgNO3溶液分别滴定浓度均为0.01mol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图像如下图所示(不考虑C2O42-的水解)。下列叙述正确的是
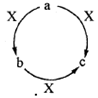
17.a、b、c、X是中学化学中常见的四种物质,且a、b、c中含有同一种元素,其转化关系如下图所示。下列说法不正确的是
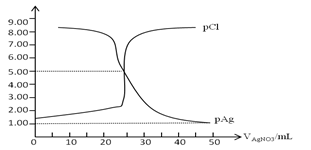
18.常温下,用0.100mol/L 的AgNO3溶液滴定50.0mL,0.0500mol/L KCl溶液,以K2CrO4为指示剂,测得溶液中pCl=-lgc(Cl-)、pAg=-lgc(Ag+)随加入AgNO3的体积变化如图所示,已知溶液中离子浓度小于等于1.0×10-5mol/L则沉淀完全,Ksp(Ag2CrO4)=2.0×10-12,Ksp(Ag2SO4)=1.4×10-5,下列说法错误的是( )
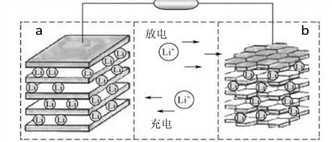
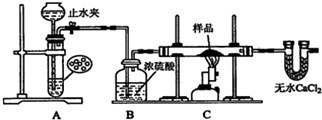
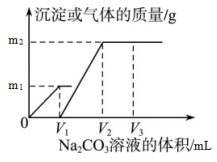
19.镍钴锰三元材料是近年来开发的一类新型锂离子电池正极材料,具有容量高、循环稳定性好、成本适中等重要优点。镍钴锰三元材料中Ni为主要活泼元素,通常可以表示为:LiNiaCobMncO2,其中a+b+c=1,可简写为LiAO2。放电时总反应为LiAO2+ nC = Li1-xAO2+ LixCn(0 20.常温下,分别向体积相同、浓度均为1 mol/L的HA、HB两种酸溶液中不断加水稀释,酸溶液的pH与酸溶液浓度的对数(lg C)间的关系如图。下列对该过程相关分析正确的是 二、实验题 21.某红色固体粉末样品可能含有Fe2O3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究。 查阅资料:Cu2O在酸性溶液中会发生反应:Cu2O+2H+=Cu+Cu2++H2O 探究一:用如图所示装置进行实验,回答下列问题: (1)仪器组装完成后,夹好止水夹,_____,则说明装置A的气密性良好. (2)装置A是氢气的发生装置,可以选用的药品是________(填选项) A.稀硫酸和锌片 B.稀硝酸和铁片 C.氢氧化钠溶液和铝片 D.浓硫酸和镁片 (3)从下列实验步骤中,选择正确的操作顺序:①________③(填序号). ①打开止水夹 ②熄灭C处的酒精喷灯 ③C处冷却至室温后,关闭止水夹 ④点燃C处的酒精喷灯 ⑤收集氢气并验纯 ⑥通入气体一段时间,排尽装置内的空气 探究二: (4)甲同学取少量样品于试管中,加入适量的稀硫酸,若无红色物质生成,则说明样品中不含Cu2O;乙同学认为观点不正确,其原因是_____________;丙同学另取少量样品于试管中,加入适量的浓硝酸,产生红棕色的气体.证明样品中一定含有________,其反应的离子方程式为_____;丁同学预设计实验证明另一种物质是否存在,其方案为__________。 (5)取一定量样品于烧杯中,加入足量的稀硫酸,若反应后经过滤得到固体3.2g,滤液中Fe2+有1.0mol,则样品中n(Cu2O)=_________mol. 三、计算题 22.向一定体积 CaCl2和 HCl 的混合溶液中逐滴加入浓度为 1.00mol·L-1 的 Na2CO3溶液,反应过程中加入的 Na2CO3溶液的体积与产生沉淀或气体的质量关系如图所示。 已知:图中 V1: V2=1:2,当加入 V2mLNa2CO3 溶液时,所得溶液的浓度为 1.00 mol·L-1,体积为 200mL。求: (1)混合溶液中 CaCl2和 HCl 物质的量之比n(CaCl2)∶n(HCl)=_______。 (2)m2=______g。 参考答案 BBBBA BCBCD CACBA DDDCB 21. 向装置A中的长颈漏斗内注入液体至形成一段液柱,若液柱高度保持不变 AC ⑥⑤④② 生成的铜与铁离子反应 Cu2O Cu2O+6H++2NO3-=2Cu2++2NO2+3H2O 取丙同学反应后的溶液加KSCN溶液,若溶液变红色,则存在;若不变红,则不存在 0.55 22. 1:2 5.00