
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
化 学
注意事项:
1、本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2、回答第Ⅰ卷时,选出每小题答案后,用铅笔把答题卡上对应题目答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其它答案标号。写在本试卷上无效。
3、回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Cu-64 S-32 Fe-56
第Ⅰ卷 选择题
一、选择题(本题共6小题,每小题2分,共12分。每小题给出的四个选项中,只有一项是符合题目要求的)
1、下列说法不正确的是
A.淀粉可以制得葡萄糖和酒精
B.铝合金的熔点和硬度均高于纯铝
C.塑料、金属、纸类均是可回收的物品
D.硬化油不易被空气氧化而便于储存和运输
![]() 2、下列有关化学用语正确的是
2、下列有关化学用语正确的是
A.次氯酸的结构式:H-Cl-OB.钾原子的结构示意图:
C.HCN的电子式:H![]() C
C![]() N
N![]() D.芒硝的化学式:Na2CO3·10H2O
D.芒硝的化学式:Na2CO3·10H2O
3、下列离子方程式书写正确的是
A.氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-=BaSO4↓+H2O
B.淀粉碘化钾溶液在空气中变蓝:4I-+O2+2H2O = 4OH-+2I2
C.向Na2SO3溶液中滴加稀硝酸:SO32-+2H+= SO2↑+H2O
D.用氨水吸收足量的CO2气体:OH-+CO2 = HCO3-
4、一定条件下,反应3A(g)+3B(g)![]() C(g)+D(g)△H<0达到平衡,欲提高B的转化率,可采取的措施是
C(g)+D(g)△H<0达到平衡,欲提高B的转化率,可采取的措施是
A.升高温度B.增大B的浓度
C.增大压强D.使用合适的催化剂
5、三种不同物质有如图所示转化关系:![]() ,则甲不可能是
,则甲不可能是
A.Al2O3B.SiO2C.CO2D.NH4Cl
6、下列实验图示及有关描述正确的是
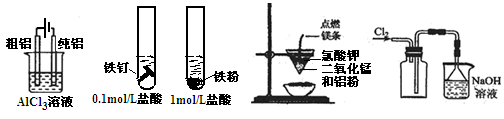
甲 乙 丙 丁
A.用甲图所示装置可以电解精炼铝 B.用乙图探究固体表面积对反应速率的影响
C.用丙图所示装置可以制得金属锰D.用丁图所示装置可以收集Cl2
二、选择题(本题包括6小题,每小题4分,共计24分。每题有1~2个选项符合题意。)
7、已知短周期元素的离子aA2+、bB+、cC3—都具有相同的电子层结构,下列叙述正确的是
A.原子半径A>B >CB.原子序数C>B>A
C.单质的还原性A>B >C D.离子半径C >B>A
8、设NA为阿伏加德罗常数,下列叙述正确的是
A.3.4gNH3中含有电子数为2NA
B.0.1mol/L CuSO4溶液中含有的SO42-数目为0.1NA
C.常温常压下,2.24L O3中含有的氧原子数为0.3NA
D.足量的MnO2与50mL 8mol/L浓盐酸充分反应后,生成Cl2的分子数为0.1NA
9、为达到预期的实验目的,下列操作中正确的是
A.鉴别AlC13溶液和MgC12溶液:向2种待测液中分别滴加足量氨水
B.可用过滤法分离氢氧化铁胶体和三氯化铁溶液的混合物
C.除去Fe(OH)3固体中少量Mg(OH)2:加入足量浓FeCl3溶液,充分搅拌过滤
D.除去铜器表面的铜绿[Cu2(OH)2CO3]:用硝酸浸泡,再用清水冲洗
10、25℃时,下列溶液中离子浓度的等量关系正确的是
A.0.1 mol/L氨水中:c(NH4+) + c(H+) = c(OH-)
B.0.1 mol/L的NH4Cl溶液中:c(NH4+) = c(Cl-)
C.pH=12的NaOH溶液与pH=12的氨水中:c(Na+)=c(NH4+)
D.pH=3的盐酸和pH=11的氨水等体积混合后:c(OH-) = c(H+)
11、CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法正确的是
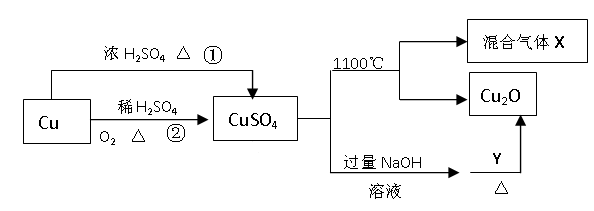
A.相对于途径①,途径②更好地体现了绿色化学思想
B.Y可以是蔗糖溶液
C.CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体
D.将CuSO4溶液蒸发、冷却、结晶,可制得胆矾晶体
12、许多马路两旁的树干都均匀地涂抹了石灰水。下列有关说法正确的是
A.饱和石灰水加入生石灰,若温度不变,则溶液中Ca2+的物质的量不变
B.饱和石灰水加入生石灰,若温度不变,则pH不变
C.升高饱和石灰水的温度时,Ca(OH)2的溶度积常数Ksp不变
D.石灰水显碱性,能使蛋白质变性,所以有防治树木害虫病的作用
第Ⅱ卷 非选择题
本卷包括必考题和选考题两部分。第13 题~第17 题为必考题,每个试题考生都必须做答。第18 题~第 20 题为选考题,考生根据要求做答。
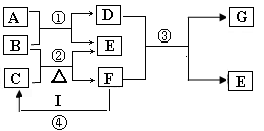 13、(8分)如图表示由元素周期表中1~20号且不同主族元素组成的单质及化合物之间转化关系(产物中的水已略去)。其中A为黄绿色气体单质;在实验室中,常用固体B和固体C加热制取刺激性气味气体F;F与G的组成元素相同.G与I分子所含电子数相同。请回答:
13、(8分)如图表示由元素周期表中1~20号且不同主族元素组成的单质及化合物之间转化关系(产物中的水已略去)。其中A为黄绿色气体单质;在实验室中,常用固体B和固体C加热制取刺激性气味气体F;F与G的组成元素相同.G与I分子所含电子数相同。请回答:
(1)写出B、I的化学式B ,I 。
(2)反应④的实验现象为 ;写出F的一种具体用途 。
(3)向具有漂白作用的D溶液加入I的浓溶液有A生成,其反应的离子方程式为: 。
(4)写出反应③的化学方程式 。
14、(10分)如图甲、乙是电化学实验装置。
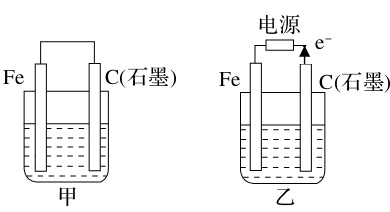
(1)若甲、乙两烧杯中均盛有饱和NaCl溶液。
①甲中石墨棒上的电极反应式_____________,电子的移动方向为_____________。
②乙中总反应的离子方程式为______________,Cl-移向_______电极(填Fe或C)。
③将湿润的淀粉-KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为:____________________________。
(2)如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入CuO的质量为 。
15、(8分)在一定体积的密闭容器中,进行如下化学反应:CO(g) + H2O(g)![]() CO2(g) + H2(g),其化学平衡常数K和温度t的关系如下表:
CO2(g) + H2(g),其化学平衡常数K和温度t的关系如下表:
| t ℃ | 700 | 800 | 830 | 1000 |
| K | 2.6 | 1.7 | 1.0 | 0.9 |
回答下列问题:
(1)该反应的化学平衡常数表达式K= 。
(2)该反应为 反应(填“吸热”或“放热”)。
(3)增加H2O(g)的浓度,CO的转化率将 (填“增大”、“减小”或“不变”)。
 (4)830℃时,向该容器中加入2molCO2与2molH2,平衡时CO2的体积分数是 。
(4)830℃时,向该容器中加入2molCO2与2molH2,平衡时CO2的体积分数是 。
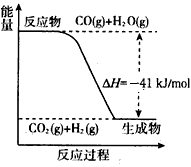
(5)已知工业制氢气的反应为CO(g) + H2O(g)![]() CO2(g) + H2(g),反应过程中能量变化如右图所示。又已知2H2(g) + O2(g) =2H2O(g) △H=-484kJ/mol。 结合图像写出CO完全燃烧生成CO2的热化学方程式: 。
CO2(g) + H2(g),反应过程中能量变化如右图所示。又已知2H2(g) + O2(g) =2H2O(g) △H=-484kJ/mol。 结合图像写出CO完全燃烧生成CO2的热化学方程式: 。
16、(8分)A~F的转化关系如下:
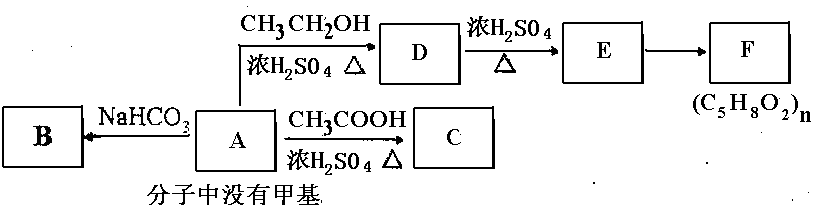
请回答下列问题:
(1)有机物A的相对分子质量为90,9.0gA和足量的金属Na反应,在标准状况下能生成2.24L的H2,则A的分子式为 。
(2)C的结构简式为 ,由E生成F的反应类型是 。
(3)写出由D生成E的化学方程式为 。
(4)写出与A具有相同官能团的A的同分异构体的结构简式 。
17、(10分)有某种含有少量FeCl2杂质的FeCl3样品。现要测定其中铁元素的质量分数,实验采用下列步骤进行:
①准确称量mg样品(在2~3g范围内);
②向样品中加入10mL 6 mol·L-1的盐酸,再加入蒸馏水,配制成250mL溶液;
③量取25mL操作②中配得的溶液,加入3mL氯水,加热使其反应完全;
④趁热迅速加入10%氨水至过量,充分搅拌,使沉淀完全;
⑤过滤,将沉淀洗涤后,移至坩埚,灼烧、冷却、称重,并重复操作至恒重。
试回答下列问题:
(1)溶解样品时,要加入盐酸,原因是__________________________________________。
(2)加入氯水后,反应的离子方程式为__________________________________________。
(3)若不用氯水,可用下列试剂中的______________代替(填序号)。
A.H2O2B.碘水C.NaClO
(4)步骤⑤中检验沉淀是否洗净的方法是__________________________________。
(5)若坩埚质量为W1g,坩埚及灼烧后的固体总质量为W2g,样品中铁元素的质量分数为____________________________________。
选考题(请考生在第l8、l9、20三题中任选一题做答,如果多做,则按所做的第一题计分。做答时用2B铅笔在答题卡上把所选题目的题号涂黑)。
第18、19、20三题的第Ⅰ题为选择题,在给出的四个选项中,有两项是符合题目要求的,请将符合题目要求的选项标号填在答题卡相应位置;第Ⅱ题为非选择题,请在答题卡相应位置做答并写明小题号。
《有机化学基础》
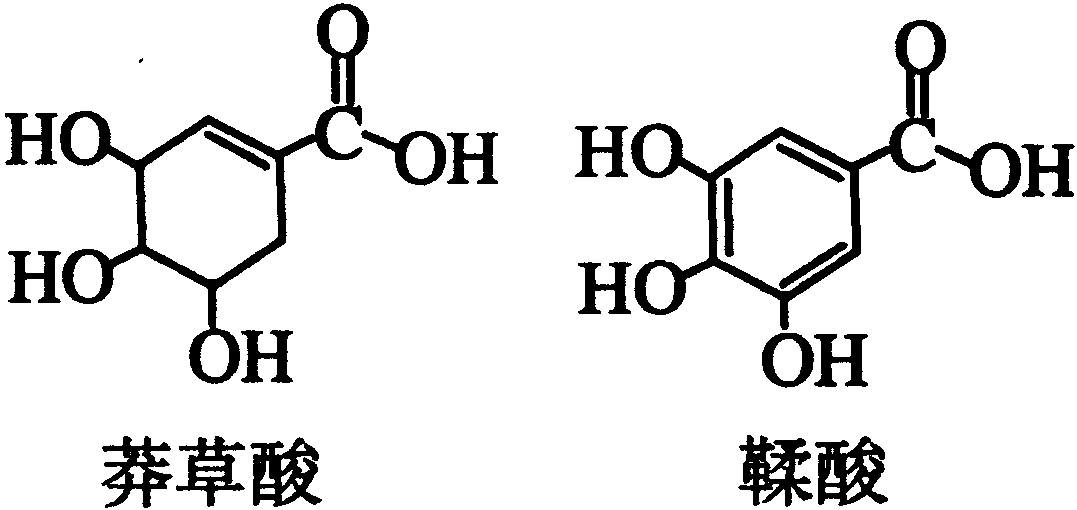 18-I(6分)莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物的说法正确的是
18-I(6分)莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物的说法正确的是
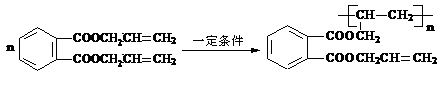
18-II(14分)DAP-A树脂是一种优良的热固性树脂,被用作高级UV油墨的一种成分。这种材料可采用如下合成路线制备:
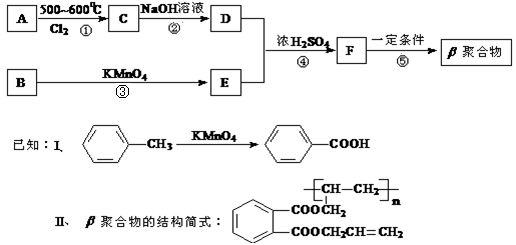
试回答下列问题:
(1)在①~④的反应中属取代反应的是 。
(2)写出反应②的化学方程式 。
(3)写出反应⑤的化学方程式 。
(4)工业上可由C经过两步反应制得甘油,这两步反应的反应类型依次是 和 。
(5)写出B(C8H10)苯环上的所有二氯代物结构简式: ,其中核磁共振氢谱只有两组峰,且峰面积比为3: 1的有 种。
《物质结构与性质》
19-Ⅰ(6分)下列说法中正确的是
A.丙烯分子中有8个σ键,1个π键
B.60g的SiO2晶体中,含有4mol共价键
C.NCl3和BCl3分子,都是三角锥形
D.SiH4的沸点高于CH4,可推测PH3的沸点高于NH3
19-Ⅱ(14分)尿素(H2NCONH2)可用于制有机铁肥,主要代表有 [Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]。
(1)基态Fe3+的核外电子排布式为 。C、N、O三种元素的第一电离能由大到小的顺序是 。
(2)尿素分子中C、N原子的杂化方式分别是 。
(3)[Fe(H2NCONH2)6](NO3)3中“H2NCONH2”与Fe(Ⅲ)之间的作用力是 ,与NO互为等电子体的一种化合物是 (写化学式)。
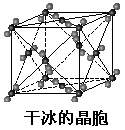 (4)CO2和NH3是工业上制备尿素的重要原料,固态CO2(干冰)的晶胞结构如下图所示。
(4)CO2和NH3是工业上制备尿素的重要原料,固态CO2(干冰)的晶胞结构如下图所示。
① 铜金合金的晶胞结构与干冰相似,若顶点为Au、面心为Cu,则铜金合金晶体中Au与Cu原子数之比为是 。
② 已知干冰晶胞边长为a pm,则该晶体的密度为
g/cm3(NA表示阿伏加德罗常数的值)。
《化学与技术》
20-I(6分)下列说法正确的是
A.石油裂解的主要目的是提高轻质液体燃料的产量
B.电解饱和食盐水制造烧碱时,采用离子交换膜可防止氯气进入阴极室
C.硫酸工业中在接触室安装热交换器的目的是利用SO2催化氧化时放出的热量
D.绿色化学的核心是应用化学原理对环境污染进行治理
20-II(14分)甲醇是一种重要的有机化工原料,需求量巨大。目前我国独创的联醇工艺的核心是采用一氧化碳加氢中压合成法。主要反应如下:
CO(g) + 2H2(g) = CH3OH(g) ;△H = -111.0kJ/mol
另有副反应:2CO + 2H2O = CO2 + CH4 等;中压法操作:压力为10—15MPa ,温度控制在513K—543K,所用催化剂是CuO-ZnO-Al2O3。合成甲醇的流程如图所示,
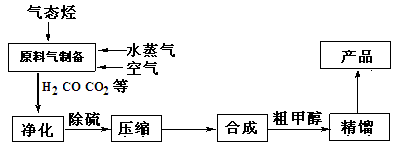
请回答:
(1)实际生产中CO不能过量,以免生成羰基铁使催化剂失去活性,而氢气过量是有益的,指出两点理由:_______________________,______________________。
(2)采取10—15MPa压力的作用是___________________________________;温度控制在513K—543K的原因是_____________________。
(3)原料气中的H2S对铜催化剂影响甚重,故必先去除之,通常用生石灰除杂,该反应的化学方程式为______________________________________ :
(4)粗甲醇中含有二甲醚等副产物,在常压下蒸馏粗甲醇,首先获得的馏分是_________________(写结构简式);获得的甲醇又可在银催化下氧化成甲醛,该反应的化学方程式为:______________________________________ 。
(5)若CO的转化率为80%,当有22.4M3(标况)CO与过量H2充分反应(不计其它副反应),可制得纯度为96%的甲醇的质量为_______kg,同时获得热量___________kJ。
化 学
第Ⅰ卷 选择题
(前6小题每个2分,后6小题每个4分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 | B | C | B | C | D | C | D | A | C | AC | AD | BD |
第Ⅱ卷 非选择题
13、共8分
(1)Ca(OH)2 HCl (每空1分)
(2)产生白烟(1分) 制氮肥(硝酸、纯碱、铵盐等)(1分)
(3)ClO-+Cl-+2H+=Cl2↑+H2O (2分)
(4)4NH3+Ca(ClO)2=2N2H4+CaCl2+2H2O (2分)
14、共10分
(1)①O2+2H2O+4e-===4OH- (2分) 由铁经导线移向石墨 (1分)
②2Cl-+2H2O2OH-+H2↑+Cl2↑ (2分) C(1分)
③5Cl2+I2+6H2O===10HCl+2HIO3(2分)
(2)0.8g(2分)
15、共8分
(1)K= C(CO2) • C(H2)∕C(CO) • C(H2O) (2分)
(2)放热(1分)
(3)增大(1分)
(4)25%(2分)
(5)CO(g) + 1∕2 O2 (g) = CO2(g) △H= —283kJ/mol(2分)
16、 共8分
(1)C3H6O3(2分)
(2)CH3COOCH2CH2COOH 加聚反应(各1分)
(3)CH2(OH)CH2COO CH2CH3![]() CH2=CH COO CH2CH3+H2O (2分)
CH2=CH COO CH2CH3+H2O (2分)
(4)CH3CH(OH) COOH (2分)
17、共10分
(1)抑制Fe3+、Fe2+水解(2分) (2)2Fe2++Cl2== 2Fe3++2Cl-(2分)
(3)A、C(2分)
(4)取少量洗涤液,加入AgNO3溶液少许,若无白色沉淀产生,则表面沉淀已洗净(2分)
(5)![]() 或
或![]() ×100% (2分)
×100% (2分)
18-I AD (6分)
18-II(14分)
(1)①②④ (全对2分)
(2)![]() (2分)
(2分)
(3) (2分)
(2分)
(4)加成反应 水解(取代)反应 (各1分,共2分)
(5)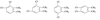
(各1分,共4分)
2种 (2分)
19-Ⅰ AB (6分)
19-Ⅱ(14分)
(1) [Ar]3d5(2分) N>O>C(2分)
(2)sp2、sp3(各1分)
(3)配位键(2分) SO3(或BF3)(2分)
(4)①1∶3(2分) ②![]() (2分)
(2分)
20-I BC (6分)
20-II(14分)
(1)既可以防止或减少副反应发生,又可带走反应热避免催化剂过热(2分)
(2)加压有利于提高CO转化率,但也增加了能源消耗和设备强度,故宜采取经济效益较好的压力,(2分),此温度下催化剂活性较高,甲醇产率较大(1分)。
(3)H2S + CaO = CaS + H2O ( 2分)
(4)CH3OCH3,2CH3OH + O2 2HCHO + 2H2O (共3分)
(5)26.67kg , 8.88×104kJ (共4分)