
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
静宁一中2016-2017学年度高三级第二次模拟考试(卷)
化 学
可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 S:32 Cl:35.5 Fe:56 Cu:64 Ba:137
第Ⅰ卷(选择题 共42 分)
一、选择题(本题包括21小题,每小题2分,42分。每小题只有一个选项最符合题目要求)
1.化学与社会、生活密切相关。对下列现象或事实的解释正确的是:
A.过氧化钠用于呼吸面具中是因为过氧化钠是强氧化剂能氧化CO2和水
B.FeCl3溶液可用于铜质印刷线路板制作是因为FeCl3能与铜单质发生置换反应
C.Al2O3作耐火材料是因为氧化铝熔点高
D.用热的纯碱溶液洗去油污原理是NaHCO3溶液水解显碱性
2.下列说法不正确的是
①铝和铜具有良好的导电性,所以电工操作时,可以把铜线和铝线拧在一起
②汽车尾气中含有能污染空气的氮氧化物,主要是汽油燃烧不充分造成的
③从海水中提取物质都必须通过化学反应才能实现
④“辽宁舰”上用于舰载机降落拦阻索的特种钢缆属于新型无机非金属材料
⑤明矾可以用于净水,主要是由于Al3+水解生成的少量氢氧化铝胶体有净水作用
A.②③⑤ B.①②④ C.①②③④ D.①③④⑤
3.观察下列有关实验装置,相关评价错误的是
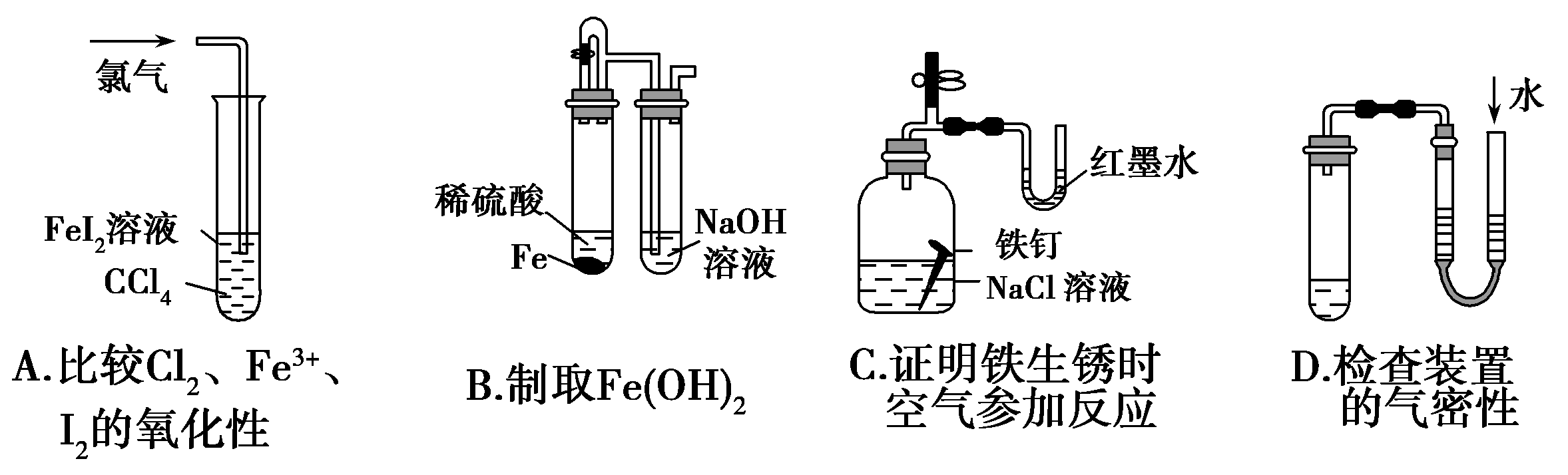
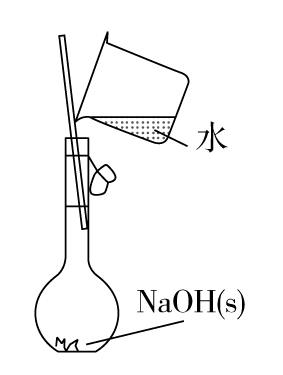
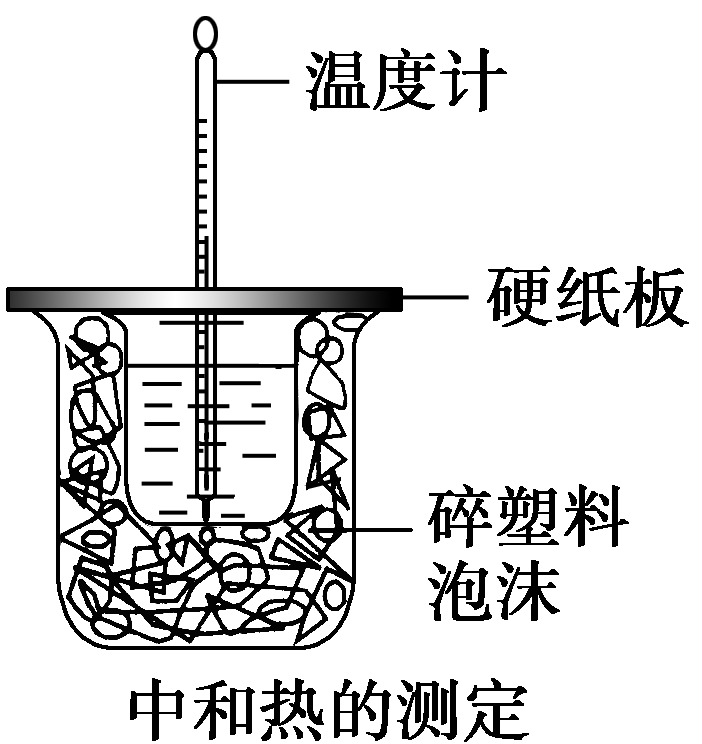
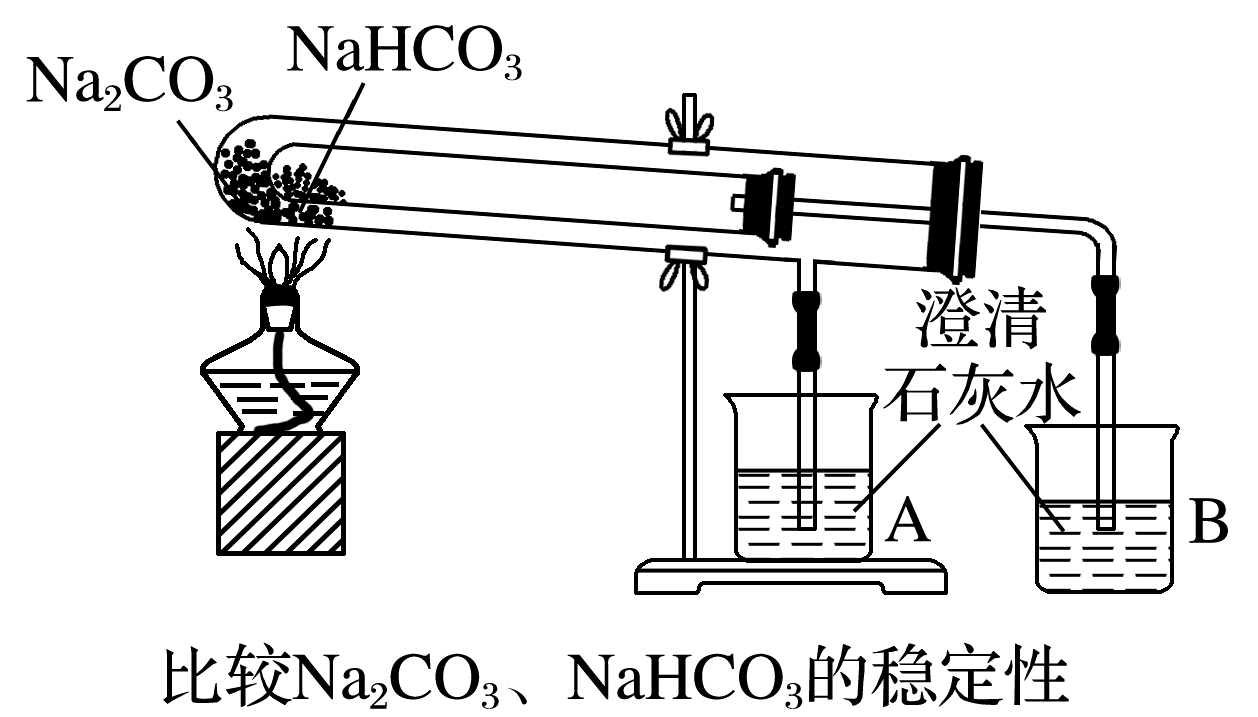
图(1) 图(2) 图(3) 图(4)
A.图(1)用于配制0.10 mol·L-1NaOH溶液;评价:正确
B.图(2)用于测定中和热;评价:错误,装置中缺少了环形玻璃搅拌棒
C.图(3)用于比较Na2CO3、NaHCO3的热稳定性;评价:正确
D.图(4)证明铁发生吸氧腐蚀时空气参加反应;评价:正确
4.NA表示阿伏加德罗常数的值。下列关于某些化学过程的描述中:
①1mol N2中含有的共价键数为2NA;
②在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA;
③密闭容器中2mol NO与1molO2完全反应,最终产物的分子数为2NA;
④将0.1 mol CO2通入足量NaOH溶液中,则反应后溶液中阴离子数目为0.1NA;
⑤含NA个Na+的Na2O2溶于1L水中,Na+物质的量浓度为1mol·L-1
错误的是
A.①③④ B.②③⑤ C.②④⑤ D.全部
5.下列关于溶液和胶体的叙述,正确的是
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
6.在标准状况下,将VL A气体(摩尔质量Mg/mol)溶于1L水中,所得A的水溶液密度为ρg/cm3,则此溶液的物质的量浓度(mol/L)为
7.下列有关物质的分类或归类不正确的是
①混合物:石炭酸、福尔马林、水玻璃、水银
②化合物:CaCl2、烧碱、苯乙烯、聚乙烯
③电解质:明矾、冰醋酸、硫酸钡
④纯净物:干冰、冰水混合物、浓硫酸、水晶
⑤同素异形体:足球烯、石墨、金刚石
⑥同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
A.①②③④ B.①②④⑥ C.①③④⑤ D.②④⑤⑥
8.下列分子或离子在指定溶液中能大量共存的是
A.酸性溶液中:Cl-、SO、Fe3+、Mg2+
B.使酚酞变红的溶液中:Na+、CO32-、Cl-、Al3+
C.1.0 mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO
D.1.0 mol·L-1的CuSO4溶液:H+、Ba2+、AlO2-、NH3·H2O
9.下列反应的离子方程式书写正确的是
A. NaAlO2溶液中通入过量的CO2: 2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32-
B.向海带灰浸出液中加入稀硫酸、双氧水:2I-+2H++H2O2=I2+ 2H2O
C.向盐酸中滴加氨水:H++OH-=H2O
D. NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+ OH-+ Ba2+=H2O+BaCO3↓
10.下列化工生产过程中,未涉及氧化还原反应的是
A.海带提碘 B.氨碱法制碱 C.氯碱工业 D.海水提溴
11.类比推理的方法在化学学习与研究中有广泛的应用,但有时会得出错误的结论。以下几种
类比推理结论中正确的是 ( )
A.CO2通入Ba(NO3)2溶液中无沉淀生成,推出SO2通入Ba(NO3)2溶液中无沉淀生成
B.Fe3Cl8可以改写为FeCl2·2FeCl3,推出Fe3I8可以改写为FeI2·2FeI3
资*源%库 C.NH3的沸点高于PH3,推出CH4沸点高于SiH4
D.H2SO4为强酸,推出HC1O4为强酸
12.在给定条件下,下列划横线的物质在化学反应中能被完全消耗的是
A.常温下,将1 g铝片投入20 mL 18.4 mol·L-1的硫酸中
B.用50 mL浓盐酸与足量MnO2共热
C.向100 mL 3 moI·L-1的硝酸中加入5.6 g铁
D.在5×107 Pa、500 ℃和铁触媒催化的条件下,用3 mol氢气和2 mol氮气合成氨
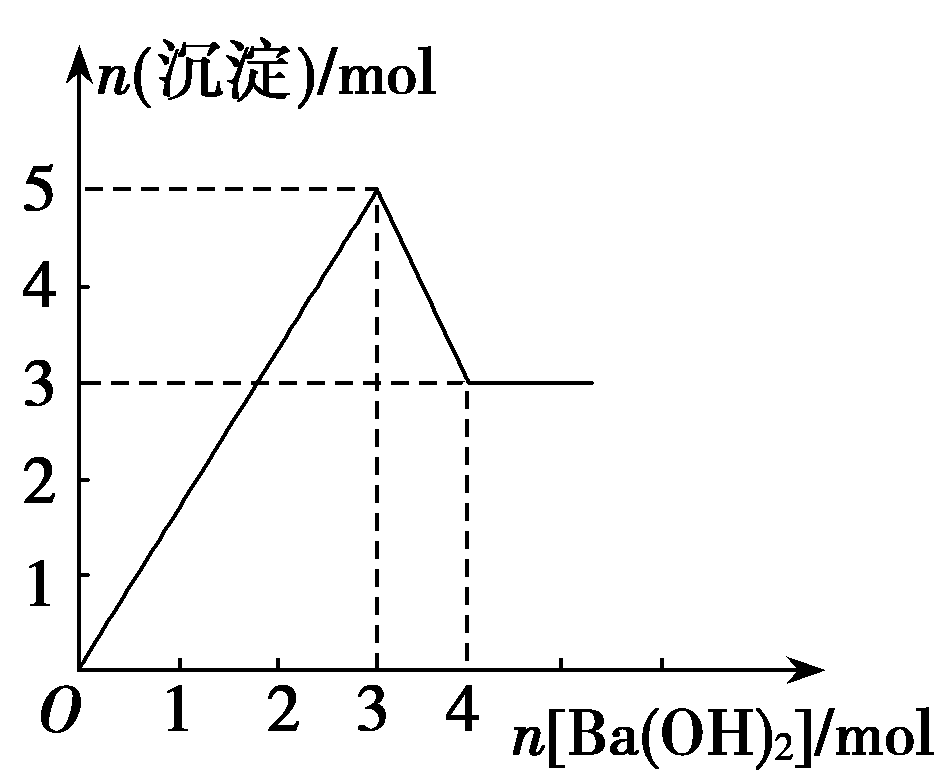 13.如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系。该溶液的成分可能是
13.如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系。该溶液的成分可能是
A.MgSO4
B.Al2(SO4)3
C.FeSO4
D.NaAlO2
14.下列溶液中Cl-的物质的量浓度最大的是
A.200mL 2mol/L MgCl2溶液
B.1000mL 2.5mol/L NaCl溶液
C.250mL 1mol/L AlCl3溶液
D.300mL 5mol/L KClO3溶液
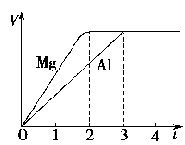 15.镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图。反应中镁和铝的
15.镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图。反应中镁和铝的
A.物质的量之比为3∶2
B.质量之比为3∶2
C.摩尔质量之比为2∶3
D.反应速率之比为2∶3
16.下列有关物质制备说法不正确的是
A.电解饱和食盐水制得Cl2B.电解熔融MgCl2制得金属Mg
C.高温下CO还原赤铁矿可用于炼铁 D.电解熔融AlCl3制得金属Al
17.FeCO3与砂糖混用可以作补血剂,实验室里制备FeCO3的流程如下图所示,下列说法不正确的是( )
A.可利用KSCN溶液检验FeSO4溶液是否变质
B.沉淀过程中有CO2气体放出
C.过滤操作的常用玻璃仪器有烧杯、漏斗和玻璃棒
D.产品FeCO3在空气中高温分解可得到纯净的FeO
18.下列装置所示的实验中,能达到实验目的的是
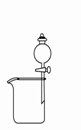
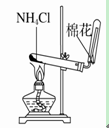
A. 分离碘酒中的碘和酒精 B. 实验室制氨气
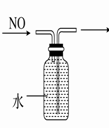
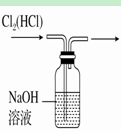
C.排水集气法收集NO D. 除去Cl2中的HCl
19.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验 | 现象 | 结论 |
| A | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| B | 将铜粉加1. 0mol·L-1Fe2(SO4)3溶液中 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
| C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| D | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
20.在80 g密度为dg·cm-3的硫酸铁溶液中,含有2.8 g Fe3+,则此溶液中SO的物质的量浓
度为(单位为mol·L-1)
A.15d/16B.5d/16C.3d/8D.5d/8
21.已知硫酸亚铁溶液中加入过氧化钠时发生反应:
4Fe2++4Na2O2+6H2O═4Fe(OH)3↓+O2↑+8Na+,则下列说法正确的是
A.该反应中FeSO4只做还原剂,Na2O2只做氧化剂
B.反应中氧化剂与还原剂的物质的量之比为3:5
C.该反应中由4 mol Fe2+还原的Na2O2是3 mol
D.4 mol Na2O2在反应中共得到8NA个电子
第Ⅱ卷(填空题 共58 分)
二、填空题(本题包括4小题,共58分)
22.(12分)某同学在实验室欲配制物质的量浓度均为1.0 mol/L的NaOH溶液、稀硫酸各450 mL。提供的试剂是:NaOH固体、98%的浓硫酸(密度为1.84 g/cm3)和蒸馏水。
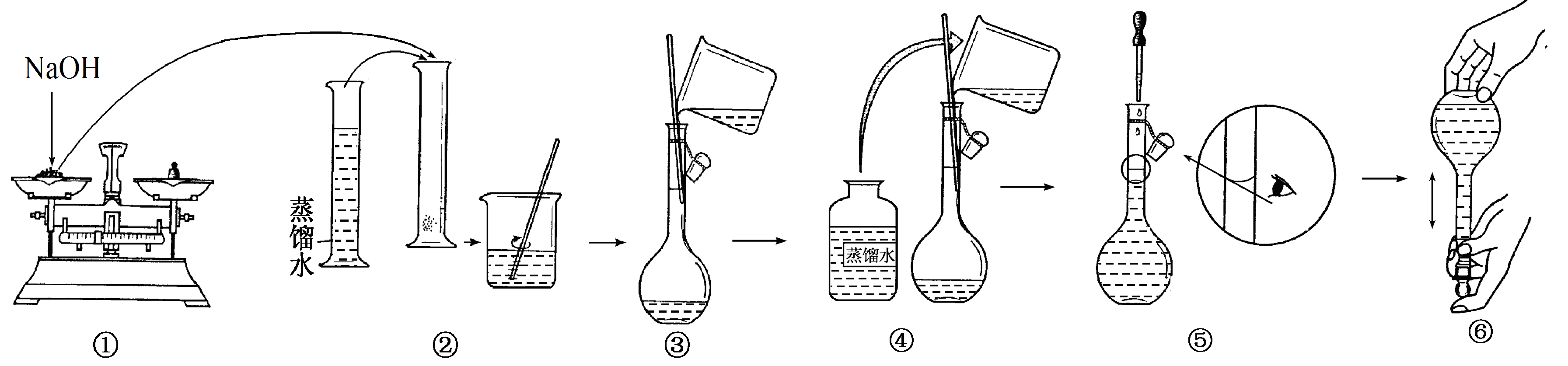
(1)请你观察图示判断其中不正确的操作有________(填序号)。
(2)应用托盘天平称量NaOH g,应用量筒量取浓硫酸________mL。
(3)浓硫酸溶于水的正确操作方法是_____________________________。
(4)在配制上述溶液实验中,下列操作引起结果偏低的有________。
A.该学生在量取浓硫酸时,俯视刻度线
B.溶解硫酸后没有冷却至室温就立即完成后面的配制操作
C.在烧杯中溶解搅拌时,溅出少量溶液
D.没有用蒸馏水洗涤烧杯2~3次,并将洗液移入容量瓶中
E.将量筒洗涤2~3次,并全部转移至容量瓶中
F.容量瓶中原来存有少量蒸馏水
G.胶头滴管加水定容时俯视刻度
(5) 若用0.010 00 mol·L-1K2Cr2O7溶液滴定 20.00 mL未知浓度的含Fe2+的溶液,恰好完全反应时消耗10.00 mL K2Cr2O7溶液,则溶液中Fe2+的物质的量浓度是 。(已知:6Fe2++Cr2O+14H+===2Cr3++6Fe3++7H2O)
23.(16分)已知A、B、C、D、E、G、H、I均为气体,G可使湿润红色石蕊试纸变蓝,J为常见的液态物质,A、B、C、I、M为单质,且M为常见金属,G和H相遇时产生白烟,它们存在如下的转化关系(图中部分反应物或产物已省略),请回答有关问题:
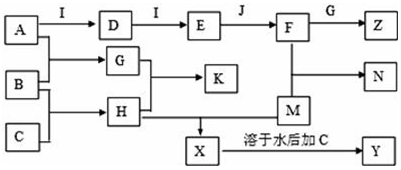
(1)请写出:A物质的化学式: ;
(2)①写出实验室用K制取G的化学方程式 ;
②实验室检验气体G是否收集满的方法: ;
③G与H相遇可生成白烟K,请写出该反应的化学方程式 .
(3)①F的浓溶液与木炭反应的化学方程式为 ;
②工业F的浓溶液呈黄色,试用化学方程式解释原因: ;
若要消除黄色可向其中通入一定量的 .
24.(14分)某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离
子的物质的量浓度相等,均为0.1mol/L。
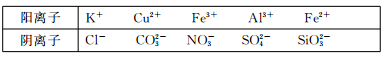
甲同学欲探究废水的组成,进行了如下实验:
I.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由I、Ⅱ判断,溶液中一定不含有的阳离子是____________________(写离子符号)。
(2)Ⅲ中加入少量盐酸生成无色气体的的离子方程式是___________________________。
(3)将Ⅲ中红棕色气体(标况下)收集一满试管然后倒扣入水中(假设溶质不扩散),所得溶液的物质的量浓度为_______________mol/L(精确到千分位)。
(4)甲同学最终确定原溶液中所含阳离子是___________,阴离子是__________。(写离子符号)
(5)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体为 质量为______________g。
25.(16分)某课外活动小组探究镁与CO2、NO2的反应。
(1)实验发现点燃的镁条能在CO2气体中继续燃烧,产生黑、白两种固体,请用化学反应方程式解释该现象 。
(2)该小组采用类比Mg与CO2反应的思路对Mg与NO2的反应进行预测:写出Mg与NO2反应的化学方程式 。
(3)设计实验验证猜测(用于连接玻璃管的乳胶管均内衬锡纸)
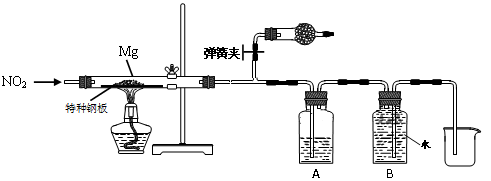
资料信息:2NO2 + 2NaOH = NaNO3 + NaNO2 + H2O
① 装置A中的试剂是 。
② 干燥管作用是 ,
装置B的作用是 。
③ 实验开始时正确的操作步骤是 → → → 。
a.通入NO2b.打开弹簧夹
c.点燃酒精灯 d.当硬质玻璃管充满红综色气体后,关闭弹簧夹
(4)实验结束时,同学们观察到与预测相符合的现象,但当用水洗涤硬质玻璃管时,固体遇水产生有刺激性气味的气体,该气体能使湿润的红色石蕊试纸变蓝。
① 同学们认为硬质玻璃管中还发生了另一个反应,该反应的方程式为 。
② 请用化学方程式解释加水产生该气体的原因 。
一、选择题
1—5 CCADD 6—10 ABABB 11—15 DCBAA 16—20 DDCAA 21 B
二、填空题
22.(12分) (1) ①②⑤ (2分,漏选得1分,错选不得分)
(2) 20.0 (2分) 27.2 (2分)
(3)先在烧杯中倒入适量水,然后将浓硫酸沿烧杯内壁慢慢倒入,并用玻璃棒搅拌(2分)
(4) A、C、D (2分,漏选得1分,错选不得分)(5) 0.03 mol·L-1(2分)
23.(16分)(1)N2;
(2)①2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
②用湿润的红色石蕊试纸靠近于集气瓶口,如果红色石蕊试纸变蓝,则说明收集满;
③NH3+HCl═NH4Cl;
(3)①C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
②4HNO3(浓)![]() 4NO2↑+O2↑+2H2O; 氧气(每空2分)
4NO2↑+O2↑+2H2O; 氧气(每空2分)
24. (共14分,每空2分)
(1)K+ Fe3+(答对一个得1分,出现错误不得分)
(2)3Fe2+ + NO3- + 4H+ = 3Fe3+ + NO↑+ 2H2O (3)0.045
(4)Fe2+ Cu2+ (答对一个得1分,出现错误不得分)
Cl-、 NO3- SO42-(答对两个得1分,出现错误不得分)
(5)CuO Fe2O31.6 (每空2分)
25.(16分)
(1)2Mg + CO2![]() 2MgO + C (2分)
2MgO + C (2分)
(2)4Mg +2NO2![]() 4MgO + N2(2分)
4MgO + N2(2分)
(4)① 3Mg + N2![]() Mg3N2(或7Mg +2NO2
Mg3N2(或7Mg +2NO2![]() 4MgO +Mg3N2)(2分)
4MgO +Mg3N2)(2分)
② Mg3N2+ 6H2O = 3Mg(OH)2+ 2NH3↑(2分)