
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
紫荆中学2016—2017学年高三第二次模拟试题(卷)
化学高三化学备课组
第Ⅰ卷选择题(每小题只有一个正确答案25×2′)
2.下列说法正确的是 ( )
A.明矾净水过程中不涉及化学变化
B.金属与盐溶液反应都是置换反应
C.化合反应一定有单质参加反应
D.石油分馏和碘的升华都是物理变化
3.化学用语是表示物质组成、结构和变化规律的一种具有国际性、科学性和规范性的书面语言。化学用语具有简便、确切地表达化学知识和化学科学思维的特点。下列化学用语中,书写错误的是 ( )
A.过氧化钠的电子式Na+[:O:O:]2-Na+
资*源%库 B.CO2的电子式:![]()
C.12753I和12953I2互为同位素
D.硫离子的结构示意图: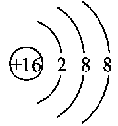
4. 在下述条件下,一定能大量共存的离子组是( )
A.无色透明的水溶液中:K+、Ba2+、Cu2+、I-
B.含有大量H+的水溶液中:NH4+、Fe2+、SO42-、MnO4-
C.c(HCO3-)=0.1mol/L的溶液中:Na+、K+、CO32-、Br-
D.强碱性溶液中:Cl-、SO32-、HSO3-、Na+
5. 列有关化学键的叙述,正确的是( )
A.离子化合物中一定含有离子键
B.单质分子中均不存在化学键
C.含有极性键的分子一定是极性分子D.含有共价键的化合物一定是共价化合物
6. 用NA表示阿佛加德罗常数,下列说法中正确的是
A.标准状况下,将22.4L氯化氢溶于足量水中,溶液中含有的HCl分子数为NA
B.常温常压下,16g14CH4所含中子数目为8NA
C.常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA
D.标准状况下,22.4L空气含有NA个单质分子
7.下列由相关实验现象所推出的结论正确的是
A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性
B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42-
C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应
D.分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水
8.为了检验某含有![]() 杂质的
杂质的![]() 样品的纯度,现将
样品的纯度,现将![]() 克样品加热,其质量变为
克样品加热,其质量变为![]() g,,则该样品的纯度(质量分数)是
g,,则该样品的纯度(质量分数)是
A.![]() B.
B.![]()
C.![]() D.
D.![]()
9.Fe2O3、ZnO、CuO的固体混合粉末a g,在加热条件下用足量CO还原,得到金属混合物4.82g,将生成的CO2气体用足量的澄清石灰水吸收后,产生l0.00g白色沉淀,则a 的数值为( )
A.4.92B.6.42C.7.18D.14.82
10.下列离子方程式书写正确的是( )
$来&源:A.氯气溶于水:Cl2+H2O===2H++Cl-+ClO-
B.硫酸铝溶液中加入足量氨水:Al3++4OH-===AlO+2H2O
C.FeSO4溶液与稀硝酸反应:3Fe2++NO+4H+===3Fe3++NO↑+2H2O
D.碳酸氢铵和足量氢氧化钠溶液反应:NH+OH-===NH3·H2O
11.下列各组离子因发生氧化还原反应而不能大量共存的是( )A.H+、Fe2+、Cr2O、SO
B.Ca2+、H+、SO、HCO
C.Na+、Cu2+、Cl-、S2-
D.Fe3+、K+、SCN-、Cl-
12.在由水电离产生的H+的浓度为1×10-13mol/L的溶液中,一定能大量共存的离子组是( )
①K+、Cl-、NO、S2- ②K+、Fe2+、I-、SO
③Na+、Cl-、NO、SO ④Na+、Ca2+、Cl-、HCO ⑤K+、Ba2+、Cl-、NO
A.①③B.③⑤
C.③④D.②⑤
13.下列离子方程式中,不正确的是( )
A.向Mg(HCO3)2溶液中加入过量的NaOH溶液:
Mg2++2HCO+4OH-===Mg(OH)2↓+2CO+2H2O
B.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO反应完全:
2Ba2++4OH-+Al3++2SO===2BaSO4↓+AlO+2H2O
C.FeBr2溶液中通入过量的Cl2:2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-
D.向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO===3Fe3++NO↑+2H2O
14.物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
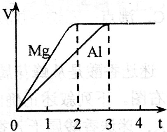 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图。反应中镁和铝的
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图。反应中镁和铝的 A.原合金质量为0.92 g
A.原合金质量为0.92 g第Ⅱ卷(非选择题,共50分)
26.有A、B、C、D四种化合物,它们分别由K+、Ba2+、SO、CO、OH-、SO离子中的两种组成,它们具有下列性质:
①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无刺激性气味的气体;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出的气体E可使溴水褪色。
(1)写出化学式:A.________、B.________、C.________、D.________、E.________。
资*源%库 (2)写出离子方程式:
资*源%库 B+盐酸______________________________________________________________;
C+硫酸______________________________________________________________;
D+硫酸______________________________________________________________;
E+溴水______________________________________________________________。
27.常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO、SO、CO,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题。 (1)五种盐中,一定没有的阳离子是________;所含阴离子相同的两种盐的化学式是________________________________________________________________________。
(2)D的化学式为________,D溶液显碱性的原因是(用离子方程式表示)______________________________________________________________________。
(3)A和C的溶液反应的离子方程式是__________________________________________。
E和氨水反应的离子方程式是________________________________________________。
(4)若要检验B中所含的阳离子,正确的实验方法是
________________________________________________________________________
________________________________________________________________________。
28.某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1 mol/L。
| 阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl- CO NO SO SiO |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是____________________(写离子符号)。
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式是
__________________________________ ______________________________________。
(3)将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为________________________________________________________________________。
(4)甲同学最终确定原溶液中所含阳离子是________,阴离子是________________(写离子符号)。
资*源%库 (5)另取100 mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为________g。
29.有一瓶澄清的溶液,其中可能含有NH、K+、Ba2+、Al3+、Fe3+、I-、NO、CO、SO、AlO。取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性;
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色;
③另取溶液适量,逐滴加入NaOH溶液;
a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;c.沉淀完全溶解;d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝;④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)由①可以排除________________________的存在。
(2)由②可以证明________的存在;同时排除____________________________________
________的存在,理由是_________________________________________________。 (3)由③可以证明________________的存在;写出c、d所涉及的化学方程式,是离子反应的用离子方程式表示:
c________________;d________________。
(4)由④可以排除________的存在,同时证明________的存在。
30向27.2Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO 和Cu(NO3)2.在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g,请列式计算
(1)Cu与Cu2O 的物质的量之比 ?
(2)硝酸的物质的量浓度?