
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2017长安一中高三模拟考试理科综合化学试题(4月)
可能用到的相对原子质量:H -1 B-11 C -12 N- 14 O -16 Na-23 Mg-24
S -32 I-127
7.下列说法都正确的是( )
① 生活中使用频率很高的一元纸币将逐步被硬币替代,硬币是合金
② 江河入海口三角洲的形成通常与胶体的性质有关
③ “钡餐”中使用的硫酸钡是弱电解质
④ 太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置
⑤ 常用的自来水消毒剂有氯气和H2O2,两者都含有极性键
⑥ 水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物
A.①②③④ B. ①②④⑥ C.①②⑤⑥ D.③④⑤⑥
8.设NA为阿伏加德罗常数的值.下列说法正确的是( )
9.化学反应终点的判断是化学定量实验的重要环节。下列对化学反应终点的判断不正确的是( )
A.向BaCl2溶液中加入足量Na2CO3溶液后,静置,向上层清液中继续滴加Na2CO3溶液,
若无沉淀,说明Ba2+已经完全沉淀
B.淀粉在稀硫酸的作用下水解后,加NaOH溶液使溶液呈碱性,加入新制Cu(OH)2,加
热,若有砖红色沉淀生成,说明淀粉已经完全水解
C.将Na2SO4·10H2O晶体置于坩埚中加热,称量,并重复上述操作,若相邻两次称量的
结果相同,说明硫酸钠已全部失去结晶水
D.用酸式滴定管向滴有酚酞的NaOH溶液中滴加HCl溶液,若滴入最后一滴HCl溶液后
红色刚好褪去,且30s内颜色不复原,说明NaOH已被完全中和
10.X、Y、Z、W、R属于短周期主族元素。X的原子半径在短周期主族元素中最大,Y核素的最外层电子数为m,次外层电子数为n, Z原子的L层电子数为m+n, M层电子数为m-n≠0 , W与Z同主族,R与Y的核外电子数之比为2:1,下列叙述错误的是( )$来&源:
11.下列关于有机物的说法正确的是( )
12.工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的
是( )
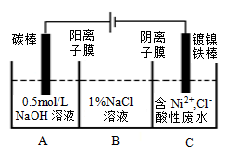
已知:放电顺序:Ni2+(高浓度)>H+>Ni2+(低浓度)
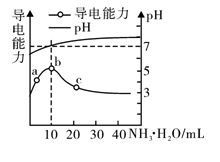
13.常温下,向10mL 0.1mol·L-1的HR溶液中逐渐滴入0.1mol·L-1的NH3·H2O溶液,所得溶液pH及导电能力变化如图。下列分析不正确的是( )
26.(14分)氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体,可用于化肥、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵:
反应式:2NH3(g)+CO2(g)![]() H2NCOONH4△H<0
H2NCOONH4△H<0
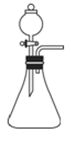
(1)如果使用如图所示的装置制取NH3,你所选择的试剂是_____________。
(2)制备氨基甲酸铵的装置如下图。把氨和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中,当悬浮物较多时,停止制备:(注:四氯化碳与液体石蜡均为惰性介质。)

发生反应的仪器名称是_______________。
②从反应后的混合物中过滤分离出产品。为了得到干燥产品,应采取的方法是_____ (选填序号)
a.常压加热烘干 b.高压加热烘干 c.真空40℃以下烘干
(3)尾气有污染,可用________溶液吸收处理。
(4)取因部分变质而混有碳酸氢铵的氨基甲酸铵钱样品1.1730g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.500g。样品中氨基甲酸铵的质量分数为__________。[己知Mr(H2NCOONH4)=78, Mr(NH4HCO3)=79, Mr(CaCO3)=100]
27.(14分)已知:硼镁矿主要成分为Mg2B2O5·H2O,硼砂的化学式为Na2B4O7·10H2O。利用硼镁矿制取金属镁及粗硼的工艺流程为:
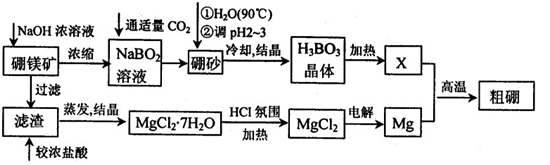
回答下列有关问题:
(1)硼砂中B的化合价为 ,将硼砂溶于热水后,常用稀H2SO4调pH=2~3制取H3BO3,该反应的离子方程式为 。
(2)MgCl2·7H2O需要在HCl氛围中加热,其目的是 。若用惰性电极电解MgCl2溶液,其阴极反应式为 。
(3)镁-H2O2酸性燃料电池的反应原理为 Mg+H2O2+2H+===Mg2++2H2O, 则正极反应式为: 。常温下,若起始电解质溶液pH=1,则pH=2时,溶液中Mg2+浓度为______。当溶液pH=6时, (填“有”或“没有”)Mg(OH)2沉淀析出(已知Ksp[Mg(OH)2]=5.6×10-12)。
(4)制得的粗硼在一定条件下生成BI3,BI3加热分解可以得到纯净的单质硼。现将0.020 g粗硼制成的BI3完全分解,生成的I2用0.30 mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液18.00 mL。该粗硼样品的纯度为_______(提示:I2+2S2O32-===2I-+S4O62-)(结果保留一位小数)。
28.(15分)亚硝酰氯(NOCl)是有机合成中的重要试剂。可通过反应制得:
NO(g)+Cl2(g)![]() 2ClNO(g)
2ClNO(g)
(1)氮氧化物与悬浮在大气的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
①2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K1
NaNO3(s)+ClNO(g) K1
②4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K2
2NaNO3(s)+2NO(g)+Cl2(g) K2
③2NO(g)+Cl2(g)![]() 2ClNO(g) K3
2ClNO(g) K3
则K3=___________(用K1和K2表示)
(2)300℃时,2NO(g)+Cl2(g)![]() 2ClNO(g)的正应速率表达式为v正=k•cn(ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正应速率表达式为v正=k•cn(ClNO),测得速率和浓度的关系如下表:
| 序号 | c (C1NO) /(mol/L) | v/(×10-8mol·L·s) |
| ① | 0.30 | 0.36 |
| ② | 0.60 | 1.44 |
| ③ | 0.90 | 3.24 |
n=____________;k=_____________。
(3)按投料比[n(NO) ∶n(Cl2)]=2∶1把NO和Cl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强P(总压)的关系如图A所示:
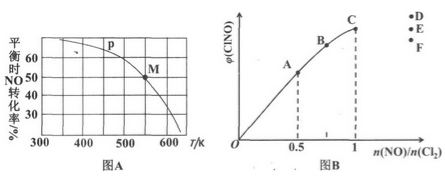
①该反应的△H_______0(填“>”“<”或“=”)
②在P压强条件下,M点时容器内NO的体积分数为_________________。
③若反应一直保持在P 压强条件下进行,则M点的分压平衡常数Kp=________(用含P的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
(4)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2 (g),平衡时ClNO的体积分数随n(NO) /n(Cl2)的变化如图B,则A、B、C三状态中NO的转化率最大的是__________;当n(NO) /n(Cl2)=1.5时,达到平衡状态C1NO的体积分数可能是D、E、F三点中的_________点。
35.(15分)【选修三-物质结构】将汽车尾气中含有的CO利用不仅能有效利用资源,还能防治空气污染。工业上常用CO与H2在由Al、Zn、Cu等元素形成的催化剂作用下合成甲醇。
(1)右图是某同学画出CO分子中氧原子的核外电子排布图,
![]()
请判断该排布图 (填“正确”或“错误”),理由是 (若判断正确,该空不用回答)。
(2)写出两种与CO互为等电子体的离子 。
(3)向CuSO4溶液中加入足量氨水可得到深蓝色[Cu(NH3)4]SO4溶液,[Cu(NH3)4]SO4中 所含配位键是通过配体分子的 给出孤电子对, 接受电子对形成,SO42-的空间构型是 ,该物质中N、O、S三种元素的第一电离能大小顺序为 > >(填元素符号)。
(4)甲醇与乙烷的相对分子质量相近,故二者分子间的作用力(范德华力)相近,但是二者沸点的差距却很大,造成该差异的原因是 ;在甲醇分子中碳原子轨道的杂化类型为 。
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图所示:
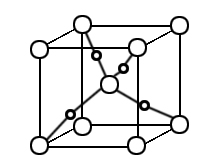
①在该晶胞中,Cu+的配位数是 ,
②若该晶胞的边长为a pm,则Cu2O的密度为________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
36.(15分)【选修五-有机化学基础】
铃兰醛()具有甜润的百合香味,对皮肤的刺激性小,对碱稳定,广泛用于百合、丁香、玉兰、茶花以及素心兰、东方型香型日用香精的合成。常用作肥皂、洗涤剂的香料,还可用作花香型化妆品的香料。其合成路线如下图所示:
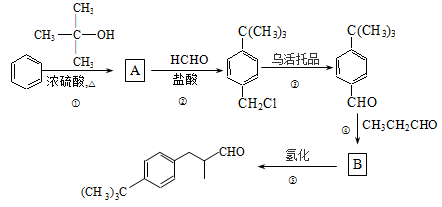
(1)B中官能团的名称是________________;
(2)①的反应类型是__________________;
(3)写出反应②的化学方程式___________________________________________;
(4)乌洛托品的结构式如图所示,其二氯取代物有____________种;
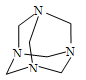
将甲醛的水溶液与氨水混合蒸发可制得乌洛托品,该反应的化学方程式是: __________________________________________________________________;
(5)写出满足下列条件的A的同分异构体____________________________
I.有两个取代基; II.取代基在邻位。
(6)已知:RCH2COOH![]() RCHClCOOH。仿照上述流程,写出以CH3CH2CHO为原料制备聚乳酸(
RCHClCOOH。仿照上述流程,写出以CH3CH2CHO为原料制备聚乳酸(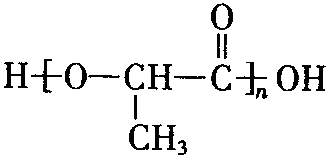 )的合成路线流程图(无机试剂可以任选):
)的合成路线流程图(无机试剂可以任选):
CH3CH2CHO—→_____________________________________________________________。
2017长安一中高三模拟考试理科综合化学答题纸(4月)
班级______________姓名______________学号_____________
26.(14分)
(1)试剂是_____________。
(2)①原因是_______________________________________________________,
作用是_______________________________________________________,
发生反应的仪器名称是_______________。
②_____ (选填序号)
(3)可用___________________溶液吸收处理。
(4)样品中氨基甲酸铵的质量分数为__________________。
27(14分)
(1)硼砂中B的化合价为 ,
该反应的离子方程式为___________。
(2)目的是_________________________________________________。
阴极反应式为________。
(3)正极反应式为:____________________。
Mg2+浓度为______________。 (填“有”或“没有”)
(4)该粗硼样品的纯度为________________________ (结果保留一位小数)。
28.(15分)
(1)K3=___________(用K1和K2表示)
(2)n=____________;k=_____________。
(3)①△H_______0(填“>”“<”或“=”)
②在P压强条件下,M点时容器内NO的体积分数为_________________。
③Kp=_____________________(用含P的表达式表示)。
(4)则A、B、C三状态中NO的转化率最大的是__________;
可能是D、E、F三点中的_________点。
35.(15分)【选修三-物质结构】
(1) (填“正确”或“错误”),
理由是___________________(若判断正确,该空不用回答)。
(2)
(3) 给出孤电子对, 接受电子对形成,SO42-的空间构型是 ,该物质中N、O、S三种元素的第一电离能大小顺为:
> >(填元素符号)。
(4)原因是_________________________________________;
__________。
(5)① ,
②密度为_________________________________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
36.(15分)【选修五-有机化学基础】
(1)_____________________________;
(2)__________________;
(3)___________________________________________________________________;
(4)____________种;____________________________________________________;
(5)____________________________________________________________________
(6)CH3CH2CHO—→_____________________________________________________________。
2017长安一中高三模拟考试理科综合化学参考答案
| 题号 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 | B | C | B | B | D | D | C |
26.(14分)
⑴浓氨水与NaOH固体(或CaO、碱石灰)
⑵①降低温度,提高反应物的转化率;通过观察气泡,调节NH3与CO2通入比例;三颈烧瓶; ②c
⑶稀硫酸 ⑷80%
27.(14分)
(1)+3;B4O72-+2H++5H2O=4H3BO3;
(2)抑制MgCl2的水解;2H2O+Mg2++2e-=H2↑+Mg(OH)2↓;
(3)H2O2+2H++2e- = 2H2O;0.045mol·L-1;没有;
(4) 97.2%;
28.(15分)
(1)K12/K2
(2)2; 4.0×10-8L·mol-1·s-1;
(3)①<; ②40%; ③Kp=5/P;
(4)A;D
35.(15分)
(1)错误;违背泡利原理
(2)CN-、C22-;
(3)氮原子(或N);Cu2+;正四面体;N>O>S;
(4)甲醇分子间存在氢键,因此其沸点远大于乙烷;sp3;
(5)① 2;②(16×2+64×4)×1030/(a3NA)
36.(15分)
(1)醛基,碳碳双键
(2)取代反应
(3)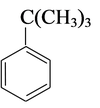 +HCHO+HCl—→
+HCHO+HCl—→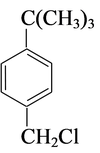 +H2O
+H2O
(4)3; 6HCHO+4NH3—→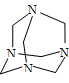 +6H2O
+6H2O
(5)![]() 、
、![]() 、
、![]()
(6)CH3CH2CHO![]() CH3CH2COOH
CH3CH2COOH![]() CH3CHClCOOH
CH3CHClCOOH![]() CH3CHOHCOOH
CH3CHOHCOOH![]()

高三模拟考试理科综合化学试题答案(4月23日)
| 题号 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 | B | C | B | B | D | D | C |
26.(14分)
⑴浓氨水与NaOH固体(或CaO、碱石灰)
⑵①降低温度,提高反应物的转化率;通过观察气泡,调节NH3与CO2通入比例;三颈烧瓶; ②c
⑶稀硫酸 ⑷80%
27.(14分)
(1)+3;B4O72-+2H++5H2O=4H3BO3;
(2)抑制MgCl2的水解;2H2O+Mg2++2e-=H2↑+Mg(OH)2↓;
(3)H2O2+2H++2e- = 2H2O;0.045mol·L-1;没有;
(4) 99.0%;
28.(15分)
(1)K12/K2
(2)2; 4.0×10-8L·mol-1·s-1;
(3)①<; ②40%; ③Kp=5/P;
(4)A;D
35.(15分)
(1)错误;违背泡利原理
(2)CN-、C22-;
(3)氮原子(或N);Cu2+;正四面体;N>O>S;
(4)甲醇分子间存在氢键,因此其沸点远大于乙烷;sp3;
(5)① 2;②(16×2+64×4)×1030/(a3NA)
36.(15分)
(1)醛基,碳碳双键
(2)取代反应
(3) +HCHO+HCl—→
+HCHO+HCl—→ +H2O
+H2O
(4)3; 6HCHO+4NH3—→ +6H2O
+6H2O
(5)![]() 、
、![]() 、
、![]()
(6)CH3CH2CHO![]() CH3CH2COOH
CH3CH2COOH![]() CH3CHClCOOH
CH3CHClCOOH![]() CH3CHOHCOOH
CH3CHOHCOOH![]()
