
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
化学试题
相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 Ca 40
Fe 56 Cu 64
一、选择题(每小题只有一个正确答案, 每小题2分,共40分)
1.化学在生产和日常生活中有着重要的作用。下列有关说法正确的是
A.福尔马林可作食品的保鲜剂
B.氢氧化铁溶胶、水玻璃、淀粉溶液、PM2.5微粒均具有丁达尔效应
C.“地沟油”经过加工处理后,可以用来制肥皂和生物柴油
D.浓硫酸可刻蚀石英制艺术品
2.下列实验装置或操作正确的是
| A | B | C | D |
向容量瓶中转移液体 | 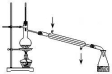 实验室制取蒸馏水 | 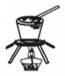 从饱和食盐水中提取NaCl晶体 | 分离酒精和水 |
3.下列说法不正确的是
A.氧化镁用作耐火材料
B.向Na2CO3溶液中滴加醋酸溶液,一定有CO2气体生成
C.明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
D.Na2O2常用于潜水艇或呼吸面具的供氧剂
4.下列叙述正确的是资*源%库
A.浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体
B.CH3COONa溶液中滴加少量浓盐酸后c(CH3COO-)减小
C. 氯化铵、次氯酸都属于强电解质
D. 漂白粉、石英都属于纯净物
5.设NA为阿伏加德罗常数的值。下列叙述正确的是
A.1mol甲苯含有6NA个C-H键
B.12 g石墨和C60的混合物中质子总数一定为6NA个
C.25℃,pH=12的Na2CO3溶液中含有CO32-的数目为0.01NA
D.56g铁片投入足量浓硫酸中生成NA个SO2分子
6. 下列关于同温同压下的两种气体12C18O和14N2的判断正确的是
7.在一定条件下,某化合物X受热分解:2X== A↑+2B↑+4C↑,测得反应后生成的混合气体对H2的相对密度为11.43,在相同条件下,X的相对分子质量是
A.11.43 B.22.85 C.80.01 D.160.02
8.在①大气固氮;②硝酸银分解;③实验室制取氨气等变化中,按氮元素被氧化、被还原、既不被氧化又不被还原的顺序排列,正确的是资*源%库
A.①②③ B.②①③
C.③②① D.③①②
9. R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表。已知:J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素。下列说法错误的是 ( )
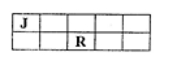 A.J和氢组成的化合物分子有多种
A.J和氢组成的化合物分子有多种
B.工业上不用电解M和T组成的化合物来制备M
C.R、T两元素的气态氢化物中,R的气态氢化物更稳定
D.J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是HTO4
10. 将盐酸逐滴滴入NaOH、NaAlO2、Na2CO3的混合溶液中,下列图像能正确表示溶液中反应的是
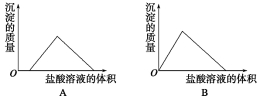
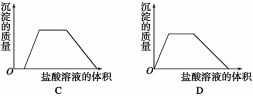
![]()
11. 四联苯的一氯代物有
A.3种 B.4种 C.5种 D.6种
12.图示为一种天然产物,具有一定的除草功效,下列有关该化合物的说法正确的是
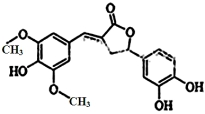
A.分子中含有三种官能团
B.1 mol 该化合物最多能与6 mol NaOH 反应
C.既可以发生取代反应,又能够发生加成反应
D.既能与FeCl3发生显色反应,也能和NaHCO3反应放出CO2
13.下列各组离子中,在给定条件下能够大量共存的是
A.通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、CO32-
B.无色溶液中:Mg2+、MnO4-、SO42-、K+
C.酸性溶液中可能大量存在Na+、ClO‾、SO42‾、I‾
D.c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl-
14.下列离子方程式正确的是
A.0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合
NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
B.100ml 0.1mol/L FeI2溶液与标况下0.224L Cl2: 2Fe2++ Cl2=2Fe3++2Cl-
C.NH4HCO3溶液与过量NaOH溶液共热:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
D.浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+![]() Fe3++3NO2↑+3H2O
Fe3++3NO2↑+3H2O
15. 根据表中信息判断,下列选项错误的是
| 序列 | 参加反应的物质 | 生成物 |
| KMnO4、H2O2、H2SO4 | K2SO4、MnSO4…… | |
| Cl2、FeBr2 | FeCl3、FeBr3 | |
| MnO4-…… | Cl2、Mn2+…… |
A.第①组反应的其余产物为H2O和 O2
B.第②组反应中Cl2与 FeBr2的物质的量之比为1︰2
C.第③组反应中生成1mol Cl2,转移电子2mol
D.氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2
16.已知1.5克NaOH和1.6克S 混合后加热,恰好发生如下反应:
aNaOH + bS → cNa2Sx + dNa2S2O3 + eH2O,则x的值为
A.4 B.3 C.2 D.1
17.下列物质的转化在给定条件下能实现的是
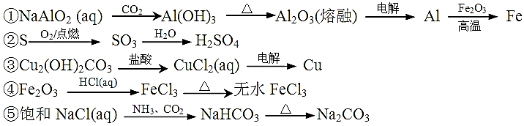
A.①③⑤ B.②③④
C.②④⑤ D.①④⑤
18.某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知有关原溶液中离子的说法不正确是
A.至少存在4种离子
B.Cl-一定存在,且c(Cl-)≥0.4mol/L
C.SO42-、NH4+一定存在
D.CO32-、Al3+、K+一定不存在
19.C和CuO在一定温度下反应,产物有Cu、Cu2O、CO、CO2。将1.20 g C跟16.0 g CuO混合,
隔绝空气加热,将生成的气体全部通过足量的澄清石灰水,反应一段时间后共收集到1.12 L气体
(标准状况),生成沉淀的质量为5.00 g。下列说法不正确的是
A.反应后的固体混合物中不含碳
B.反应后的固体混合物总质量为13.6 g
C.反应后的固体混合物中氧化物的物质的量为0.05 mol
D.反应后转移电子数为0.4NA
20.a molNa2O2和b molNaHCO3固体混合后,在密闭容器中加热到250℃,使其充分反应,当排
出气体为两种气体时, a:b不可能为
A.3:4 B.4:5
C.2:3D.3:2
二、非选择题(共60分)
21.(11分) 人体血液里Ca2+离子的浓度一般采用g/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度:
【配制KMnO4标准溶液】下图是配制50mLKMnO4标准溶液的过程示意图。
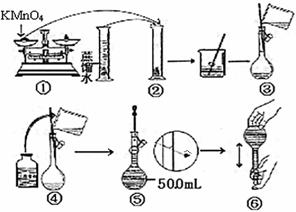
(1)上述过程中有两处错误,请你观察图示判断其中不正确的操作是(填序号)____________;
(2)其中确定50mL溶液体积的容器是(填名称)__________________;如果按照图示的操作配制溶液,所得的实验结果将____________(填偏大或偏小)。
【测定血液样品中Ca2+的浓度】抽取血样20.00mL,经过上述处理后得到草酸,再用硫酸酸化的0.020mol/L KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液。
(3)滴定时,盛放高锰酸钾溶液的仪器名称为 ,确定反应达到终点的现象_____________________________。
(4)草酸跟酸性KMnO4溶液反应的离子方程式为: 。
(5)根据所给数据计算血液样品中Ca2+离子的浓度为________mg/cm3。
22.(15分)研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知Fe2O3(s)+ 3C(s)=2Fe(s)+ 3CO(g) ΔH1=+489.0 kJ·mol-1,
C(s) +CO2(g)=2CO(g) ΔH2=+172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为 。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。
写出该电池的负极反应式: 。
(3)CO2和H2充入一定体积的密闭容器中,在两种温度
下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
测得CH3OH的物质的量随时间的变化见图。
![]()
![]()
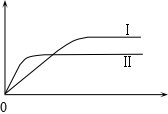
![]() ①曲线I、Ⅱ对应的平衡常数大小关系为KⅠKⅡ
①曲线I、Ⅱ对应的平衡常数大小关系为KⅠKⅡ
(填“>”或“=”或“<”)。
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | amolCO2、bmolH2、 cmolCH3OH(g)、cmolH2O(g) |
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。$来&源:
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为 。
③一定温度下,此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是 。$来&源:
a.容器中压强不变 b.H2的体积分数不变 c.c(H2)=3c(CH3OH)
d.容器中密度不变 e.2个C=O断裂的同时有6个H-H断裂
(4)将燃煤废气中的CO2转化为二甲醚的反应原理为:
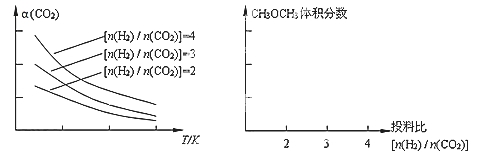
2CO2(g) + 6H2(g)![]() CH3OCH3(g) + 3H2O(g)。已知一定条件下,该反应中CO2的平衡转化率随温度、投料比[n(H2) / n(CO2)]的变化曲线如下左图。在其他条件不变时,请在右图中画出平衡时CH3OCH3的体积分数随投料比[n(H2) / n(CO2)]变化的曲线图
CH3OCH3(g) + 3H2O(g)。已知一定条件下,该反应中CO2的平衡转化率随温度、投料比[n(H2) / n(CO2)]的变化曲线如下左图。在其他条件不变时,请在右图中画出平衡时CH3OCH3的体积分数随投料比[n(H2) / n(CO2)]变化的曲线图
23.(14分)二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料.现在工业由以下两种方法制备二氧化钛:
方法1:可用含有Fe2O3、SiO2的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要工艺流程如下:
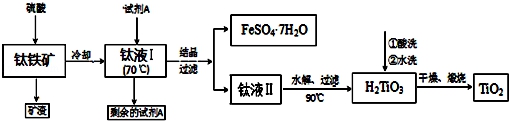
已知有关反应包括:酸溶FeTiO3(s)+2H2SO4(aq)==FeSO4(aq)+TiOSO4(aq)+2H2O(l)水解TiOSO4(aq)+2H2O(l)==H2TiO3(s)+H2SO4(aq)
(1)试剂A为 ,钛液Ⅰ需冷却至70℃左右,若温度过高会导致产品收率降低,原因是 ;
(2)取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现红色,说明H2TiO3中存在的杂质离子是 .这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2会略发黄,发黄的杂质是 (填化学式).
方法2:
Ⅰ.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应制得混有SiCl4杂质的TiCl4;
Ⅱ.将SiCl4分离,得到纯净的TiCl4;
Ⅲ.在TiCl4中加水、加热,水解得到沉淀TiO2•xH2O,洗涤和干燥;
IV.TiO2•xH2O高温分解得到TiO2.
(3)TiCl4水解生成TiO2•x H2O的化学方程式为 ;
(4)检验TiO2•x H2O中Cl﹣是否被除净的方法是 ;
金属钛被称为“21世纪金属”,工业制备金属钛是在800~900℃及惰性气体的保护下,在密闭反应器中,将TiCl4以一定的流速通入通电熔化的镁即可.主要涉及以下反应:
①TiO2+2Cl2+C![]() TiCl4+CO2
TiCl4+CO2
②TiCl4+2Mg→2MgCl2+Ti
(5)下列推断不合理的是
A.钛在高温下可能易与氧气反应
B.镁的熔点比钛的熔点高
C.钛的金属活动性比镁的金属活动性强
D.反应②产生的MgCl2可作为电解法制取镁的原料
24.(10分)(1)下列说法正确的是
A. 第一电离能大小:S>P>Si
B. 电负性顺序:C<N<O<F
C. 因为晶格能CaO比KCl高,所以KCl比CaO熔点低
D. SO2与CO2的化学性质类似,分子结构也都呈直线型,相同条件下SO2的溶解度更大
E. 分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
(2).图1是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体.
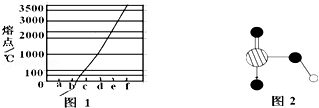
①图中d单质的晶体堆积方式类型是 .
②图2是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因: .
(3)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等.
①基态Fe3+的M层电子排布式为 .
②尿素(H2NCONH2)分子中C、N原子的杂化方式分别是 、 ;
③配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x= .
Fe(CO)x常温下呈液态,熔点为﹣20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断
Fe(CO)x晶体属于 (填晶体类型).
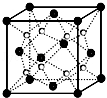 (4)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为 .已知该晶胞的密度为ρ g/cm3,阿伏加德罗常数为NA,求晶胞边长a= cm.(用含ρ、NA的计算式表示)
(4)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为 .已知该晶胞的密度为ρ g/cm3,阿伏加德罗常数为NA,求晶胞边长a= cm.(用含ρ、NA的计算式表示)
25.(10分)M为石油裂解最主要产物。高分子材料PET聚酯树脂和PMMA合成路线如下:
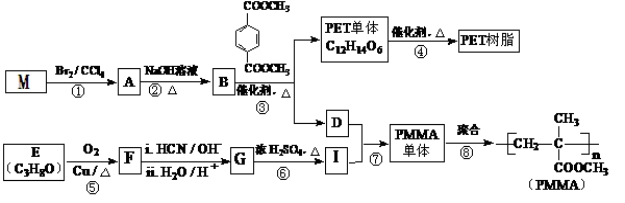
已知:Ⅰ. RCOOR’+ R’’18OH![]() RCO18OR’’+R’OH(R、R’、R’’代表烃基)
RCO18OR’’+R’OH(R、R’、R’’代表烃基)
![]()
![]() Ⅱ.
Ⅱ.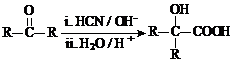 (R、R’代表烃基)
(R、R’代表烃基)
(1)M的结构简式是
(2)PMMA单体的官能团名称是
(3)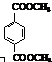 有多种同分异构体,同时满足下列条件的同分异构体有 种。
有多种同分异构体,同时满足下列条件的同分异构体有 种。
a:具有与该物质相同的官能团; b:苯环上的一氯取代物只有一种。
(4)下列说法正确的是 (填字母序号)
a. ②③④⑦为取代反应 b.E和D互为同系物
c.I能使酸性高锰酸钾液褪色,G不能 d. F的同分异构体一定能发生银镜反应
(5)写出由PET单体制备PET聚酯树脂并生成B的化学方程式
化学试题答卷
一、选择题(每小题只有一个正确答案, 每小题2分,共40分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | ||||||||||
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 |
二、非选择题(共6小题,合计60分)
21. (11分)
(1)____________;
(2)__________________; ____________。
(3)___________________, 。
(4) 。
(5)________ 。
22. (15分)
(1) 。
(2) 。
(3)![]() ① ② 。③ 。
① ② 。③ 。
 (4)
(4)
23.(14分)
(1) , ;
(2) , ;
(3) ;
(4) ;
(5)
24.(10分)(1)
(2)① .
② .
(3)① .② 、 ;
③ .
(4) . .
25.(10分)
(1) (2)
(3) 。(4) 。
(5)
化学试题参考答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | C | A | B | B | B | C | C | A | C | C |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | C | C | D | A | D | B | A | D | D | D |
21.(11分)(1)②⑤ (2分)
(2)容量瓶偏小(2分)
(3)酸式滴定管溶液由无色变为紫红色(2分)
(4) 2MnO4―+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O (2分) (5)1.2(3分)
22.(15分) (1)Fe2O3(s)+ 3CO(g)=2Fe(s)+ 3CO2(g)(2分) △H=-28.5 kJ·mol-1(1分)
(2)CO + 4OH-― 2e-= CO32-+ 2H2O(2分)
(3)①>(2分) ②0.4<c≤1(4分)③bd(2分)
(4)(2分)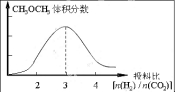 (0点开始1分, 3这点最高,1分)
(0点开始1分, 3这点最高,1分)
23(14分,每空2分)(1) 铁粉 , 由于TiOSO4容易水解,若温度过高,则会有较多TiOSO4水解为固体H2TiO3而经过滤进入FeSO4•7H2O中导致TiO2产率降低 ;
(2) Fe2+、Fe2O3
(3) TiCl4+(x+2)H2O(过量)=TiO2•xH2O↓+4HCl ;
(4) 取少量水洗液,滴加硝酸酸化AgNO3溶液,若不产生白色沉淀,说明Cl﹣已除净 ;
(5) BC
24(10分,每空1分)(1)BC
(2)① 面心立方最密堆积
② 硝酸分子是极性分子,易溶于极性溶剂的水中,硝酸分子中氢氧键易与水分子间形成氢键
(3)① 3s23p63d5 ② sp2 、 sp3 ③x= 5 分子晶体
(4) 立方体结构 a= ![]() cm
cm
25.(10分)
(1)CH2=CH2(2)酯基 、 碳碳双键
(3)8(4)a.bc
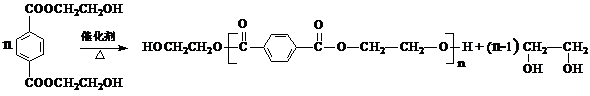 (5)
(5)