
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
重庆市巴蜀中学2015届高三下学期第二次模拟考试化学试题
化学部分(共100分)
可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32
Cl-35.5 K-39 Ca-40 Fe-56 Cu-64 Br-80 Ag-108 Ba-137
一、单项选择题:(7个小题,每题6分,共42分)
1.生活中处处有化学,下列表述不正确的是
A.福尔马林可作食品的保鲜剂 B.聚乙烯塑料制品可用于食品的包装
C.碳酸氢钠可作胃酸的中和剂 D.食盐可作调味剂,也可作食品防腐剂
2.设NA为阿伏伽德罗常数的值,下列说法正确的是
A.0.1 mol OD-离子含有的质子、中子数均为1.0NA
B.含有4.6 g钠元素的过氧化钠和氧化钠的混合物中,所含离子总数为0.3NA
C.3.6 g石墨中,含有共价键数为0.3NA
D.标准状况下,4.48 L己烷含有的分子数为0.2NA
3.已知废旧干电池中的填充物主要有二氧化锰、炭黑、氯化锌、氯化铵、淀粉糊、Mn2O3、ZnO、FeO、汞的化合物等。某实验小组的同学拟回收废旧电池中的部份物质,主要操作流程如下图:
火柴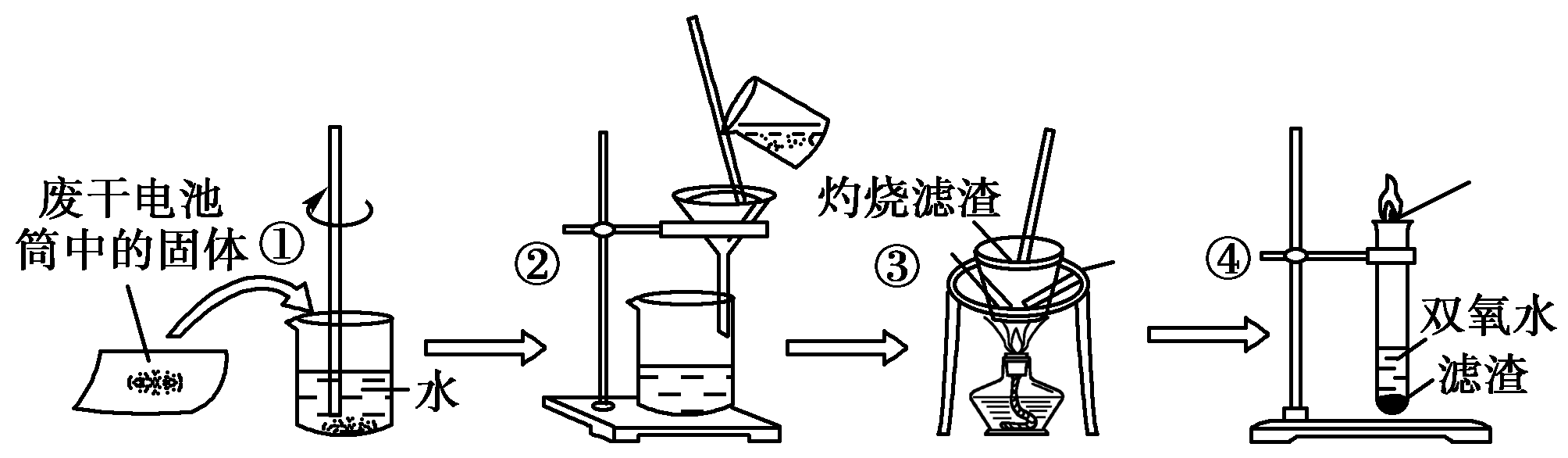
下列说法不正确的是
4.下列判断正确的是
A.通入足量CO2后的溶液中大量共存:Na+、SiO32-、CH3COO-、CO32-
B.pH=9的CH3COONa溶液和pH=9的NH3·H2O溶液,两溶液中水的电离程度相同
C.NH4Al(SO4)2溶液中滴加足量的NaOH的离子方程式为:NH4++ Al3++5OH-=NH3·H2O+ AlO2-+2H2O
D.Fe2+、SO2都能使酸性高锰酸钾溶液褪色,前者表现出还原性,后者表现出漂白性
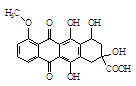
5.某种药物合成中间体的结构简式为: ,有关该物质的说法不正确的是
A.属于芳香族化合物
B.能发生消去反应和酯化反应
C.能分别与金属Na、NaHCO3溶液反应
 D.1 mol该有机物与足量NaOH溶液反应,消耗5 mol NaOH
D.1 mol该有机物与足量NaOH溶液反应,消耗5 mol NaOH
6.25 ℃时某些弱酸的电离平衡常数如表所示:
| CH3COOH | HClO | H2CO3 |
| K(CH3COOH) =1.8×10-5 | K(HClO) =3.0×10-8 | K(H2CO3)a1=4.4×10-7 K(H2CO3)a2=4.7×10-11 |
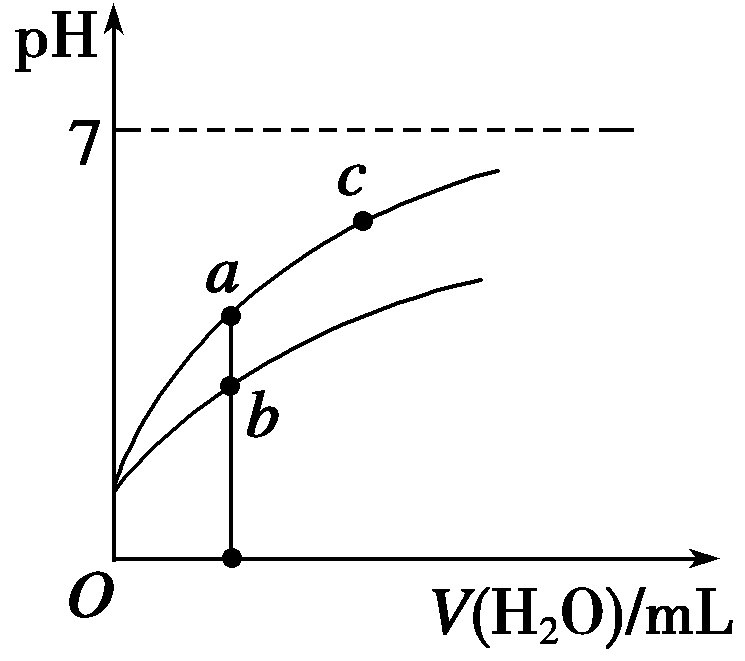
常温下,稀释CH3COOH、HClO两种酸时,溶液的pH随加水量变化的曲线如右图所示,下列说法正确的是
A.相同浓度的CH3COONa和NaClO的混合溶液中,各离子浓度的大小关系是:
c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B.图像中a、c两点所处的溶液中相等(HR代表CH3COOH或HClO)
C.图像中a点酸的浓度大于b点酸的浓度
D.向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O==2HClO+CO
7.一定温度下,向2.0 L恒容密闭容器中充入1.0 mol A,经一段时间后反应A(g)![]() B(g)+C(g)达到平衡。反应过程中测定的部分数据见下表:
B(g)+C(g)达到平衡。反应过程中测定的部分数据见下表:
下列说法正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(B)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.前50 s内B的平均反应速率v(B)=0.0032 mol·L-1·s-1
B.相同温度下,若达到平衡后向容器中继续充入A,则平衡向右移动,平衡常数增大
C.相同温度下,若起始时向容器中充入1.0 mol A、0.20 mol B和0.20 mol C,则达到平衡前v(正)>v(逆)
D.若保持其他条件不变,升高温度,平衡时,平衡常数K=0.2 mol·L-1,则反应的ΔH<0
二、非选择题(共4个小题,58分)
8.(14分)非金属元素H、C、O、S、Cl能形成的化合物种类很多,单质及化合物的用途很广泛。
⑴ O2-的离子结构示意图为 ,CS2的晶体类型为 晶体;
⑵ O、Cl两元素形成的单质和化合物常用来杀菌消毒,试举例________(写化学式,任写两种);
⑶ CH3OH在常温下为液态,沸点高于乙烷的主要原因是 ;
⑷ Cl2是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
| 危险性 | |
| 储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
| 泄漏处理 | NaOH、NaHSO3溶液吸收 |
| 包装 | 钢瓶 |
①用离子方程式表示“泄漏处理”中NaHSO3溶液的作用 。
②若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是 。
③将Cl2通入适量KOH溶液中,产物中可能有KCl、KClO、KClO3。当溶液中c(Cl-):c(ClO-)=11:1时,则c(ClO-):c(ClO3-)比值等于
⑸ 镁是一种较活泼的金属, Mg与Ca类似,也能与C形成某种易水解的离子化合物。已知该化合物0.1mol与水完全反应后,产生0.1mol的某种气体。该气体被溴水全部吸收后,溴水增重2.8g。请写出该水解反应方程式 。
9. (14分) 某化学兴趣小组欲验证:“铜和一定量的浓硝酸反应有一氧化氮产生”。设计使用了如下装置进行实验。(假设气体体积均为标准状况,导气管中气体体积忽略不计,且忽略反应中的溶液体积变化)
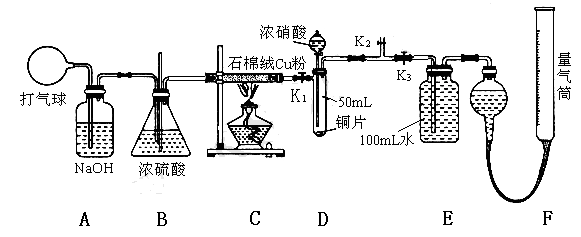
试回答下列问题:
⑴将铜粉分散在石棉绒中的原因是 ;
⑵在铜和浓硝酸反应前,挤压打气球(球内充满空气),经A、B、C反应后,进入D中的气体主要成分是 (填化学式),通入该气体的目的是 ;进行此步操作时应关闭 ,打开 (填K1、K2或K3)。
⑶关闭K1、K2,打开K3,由分液漏斗向D中滴加浓硝酸。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入CCl4至满。则D中一定发生反应的离子方程式为:____ __________。
⑷若E装置中出现倒吸,可采取的应急操作是 ;
⑸从E装置所得溶液中取出25.00mL,加两滴酚酞,用0.1000 mol·L-1的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,若实验测得F装置所收集到的气体体积为139.00 mL,则铜和一定量的浓硝酸反应 (填“有”或“无”)NO生成。
10.(本题共14分)
某酯(H)是一种合成多环化合物的中间体,可由下列路线合成(部分反应条件略去):
⑴ A→B的反应类型是 ,
B→C为加成反应,则化合物M的结构简式是 ;
⑵ H中除了羰基(![]() )外,含有的官能团名称是 ;
)外,含有的官能团名称是 ;
⑶ 实验室制A的化学方程式为 ;
⑷ E→ F的化学方程式是 ;
⑸ 下列说法正确的是
a. D和F中均属于炔烃类物质 b. A能和HCl反应得到聚氯乙烯的单体
c. 1mol G完全燃烧生成7mol H2O d. H能发生加成、取代反应
⑹ TMOB是H的同分异构体,具有下列结构特征:①核磁共振氢谱表明,分子中除苯环外,其它氢原子化学环境相同;②存在甲氧基(CH3O-)。TMOB的结构简式是
11.(16分)二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放。
⑴有一种用CO2生产甲醇燃料的方法:
已知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H=-akJ·mol-1;
CH3OH(g)+H2O(g)△H=-akJ·mol-1;
CH3OH(g)=CH3OH(l)△H=-bkJ·mol-1;
2H2(g)+O2(g)=2H2O(g)△H=-ckJ·mol-1;
H2O(g)=H2O(l)△H=-dkJ·mol-1,
则表示CH3OH(l)燃烧热的热化学方程式为:_____________________________
 ⑵在一定温度下的2L固定容积的密闭容器中,通入2 molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g)
⑵在一定温度下的2L固定容积的密闭容器中,通入2 molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),△H=-akJ·mol-1(a>0), 测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),△H=-akJ·mol-1(a>0), 测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
①能说明该反应已达平衡状态的是________。(选填编号)
A.CO2的体积分数在混合气体中保持不变
B.混合气体的平均相对分子质量不随时间的变化而变化
C.单位时间内每消耗1.2mol H2,同时生成0.4molH2O
D.该体系中H2O与CH3OH的物质的量浓度之比为1:1,且保持不变
②计算该温度下此反应的平衡常数K=_______。(保留两位有效数字)。若改变条件 (填选项),可使K=1。
A.增大压强 B.增大反应物浓度 C.降低温度 D.升高温度 E.加入催化剂
⑶ 某甲醇燃料电池原理如图1所示。
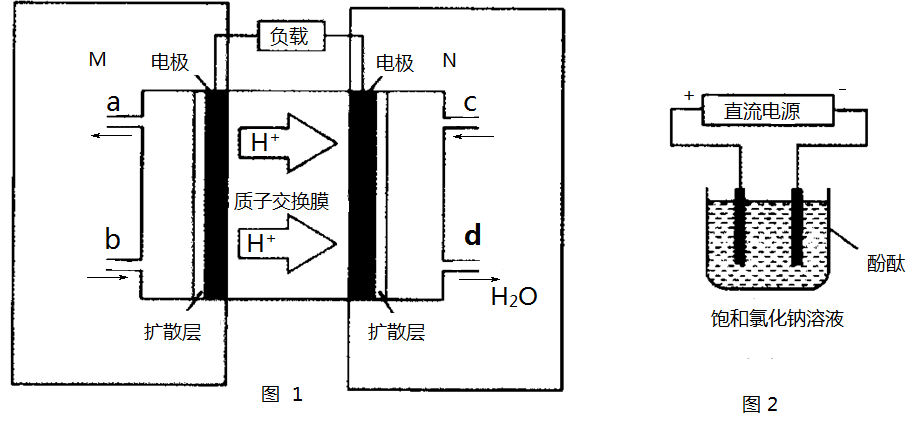
①M区发生反应的电极反应式为_______________________________。
②用上述电池做电源,用图2装置电解饱和食盐水(电极均为惰性电极),则该电解的总反应离子方程式为: 。假设溶液体积为300mL,当溶液的pH值变为13时(在常温下测定),理论上消耗甲醇的质量为______________(忽略溶液体积变化)。
化学答案
参考答案:
1-7 ABDCD BC
8.(本题共14分)⑴略 (1分) 分子晶体 (1分)
⑵ClO2O3Cl2(2分)
⑶甲醇分子之间能形成氢键而乙烷不能 (2分)
⑷①HSO3-+Cl2+H2O=SO42-+3H++2Cl- (2分)
②Fe(FeCl3)能催化苯与氯气的反应 (2分) ③1:2(2分)
⑸MgC2+2H2O=Mg(OH)2 + C2H2(2分)
9.(共14分)
⑴增大铜与氧气反应的接触面积(2分)
⑵N2(2分) 排出D中的空气(2分) 关闭K3(1分) 打开K1、K2(1分)
⑶Cu + 2NO3-+ 4H+= Cu2++ 2NO2↑+ 2H2O (2分) ⑷关闭K3(2分)
⑷有(2分)
10、(本题共14分)
⑴加成反应(2分)CH3OH(2分) ⑵碳碳双键、酯基;(2分)
⑶CaC2+2H2O==Ca(OH)2+C2H2↑(2分)
⑷CH3C≡CCOOH+HOCH2CH3![]() CH3C≡CCOOCH2CH3 + H2O (2分)
CH3C≡CCOOCH2CH3 + H2O (2分)
⑸b d (2分)
⑹ 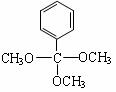 (2分)
(2分)
11(本题16分)
(1)CH3OH(l) +3/2O2(g) =CO2(g) +2H2O(l) ΔH=-(3c/2+2d-a-b)kJ·mol-1(3分)
(2)①AB(少选得1分,错选不得分) (2分) ② 0.20 (2分) C (2分)
(3)①CH3OH-6e-+H2O=CO2+6H+(3分)
②2Cl-+2H2O=H2↑+Cl2↑+2OH-(2分) 0.16g(2分)