
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
重庆市铜梁中学校2015届高三下学期模拟测试(一)化学试题
可能用到的原子量:Cu-64Fe-56H-10-16S-32Mg-24B-11
一、选择题(本大题共7小题,每小题6分,共42分。在每小题给出四个选项中,只有一项符合题目要求)
1.化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,不正确的是( )
A.加热饱和三氯化铁溶液制备氢氧化铁胶体:![]()
![]()
![]()
![]()
B.磷酸二氢根电离的离子方程式:![]()
![]()
![]()
C.少量碳酸氢钙溶液与氢氧化钠溶液混合的离子方程式
![]()
![]()
![]()
D.在0.5mol·L-1的K2Cr2O7溶液中存在如下平衡:![]()
![]()
![]() ,
,
其平衡常数K的表达式为![]()
2.化学与能源开发、环境保护、生产生活等密切相关。下列有关说法正确的是( )
A.二氧化硫可用于纸浆漂白,表明二氧化硫具有还原性
B.煤经过气化和液化等物理变化可以转化为清洁燃料
C.为防止月饼等富脂食品氧化变质,常在包装袋中放入生石灰
D.![]() 可用作呼吸面具的供氧剂
可用作呼吸面具的供氧剂
3.下列叙述正确的是( )
A.将![]() 通往入溶有少量氨的
通往入溶有少量氨的![]() 溶液中,无白色沉淀生成
溶液中,无白色沉淀生成
B.常温下,稀释0.1mol/L的醋酸,溶液中所有离子浓度均下降
C.等体积等浓度的![]() 与
与![]() 溶液混合后,溶液中离子浓度:
溶液混合后,溶液中离子浓度:
![]()
D.![]() 在同浓度的
在同浓度的![]() 和
和![]() 溶液中的溶解度相同
溶液中的溶解度相同
4.用题4图所示装置进行实验,装置正确且设计合理的是( )
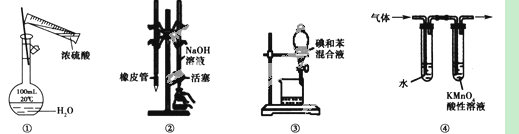
A.图①所示装置进行浓硫酸稀释配制稀硫酸的实验
B.图②所示装置进行用已知浓度为![]() 溶液测定盐酸浓度的实验
溶液测定盐酸浓度的实验
C.图③所示装置进行用苯萃取碘水中碘的实验,并把碘的苯溶液从漏斗下口倒出
D.图④所示装置可检验溴乙烷发生消去反应得到的气体中含有乙烯
5.化合物M(fumimycin)是从微生物中分离得到的,它显示出广谱抗菌活性。下列关于化全物M的说法中错误的是( )
A.化全物M的分子式为![]()
B.1 mol M在NaOH溶液中反应,最多消耗4 mol NaOH
C.化合物M能发生加成反应,不能发生消去反应
D.化合物M能使酸性![]() 溶液褪色
溶液褪色
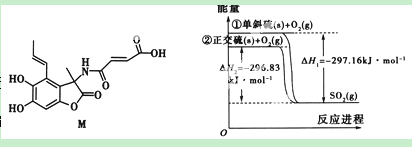
6.单斜硫和正交硫转化为二氧化硫的能量变化图如题6所示。下列说法正确的是( )
A.S(s,单斜)![]() S(s,正交)
S(s,正交)
![]()
B.正交硫比单斜硫稳定
C.单斜硫燃烧的热化学方程式为:S(s,单斜) + ![]()
![]()
![]()
![]()
D.①式表示断裂1 mol ![]() 中的共价键所吸收的能量比形成1 mol
中的共价键所吸收的能量比形成1 mol ![]() 中的共价键所放出的能量少297.16kJ
中的共价键所放出的能量少297.16kJ
7.在 2L的密闭容器中,一定条件下发生化学反应:![]()
![]()
![]()
![]() 。起始反应时NO和CO为4 mol,10s达到化学平衡,测得N2为1 mol。下列说法中正确的是( )
。起始反应时NO和CO为4 mol,10s达到化学平衡,测得N2为1 mol。下列说法中正确的是( )
A.反应前5 s内,用NO表示的平均反应速率为0.1 mol·L-1·S-1
B.达到平衡后,CO2的浓度与CO的浓度不同
C.当v正(CO)=2v逆 (N2)时反应达到平衡
D.达到平衡后,升高温度,正反应速率将减小,逆反应速率将增大
二、非选择题(本大题共4小题,共58分)
8.(14分)在生产和生活中,合金材料无处不在。
(1)铝合金是家庭装修中必不可少的金属材料。
①Al的原子结构示意图为 。Al2O3属于 氧化物。
②从Na2SiO3和NaAlO2混合溶液中制得Al(OH)3,需要从下列试剂中选择2种,选用的试剂组合最好是 。
a.NaOH溶液b.氨水c.CO2d.盐酸
(2)铁是生活、生产中用量最大的金属材料。
①将炽热的铁浸入水中快速冷却可称之为淬火,若生成磁性氧化铁,反应方程式为 。
②某铁的氧化物溶于足量酸后得澄清溶液,为检验该溶液中某种阳离子的存在,可在溶液中加入 溶液(填化学式),溶液显红色。
(3)铜合金是我国最早使用的金属材料。
①铜在潮湿的空气中长久放置后,表面会生成一层铜绿[主要成分是Cu2(OH)2CO3],写出铜生成铜绿的总反应式:
②将80.0 g Cu-Fe合金用酸完全溶解后,加入过量氨水,过滤得沉淀。将沉淀洗涤、灼烧后称重,质量仍为80.0 g。则合金中铜的质量分数为 。
9.(16分)氮化硼(BN)是新型无机非金属材料,溶点3000℃,可以作润滑剂、高级耐火材料和超硬材料。某兴趣小组以下图装置用NH3与B2O3固体在高温下制备少量氮化硼。
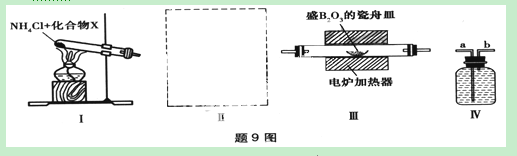
(1)装置的连接顺序是Ⅰ—Ⅱ—Ⅲ—Ⅳ,则化合物X是 ,装置Ⅱ中的药品和仪器是 和 。
(2)装置Ⅲ中发生反应的化学方程式是 。
(3)装置Ⅳ中广口瓶里盛装的是水,其作用是 ,进尾气的入口是 (填“a”或“b”)
(4)为防止装置内空气中的O2对制备反应的不利影响,则检验装置内空气被排尽的方法是先加入药品,连接装置Ⅰ、Ⅱ、Ⅲ, 。
(5)反应前瓷舟皿中盛有8.4g B2O3固体,反应结束后称得瓷舟皿中固体为6.4g,则氮化硼的产率为 (保留百分号前一位小数)。
(6)NH3与BCl3在高温下反应也能制备氮化硼,请从产物影响分析,工业上往往采用NH3与B2O3在高温下制备氮化硼的原因是 。
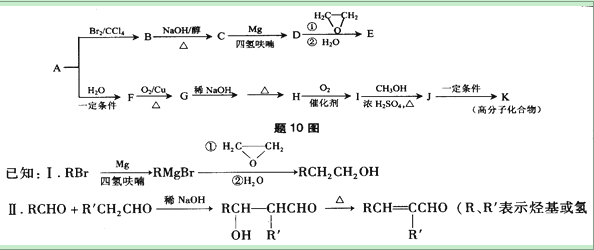
10.(14分)烃A是一种重要的基本化工原料,用质谱法测得其相对分子质量为28。题10图是以A为原料合成药物中间体E和树脂K的路线
(1)A中官能团的结构简式是 。
(2)B→C的化学方程式为 。
(3)E的分子式为C4H8O。下列关于E的说法正确的是 (填字母序号)。
![]()
 |
a.能与金属钠反应b.分子中4个碳原子一定共平面
c.一定条件下,能与浓氢溴酸反应d.与CH2![]() CHCH2OCH2CH3互为同系物
CHCH2OCH2CH3互为同系物
(4)写出符合下列条件的E的一种同分异构体: 。
a.该有机物能与新制的Cu(OH)2发生反应;b.核磁共振氢谱有3组峰,其比值为6:1:1
(5)G→H涉及到的反应类型有 。
(6)I的分子式为C4H6O2,其结构简式为 。
(7)J→K的化学方程式为 。
11.(14分)目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题。
(1)向浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(离子直径在1~10nm之间)。
①向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入NH3,后通入CO2。
制备纳米级碳酸钙的离子方程式是 。
②判断产品中是否含有纳米级碳酸钙的实验方法是 。
(2)已知CO2(g)+3H2(g)![]() CH3OH(1)+H2O(1)
CH3OH(1)+H2O(1)![]() ,该反应在低温下 自发进行(填“能”或“不能”)
,该反应在低温下 自发进行(填“能”或“不能”)
若其他条件不变,实验测得平衡常数:![]() ,则
,则![]()
![]() (填“<”“>”或“=”)
(填“<”“>”或“=”)
(3)如题11图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH![]() 2K2CO3+6H2O。
2K2CO3+6H2O。
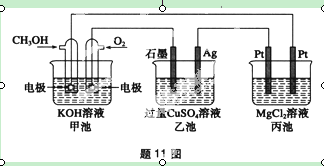
①其中 池是电能转化为化学能的装置;
②甲池通入CH3 OH的电级反应式为 ;
③若甲池中消耗280 mL(标准状况下)O2,此时丙地池中理论上最多产生 g固体
