湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
7.如图所示是四种常见有机物的比例模型示意图。下列说法正确的是 ( )
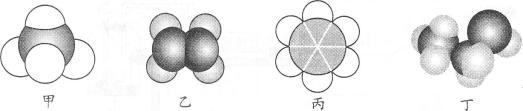
A.22.4 L甲中含有10 mol电子
B.乙与乙的加聚产物都能使溴水褪色
C.丙不能与溴水、酸性高锰酸钾溶液发生反应
 D.丙、丁都可以萃取溴水中的溴单质
D.丙、丁都可以萃取溴水中的溴单质
8.化学与生活密切相关.下列说法中不正确的是( )
A.“雨后彩虹”是一种与光学和胶体性质相关的自然现象
B.纯银器表面在空气渐渐变暗,是电化学腐蚀所致
C.右图电流表指针偏转,有电流通过
D.在食品中科学使用食品添加剂对人体无害
9.如下图所示装置,通入空气,开启a,b两个活塞,灼热铜丝,下列有关分析正确的是
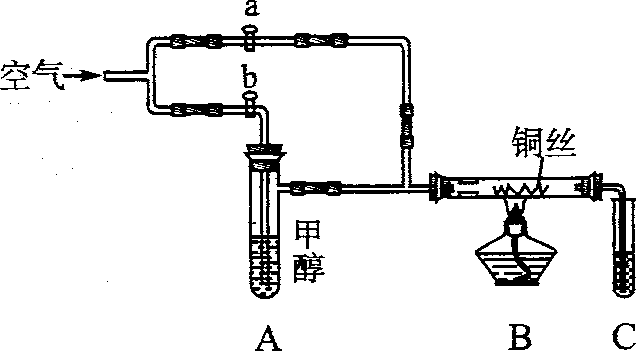
A.灼热铜丝发生的现象变化为紫红色与黑色交替出现,甲醇发生还原反应
B.C中有机产物易溶于水,与水分子间只形成1种氢键
C.检验C中产物的试剂可用1 mol·L-1的CuS04溶液2 mL和O.4 mol·L-1的NaOH溶液4 mL混合得到
D.可用酸性高锰酸钾溶液检验产物生成
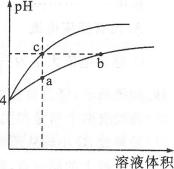 10.某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断不正确的是 ( )
10.某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断不正确的是 ( )
A.a、b、c三点溶液的Kw相同
B.b点溶液中C(H+)+c(NH3·H2O)=c(OH-)
C.用等浓度的NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液的体积Vb>Vc
D.a、b、c三点溶液中水的电离程度a>b>c
11.相关物质的溶度积常数见下表(25℃):
| 物质 | Mg(OH)2 | CH3COOAg | AgCl | Ag2CrO4 |
| Ksp(单位略) | 1.1X10-11 | 2.3X10-3 | 1.8X10-10 | 1.9X10-12 |
下列有关说法中不正确的是( )
A.浓度均为0.2 mol·L-1的AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg
沉淀
B.将O.001 mol·L-1的AgN03溶液滴入O.001 mol·L-1的KCl和O.001 mol·L-1的K2CrO4混合溶液中。先产生Ag2Cr04沉淀
C.0.ll mol·L-1的MgCL2溶液中加入氨水产生Mg(OH)2沉淀时溶液的pH为9
D.在其他条件不变的情况下,向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不变
12.右图是一种正在投入生产的大型蓄电系统的原理图。电池的中间为只允许钠离子通过的离子选择性膜。电池充、放电的总反应方程式为:![]()
![]()
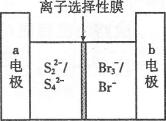 下述关于此电池说法正确的是 ( )
下述关于此电池说法正确的是 ( )
A.充电的过程中当O.1 mol Na+通过离子交换膜时,导线通过O.1 mol电子
B.电池放电时,负极反应为:3NaBr一2e-=NaBr3+2Na
C.充电过程中,电极a与电源的正极相连
D.放电过程中钠离子从右到左通过离子交换膜
13.硫酸生产中,其尾气是大气污染来源之一,![]()
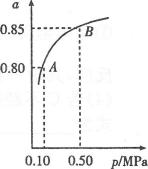 现在一种新型纳米材料氧缺位铁酸盐CoFe2OX由铁酸盐CoFe2O4经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。右图是某温度下SO2的平衡转化率(a)与体系总压强(p)的关系,下列说法正确的是 ( )
现在一种新型纳米材料氧缺位铁酸盐CoFe2OX由铁酸盐CoFe2O4经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。右图是某温度下SO2的平衡转化率(a)与体系总压强(p)的关系,下列说法正确的是 ( )
A.新型纳米材料氧缺位铁酸盐CoFe2OX的X的值是5
B.新型纳米材料氧缺位铁酸盐CoFe2OX在将酸性氧化物分解除去的过程中起催化作用
C.温度升高,SO2浓度增大,该反应的焓变为正值
D.平衡状态由A变到B时,平衡常数K(A)=K(B)
26.(14分)四氯化锡用作媒染剂和有机合成上的氯化催化剂,实验室制备四氯化锡的反应、装置示意图和有关信息数据如下:
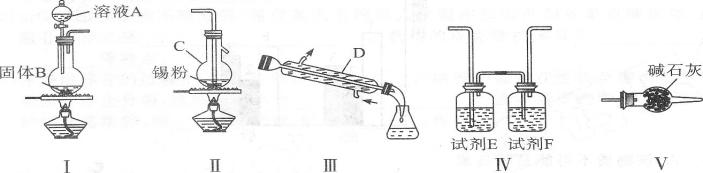
有关信息数据:①将金属锡熔融,通入干燥氯气进行反应。生成四氯化锡。②无水四氯化锡是无色易流动的液体,熔点-33℃,沸点114.1℃。⑧无水四氯化锡暴露于空气中与空气中的水分反应生成白色烟雾.有强烈的刺激性。回答下列问题:
(结果保留三位有效数字)。
27.(15分)某铜矿石的成分中含有Cu2O,还含有少量的Al2O3、Fe203和Si02。某工厂利用此矿石炼制精铜的工艺流程示意图如下:
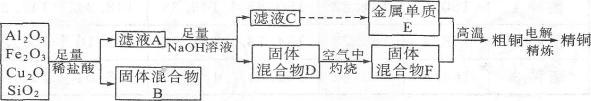
已知![]()
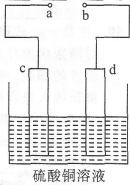 ①粗铜的电解精炼如图所示。在粗铜的电解精炼过程中,c为粗铜板,则a端应连接电源的(填“正”或“负”)极,若粗铜中含有Au、Ag、Fe杂质,则电解过程中c电极上发生反应的方程式有、。
①粗铜的电解精炼如图所示。在粗铜的电解精炼过程中,c为粗铜板,则a端应连接电源的(填“正”或“负”)极,若粗铜中含有Au、Ag、Fe杂质,则电解过程中c电极上发生反应的方程式有、。②可用酸性高锰酸钾溶液滴定法测定反应后电解液中铁元素的含量。
滴定时不能用碱式滴定管盛放酸性高锰酸钾溶液的原因是.
滴定中发生反应的离子方程式为,
滴定时.锥形瓶中的溶液接触空气,则测得铁元素的含量会(填“偏高”或“偏低”)。
28.(15分)目前工业合成氨的原理是![]() ΔH=一93.O kJ·mol-1
ΔH=一93.O kJ·mol-1
 已知一定条件下
已知一定条件下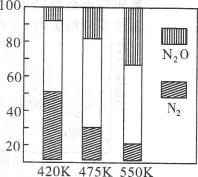
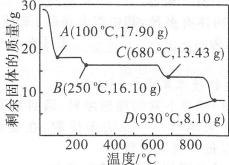
680℃时所得固体的化学式为(填字母序号)。
a.ZnO b.Zn30(S04)2c.ZnS04d.ZnS04·H20
36.(15分)
以黄铁矿为原料生产硫酸的工艺流程图如下:
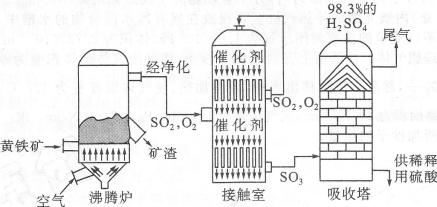
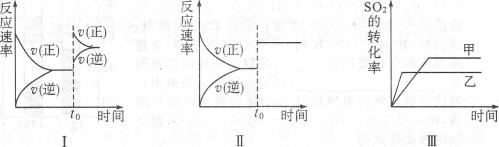
已知:Cr2072-+Fe2++H+→Fe3++H20十Cr3+(未配平)
①SO2通入Fe2(S04)3溶液中.发生反应的离子方程式为。
②接触室所得气体中SO2的体积分数为。
37.(15分)
As、N、0等非金属元素的化合物在工业生产中有重要的应用。
 已知氮的最高价氧化物为无色晶体.它由两种离子构成,其阴离子构型为平面正
已知氮的最高价氧化物为无色晶体.它由两种离子构成,其阴离子构型为平面正三角形,则其阳离子的构型为形,阳离子中氮的杂化方式为。
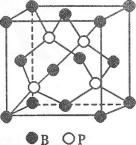
(4)磷化硼有多种晶型,右图示意的是磷化硼分子的分子结构图,其分子式
为
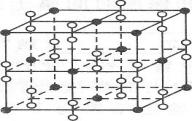
(5)钙在氧气中燃烧时得到一种钙的氧化物晶体,其结构如下图所示。由此判断该钙的氧化物的化学式为。已知该氧化物的密度是ρg·cm-3.则晶胞离得最近的两个钙离子间的距离为cm(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。
38.(15分)
2一苯基乙醇苯乙酸酯(分子式C16H16O2)具有玫瑰、海仙花、蜂蜜样极甜的香气和水果味,常用作定香剂,用于配制蜂蜜、樱桃、杏仁等型香精。H是2一苯基乙醇苯乙酸酯的同分异构体。合成过程如下图昕示:
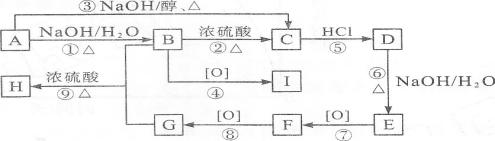
已知:
①A与D、B与E、I与F互为同分异构体。
②加热条件下新制Cu(OH)2分别加入到有机物I、F中,I中无明显现象,F中有红色
沉淀。
根据以上信息,回答下列问题:
化学:
答案:7.C 8.B 9.B 10.B 11.B 12.A 13.D
26.答案:(1)蒸馏烧瓶(1分) 将SnCl4气体冷凝为液体(1分)
(2)I Ⅳ Ⅱ Ⅲ V(2分)
(3)饱和食盐水(1分)浓硫酸(1分) 吸收未反应的氯气、防止空气中的水蒸气进入装置Ⅲ内.使SnCl4水解(2分)
(4)Sn(OH)4或SnO2(2分)
(5)加热蒸馏(2分)
(6)92.O%(2分)
27. 答案:(1)Fe2+(1分) Cu+2Fe3+=Cu2++2Fe2+(1分) 硫氰化钾溶液和新制氯水(1分)
![]()
(3)1l(1分)
(4)Cu2++CO32-+H2O=Cu(OH)2+CO2(2分)
(5)①正(1分) Fe-2e—=Fe2+(1分) Cu-2e—=Cu2+(1分)
②酸性高锰酸钾溶液有强氧化性,能腐蚀碱式滴定管上的橡胶管(或易使橡胶管老化),所以不能用碱式滴定管盛高锰酸钾溶液(2分) 5Fe2++MnO42-+8H+=5Fe2++Mn2++4H2O(2分)偏低(1分)
28.![]() (2分)
(2分)
(2)①C(1分)
②O.12 mol·L-·min-(2分)![]()
(3)AD(2分)
(4)随温度升高,N2的含量降低(1分) 主反应为放热反应.升温使主反应的平衡左移(或副反应为吸热反应,升温使副反应的平衡右移,降低了NH3和NO的浓度,使主反应的平衡左移)(1分)
(5)2NH3+6OH一+6e—=N2+5H20(2分)
(6)b(2分)
36.
37.![]() (2)5(2分)
(2)5(2分)
(3)直线(2分) sp(2分)
(5)B14P4(2分) (6)CaO2(2分)
![]() (3分)
(3分)
38.