
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
青冈一中2017-2018学年度高三第一次模拟考试
化学试题
时间90分钟
满分100分
可能用到的原子量:H:1 C:12 O:16 Mg:24 S:32 Cl:35.5 Fe:56 N:14 Al:27
Na:23
第Ⅰ卷(选择题共54分)
一、选择题(本题包括18小题,每小题3分,共54分,每小题只有一个正确选项
1、下列金属中,表面自然形成的氧化层能保护内层金属不被空气氧化的是( )
A.K B.Na C.Fe D.Al
2、下列有关水处理方法不正确的是
A.用石灰、碳酸钠等碱性物质处理废水中的酸
B.用可溶性的铝盐和铁盐处理水中的悬浮物
C.用氯气处理水中的Cu2+、Hg+等重金属离子
D.用烧碱处理含高浓度![]() 的废水并回收利用氨
的废水并回收利用氨
3、设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A.14 g乙烯和丙烯混合气体中的氢原子数为2NA
B.1 mol N2与4 mol H2反应生成的NH3分子数为2NA
C.1 mol Fe溶于过量硝酸,电子转移数为2NA
D.标准状况下,2.24 L CCl4含有的共价键数为0.4NA
4、化学与生产和生活密切相关。下列过程中没有发生化学变化的是( )
A.氯气作水杀菌消毒剂
B.硅胶作袋装食品的干燥剂
C.二氧化硫作纸浆的漂白剂
D.肥皂水作蚊虫叮咬处的清洗剂
5、化学在生活中应用广泛,下列物质性质与对应用途错误的是
C. 氮气化学性质稳定,可用作粮食保护气 D. 溴化银见光易分解,可用作胶片感光剂
6、下列反应中,反应后固体物质增重的是( )
A.氢气通过灼热的CuO粉末 B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热反应 D.将锌粒投入Cu(NO3)2溶液
7、寿山石的主要成分为叶腊石,其组成为Al2O3·4SiO2·H2O,可以表示为Al2Si4Ox(OH)y。其中x、y的数值分别是( )
A.10、2 B.6、4 C.8、2 D.2、8
8、下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实 验 | 现 象 | 结 论 |
| A. | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
| B. | 将铜粉加1.0 mol·L-1Fe2(SO4)3溶液中 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
| C. | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| D. | 将0.1mol·L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol·L-1CuSO4溶液 | 先有白色沉淀生成后变为浅蓝色沉淀 | Cu(OH)2的溶度积比Mg(OH)2的小 |
9、在给定的条件下,下列选项所示的物质间转化均能实现的是
A.SiO2![]() SiCl4
SiCl4![]() Si
Si
B.FeS2![]() SO2
SO2![]() H2SO4
H2SO4
C.N2![]() NH3
NH3![]() NH4Cl(aq)
NH4Cl(aq)
D.MgCO3![]() MgCl2(aq)
MgCl2(aq)![]() Mg
Mg
10、在含有Fe3+、Fe2+、Al3+、NH4+的稀溶液中加入足量的Na2O2固体,充分反应后微热,再加入过量的稀盐酸,完全反应后,离子数目没有变化的是( )
A.Fe3+ 、Al3+B.Al3+C.Fe2+、NH4+D.Fe3+
11、下列有关实验原理或操作正确的是( )
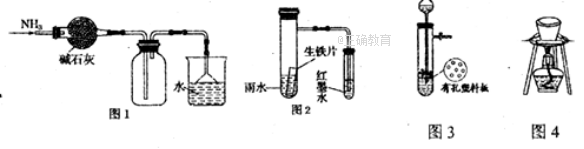
12、下列有关物质分类或归类正确的是( )
①混合物:石炭酸、福尔马林、水玻璃、水银
②化合物:CaCl2、烧碱、聚苯乙烯、HD
③电解质:明矾、胆矾、冰醋酸、硫酸钡
④同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
⑤同素异形体:C60、C70、金刚石、石墨.
A.①③④B.③⑤C.②③④D.②④
13、下列所得溶液的物质的量浓度等于0.1mol•L﹣1的是( )
A.将0.1 mol HCl充分溶解在1 L水中
B.将60 g质量分数为10%的醋酸与940 g水混合
C.将3.1 g氧化钠溶于水并配成1 L溶液
D.将14.2 g Na2SO4•10H2O溶于水中配成1 L溶液
14、下列离子方程式书写正确的是( )
A.单质钠放入水中:Na+H2O═Na++OH﹣+H2↑
B.二氧化硅溶于NaOH溶液:SiO2+2OH﹣═SiO32﹣+H2O
C.向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2﹣+4NH4++2H2O
D.碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH﹣![]() NH3↑+H2O
NH3↑+H2O
15、水热法制直径为1到100nm的颗粒Y(化合物),反应原理为:3Fe2++2S2O32﹣+O2+aOH﹣=Y+S4O62﹣+2H2O,下列说法中不正确的是( )
A.a=4
B.S2O32﹣是还原剂
C.将Y均匀分散到水中形成的体系具有丁达尔效应
D.每有3 mol Fe2+参加反应,反应中转移的电子总数为5 mol
16、为提纯下列物质(括号内为杂质),选用的除杂试剂和分离方法都正确的是
| 选项 | 物质 | 除杂试剂 | 分离方法 |
| A | 二氧化硅(碳酸钙) | 氢氧化钠溶液 | 过滤 |
| B | 硫酸铜溶液(硫酸铁) | 加入过量铜粉 | 过滤 |
| C | 乙醇(乙酸) | 生石灰 | 蒸馏 |
| D | SO2(CO2) | 碳酸钠溶液 | 洗气 |
17.如图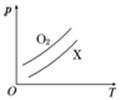 表示1 g O2与1 g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是( )
表示1 g O2与1 g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是( )
A. C2H4 B. CH4C. CO2 D. NO
18、NA为阿伏伽德罗常数的值。下列说法正确的是
A.4.0gNaOH所含电子总数为2NA
B.18g重水(D2O)所含共价键总数为2NA
C.1L0.1mol•L-1KHC2O4溶液中,HC2O4-、C2O42-的粒子数之和为0.1NA
D.常温下,1LpH=9的CH3COONa溶液中,发生电离的水分子数为1×10-9NA
第II卷 非选择题(共46分)
19、次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性.回答下列问题.
(1)H3PO2与足量的NaOH溶液反应,生成NaH2PO2,则H3PO2为 元酸.
(2)H3PO2是中强酸,写出其与NaHCO3溶液反应的离子方程式 .
(3)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银.
①H3PO2中,P元素的化合价为 ;
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为 (填化学式);
Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式 .
20、过氧化钙(CaO2·8H2O)是一种在水产养殖中广泛使用的供氧剂。
O2![]() MnO(OH)2
MnO(OH)2![]() I2
I2![]() S4O
S4O![]()
写出O2将Mn2+氧化成MnO(OH)2的离子方程式:
21、(11分)如图是工业制取菱镁矿MgCO3(含杂质Al2O3、FeCO3)制取镁的工艺流程
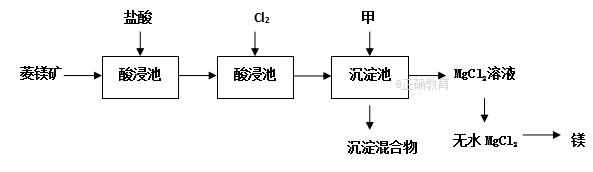
请回答有关问题:
(2)氧化池通入Cl2的目的是氧化 (填化学式),工业上不选用硝酸做氧化剂的原因是 和 。
(3)物质甲可以是
A、MgO B、Mg(OH)2C、NaOH溶液 D、稀氨水
(4)由MgCl2溶液制取无水MgCl2的操作方法 。
(5)当Fe3+完全沉淀时,求最小pH 。
已知:氢氧化铁ksp=1.0×10-38,离子浓度小于1×10-5mol/L认为沉淀完全
22、(15分)氰基丙烯酸酯在碱性条件下能快速聚合为![]() 从而具有胶黏性。某种氰基丙烯酸酯(G)的合成路线如下:
从而具有胶黏性。某种氰基丙烯酸酯(G)的合成路线如下:
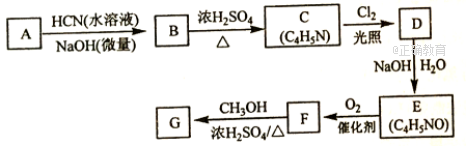
已知:
①A的相对分子质量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| D | C | A | B | B | B | A | D | C |
| 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| B | B | B | C | B | D | C | C | A |
高三一模化学答案
一、选择题(每题3分,共54分)
19、(10分)(每空2分)
(1)一;
(2)H3PO2+HCO3-=H2PO﹣2+CO2↑+H2O;
(3)①+1;
②H3PO4;
(4)2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑.
21、(14分)
22、(15分)(1)丙酮 (2分) (2) 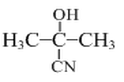 (2分) 2 (1分) 6:1或1:6(1分) (3)取代反应(1分)
(2分) 2 (1分) 6:1或1:6(1分) (3)取代反应(1分)
(4)![]() (2分)
(2分)
(5)碳碳双键 酯基 氰基 (3分)(6)8(3分)
