湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
山西省太原市2017届高三第二次模拟考试理综化学试题
可能用到的相对原子质量: H-1 C-12 O-16 S-32 Zn-65
第一部分
选择题(一)本题共13小题,每小题6分。在每小题给出的四个选项中,只有一项是符合题目要求的。
7、有机化学与材料、生活和环境密切相关。下列说法正确的是
A.利用植物秸秆可以生产香料乙酸乙酯
B.从煤焦油中提取苯和苯的同系物,可采取的方法是萃取
C.用石油裂解产物通过加聚反应直接制备PVC(聚氯乙烯)
D.油脂在氢氧化钠溶液中加热发生皂化反应,最终生成高级脂肪酸和丙三醇
8、1934年,科学家首先从人尿中分离出具有生长素效应的化学物质一吲哚乙酸,吲哚乙酸的结构如图所示。下列有关吲哚乙酸的说法正确的是
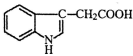
A.吲哚乙酸的分子式是C10H10NO2
B.吲哚乙酸苯环上的二氯代物共有四种(不考虑立体异构)
C.吲哚乙酸可以发生取代反应、加成反应、氧化反应和还原反应
D. 1 mol吲哚乙酸与足量氢气发生加成反应时,最多可以消耗5 mol H2
9、短周期元素a、b、c、d分属三个周期,且原子序数依次增大。其中b与a、c两种元素均可形成原子个数比为1:1或1:2的化合物,a、c的原子具有相同的最外层电子数,b、d形成的一种化合物在工业上是一种新型自来水消毒剂。下列说法一定正确的是$来&源:
| 实验操作和现象 | 实验结论 | |
| A | 检验某溶液中是否含有SO42-时,向溶液中滴加用盐 酸酸化的BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 检验输送氯气的管道是否发生泄漏时,用一根玻璃棒蘸取浓氨水,然后靠近管道 | 有白色烟雾产生时说明管道发生泄漏 |
| C | 检验FeCl3溶液中是否含有Fe2+时,向溶液中滴加 酸性KMnO4溶液,溶液变为无色 | 该溶液中一定含有Fe2+ |
| D | 向2mL0.1 mol•L-1 硝酸银溶液中加入1 mL mol•L-1NaCl溶液,出现白色沉淀,再加入几滴0.1 mol•L-1Na2S溶液,有黑色沉淀生成 | 该现象说明相同温度下Ksp (Ag2S) |
C.若用氨水标准溶液滴定盐酸,则应选择酚酞作为指示剂
D. 25℃时,反应NH4++H2O![]() NH3•H2O+H+的平衡常数约为 5.6 ×10-10
NH3•H2O+H+的平衡常数约为 5.6 ×10-10
26、(15分)某化学实验小组的同学将打磨过的镁条投入到滴有酚酞的饱和NaHCO3溶液中, 发现反应迅速,产生大量气泡和白色不溶物,溶液的浅红色加深。该小组同学对白色不溶物的成分进行了探究和确定。
I .提出假设:
(1)甲同学:可能只是MgCO3;
乙同学:可能只是______________;
丙同学:可能是:xMgCO3·yMg(OH)2。
(2)在探究沉淀成分前,需将沉淀从溶液中过滤、洗涤、低温干燥。洗涤沉淀的操作方法是____________________________________________________________。
(3)请设计一个简单的实验证明乙同学的假设是错误的_________________________。
Ⅱ.定量实验探究:取一定量已干燥过的沉淀样品,利用下列装置测定其组成(部分固定夹持装置未画出),经实验前后对比各装置的质量变化来分析沉淀样品的组成,得出丙同学的假设是正确的。请回答下列问题:
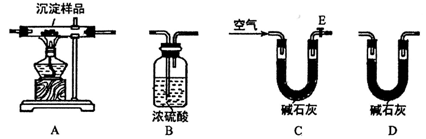
(4)写出xMgCO3·yMg(OH)2受热分解的化学方程式______________________。(用x、y表示)
(5)①合理的实验装置连接顺序为:_____→_____→_____→_____→。(各装置只使用一次)
② 实验一段时间后,当装置B中___________(填实验现象)时,停止加热,说明沉淀样品完全分解;然后打开E处的活塞,缓缓通入空气数分钟的目的是________________。
③指导老师认为在上述实验装置末端还需再连接一个装置D,若无此装置,.则会使测出的x∶y的值(填“偏大”、“偏小”或“无影响”)
27、(16分)近年华北地区频繁的雾霾天气已经引起人们的高度重视,化学反应原理可用于治理环境污染,请回答下列问题:
(1)一定条件下,可以用CO处理燃煤烟气生成液态硫,实现硫的回收。
①已知:2CO(g)+O2(g) = 2CO2(g) ΔH= -566 kJ·mol-1
S(l) +O2(g) = SO2(g) ΔH=-296 kJ·mol-1
则用CO处理燃煤烟气的热化学方程式是_______________________________。
②在一定温度下,在2 L密闭容器中投入2 mol CO、l mol SO2发生上述反应,达到化学平衡时SO2的转化率为90%,则该温度下该反应的平衡常数K的数值为____________。
(2)SNCR—SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),其流程如下:
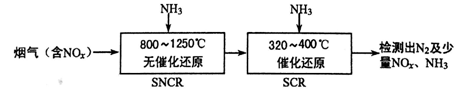
已知该方法中主要反应的热化学方程式:
4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) ΔH=-1646 kJ·mol-1,在一定温度下,在密闭恒压的容器中,能表示上述反应达到化学平衡状态的是__________________(填字母)。
4N2(g)+6H2O(g) ΔH=-1646 kJ·mol-1,在一定温度下,在密闭恒压的容器中,能表示上述反应达到化学平衡状态的是__________________(填字母)。
b.混合气体的密度保持不变
c. c(N2)∶c(H2O)∶c(NH3)=4∶6∶4
d.单位时间内断裂4 mol N-H键的同时断裂4 mol![]() 键
键
(3)如图所示,反应温度会直接影响SNCR技术的脱硝效率。
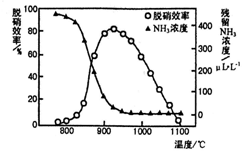
①SNCR技术脱硝的最佳温度选择925 ℃的理由是___________________________。
②SNCR与SCR技术相比,SNCR技术的反应温度较高,其原因是________________;但当烟气温度高于1000℃时,SNCR脱硝效率明显降低,其原因可能是______________________。
(4)一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示:
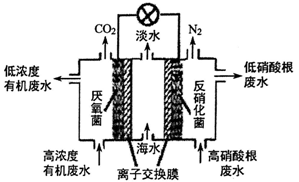
①中间室的Cl-移向_________(填“左室”或“右室”),处理后的含硝酸根废水的pH__________(填“降低”或“升高”)
②若图中有机废水中有机物用C6H12O6表示, 请写出左室发生反应的电极反应式:____________________________。
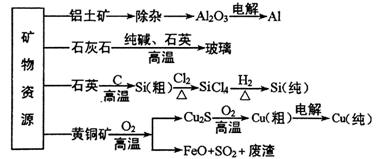
28、(12分)以某菱锰矿(含MnCO3、SiO2、FeCO3和少量Al2O3等)为原料通过以下方法可获得碳酸锰粗产品:
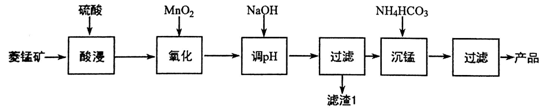
(1)“酸浸”时加快反应速率的方法除了增加硫酸的浓度和加热外,还有___________________。(写出一种)
(2)在加NaOH调节溶液的pH时约为5,如果pH过大,可能导致滤渣1中___________________
(填化学式)的含量减少。
(3)取“沉锰”前溶液a mL于锥形瓶中,加入少量AgNO3溶液(作催化剂)和过量的1.5%(NH4)2S2O8(过二硫酸氨)溶液,加热,Mn2+被氧化为MnO4-,反应一段时间后再煮沸5 min[除去过量的(NH4)2S2O8],冷却至室温。选用适宜的指示剂,用b mol·L-1的(NH4)2Fe(SO4)2标准溶液滴定至终点,平均消耗(NH4)2Fe(SO4)2标准溶液的体积为V mL。
①Mn2+与(NH4)2S2O8反应的离子方程式为 _________________。
②用含a、b、V的代数式表示“沉锰”前溶液中c(Mn2+)=_______________。
(4)①写出“沉锰”时的离子方程式: _________________。
②在其他条件相同时,NH4HCO3的初始浓度越大,锰元素回收率越高,请从沉淀溶解平衡的角度解释其原因 _________________。
35、【化学一选修3:物质结构与性质】(15分)
A、B、C、D、E是前四周期原子序数依次增大的五种元素。A、D同主族且能形成两种常见化合物DA2和DA3;基态C原子最外电子层上有1个未成对电子;基态B、E原子的最外层均只有2个电子,其余各电子层均全充满。回答下列问题:
(1)基态D原子价电子的轨道表达式为_________,元素铜与E的第二电离能分别为ICu=1985 kJ·mol-1,
IE=1733 kJ·mol-1,ICu>IE的原因是_____________________。
(2)DA2分子的VSEPR模型是_________。写出一种与DA3互为等电子体的离子的化学式:_____。
(3)实验测得C与氯元素形成气态化合物的实际组成为C2Cl6,其球棍模型如图所示,其中C原子的杂化方式为_____________。
已知CCl3在加热时易升华,与过量的NaOH溶液反应可生成 Na[C(OH)4],CCl3固体属于______晶体(填晶体类型)
(4)试比较A、D简单氢化物的热稳定性,并说明理由:_________________(用键参数解释)
(5)D与E所形成化合物晶体的晶胞如图所示:
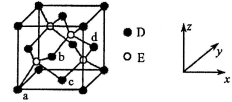
①在该晶体中,D的配位数为_____________。
②原子坐标参数可表示晶胞内部各原子的相对位置。上图晶胞中,原子坐标参数a为(0,0,0);b为(![]() ,0,
,0,![]() );c 为(
);c 为(![]() ,
,![]() ,0)。则d 的坐标参数为_______________。
,0)。则d 的坐标参数为_______________。
③已知该晶体的密度为p g·cm-3,设NA表示阿伏加德罗常数的值,则晶胞中D离子与E离子之间的最近距离为__________________pm。
36、【化学——选修5:有机化学基础】(15分)
A(C2H4)是基本的有机化工原料。用A和常见的有机物可合成一种醚类香料和一种缩醛类香料,具体合成路线如图所示(部分反应条件略去):
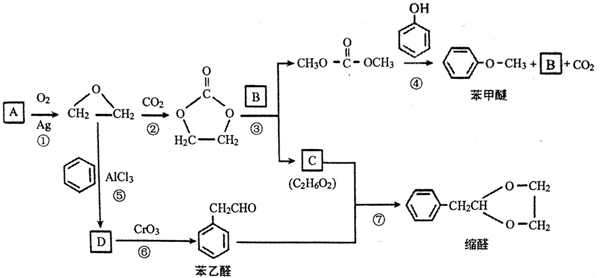
已知:
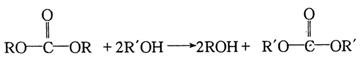
回答下列问题:
(1)B的分子式是___________,C中含有的官能团名称是____________。
(2)若D为单取代芳香族化合物且能与金属钠反应;每个D分子中只含有1个氧原子,D中氧元素的质量分数约为13.1%,则D的结构简式为___________,⑥的反应类型是________________。
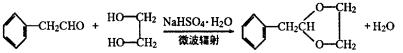
(3)据报道,反应⑦在微波辐射下,以NaHSO4·H2O为催化剂进行,请写出此反应的化学方程式:____________________________________。
(4)请写出满足下列条件的苯乙醛的所有同分异构体的结构简式:___________________。
i .含有苯环和![]() 结构
结构
ii.核磁共振氢谱有4组峰,且峰面积之比为3∶2∶2∶1
(5)若化合物E为苯甲醚的同系物,且相对分子质量比苯甲醚大14,则能使FeCl3溶液显色的E的所有同分异构体共有(不考虑立体异构)________________种。
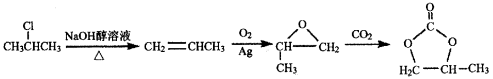
(6)参照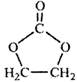 的合成路线,写出由2-氯丙烷和必要的无机试剂制备
的合成路线,写出由2-氯丙烷和必要的无机试剂制备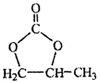 的合成流程图:_______________________________________
的合成流程图:_______________________________________
合成流程图示例如下:CH2 = CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH

7-13 ACDDBBD
26、(除标注外,每空2分,共15分)
(1)Mg(OH)2(1分)
(2)向过滤器(或漏斗)中沿玻璃棒注入蒸馏水至浸没沉淀,待水自然流下后重复操作2〜3次
(3)取沉淀物少许于试管中,加入足量稀盐酸(或稀硫酸、稀硝酸)时全部溶解,并产生气泡 (或其他合理答案)
(4)xMgCO3·yMg(OH)2![]() (x+y)MgO+xCO2+yH2O
(x+y)MgO+xCO2+yH2O
(5)①CABD
②无气泡冒出将装置中生成的CO2和水蒸气排入后续装置
③偏大
27、(除标注外,每空2分,共16分)
(1)①2CO(g)+SO2(g)=2CO2(g)+S(l) ΔH=-270kJ·mol-1,② 1620
(2)b
(3)①925℃时脱硝效率高,残留氨浓度较小
②反应的活化能较大,没有使用催化剂因为脱硝主要反应是放热反应,温度过高,使脱硝主要反应的平衡逆向移动(或生成的N2与O2反应生成NO等其他合理答案)
(4)①左室(1分) 升高(1分)
②C6H12O6-24e-+6H2O=6CO2↑+24H+
28、(每空2分,共12分)
(1)将矿石粉碎(或搅拌等)
(2)Al(OH)3、SiO2
(3)①2Mn2++5S2O82-+8H2O![]() 2MnO4-+10SO42-+16H+
2MnO4-+10SO42-+16H+
②![]() mol•L-1
mol•L-1
(4)①Mn2++2HCO3-=MnCO3↓+CO2↑+H2O
②c(NH4HCO3)越大,c(CO32-)越大,使平衡MnCO3(s)![]() CO32- (aq)+Mn2+ (aq)向逆反应方向移动,析出的MnCO3越多(或其他合理解释)
CO32- (aq)+Mn2+ (aq)向逆反应方向移动,析出的MnCO3越多(或其他合理解释)
35、(除标注外,每空2分,共15分)
(1)![]() 失去第二个电子对,Cu失去的是全充满的3dl0电子,Zn失去的是4s1电子,所以Zn的第二电离能比Cu小(或其他合理解释)
失去第二个电子对,Cu失去的是全充满的3dl0电子,Zn失去的是4s1电子,所以Zn的第二电离能比Cu小(或其他合理解释)
(2)平面三角形(1分)CO32- (或NO3-等其他合理答案)(1分)
(3)sP3(1分) 分子(1分)
(4)热稳定性:H2O>H2S,因为O原子半径小于S原子半径,键长小,键能大
(5)①4②(1,![]() ,
,![]() ) (1分)③
) (1分)③![]() ×
×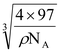 ×1010(或其他合理答案)
×1010(或其他合理答案)
36、(共15分,除标注外,每空2分)
(1)CH4O(1分) 羟基(1分)
(2)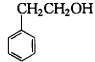 (1分) 氧化反应(1分)
(1分) 氧化反应(1分)
(3)
(4) (每个2分)
(每个2分)
(5)9
(6)