
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2015年惠州市高三4月模拟考试
理科综合化学试题
7.下列有关说法中,正确的是
C. 粮食酿酒主要经过淀粉→葡萄糖→乙醇的化学变化过程
D. 明矾既可用于净水,也可杀菌消毒
8.下列说法正确的是
A.放热反应一定能自发的进行
B.SO2能使品红溶液和溴水褪色,说明SO2具有漂白性
C.将AlCl3溶液和Al2(SO4)3溶液分别蒸干灼烧,所得产物均为Al2O3
D.由反应AgCl(s) +KI(aq) ![]() Ag I(s) + KCl (aq) 可知Ksp(AgCl)>Ksp(Ag I)
Ag I(s) + KCl (aq) 可知Ksp(AgCl)>Ksp(Ag I)
9.下列各组离子在一定条件下能够大量共存的是
A.无色溶液:Cu2+、K+、MnO4-、SO42-
B.能溶解Al2O3的溶液:Na+、Ca2+、HCO3-、NO3-
C.常温下c(OH-)=1×10-13mol·L-1的溶液:NH4+、Al3+、SO42-、Cl-
D.含1.2 mol·L-1NO3-的溶液:H+、Fe2+、Mg2+、Br-
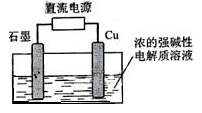 10.Cu2O是一种半导体材料,制取Cu2O的电解池如图,总反应为:2Cu+H2O==Cu2O+H2
10.Cu2O是一种半导体材料,制取Cu2O的电解池如图,总反应为:2Cu+H2O==Cu2O+H2![]() 。下列说法不正确的是
。下列说法不正确的是
A.铜电极发生氧化反应
B.铜电极接直流电源的负极
C.石墨电极上产生氢气
D.每生成1molCu2O时,就有2mol电子转移
11.已知X、Y、Z元素的原子具有相同的电子层数,且原子序数依次增大,其最高价氧化物对应水化物酸性依次增强,下列判断正确的是
A.最高化合价按X、Y、Z的顺序减小
B.阴离子的还原性按X、Y、Z顺序增强
C.单质的氧化性按X、Y、Z顺序增强
D.氢化物的稳定性按X、Y、Z顺序减小
12. 用![]() 表示阿伏加德罗常数的值,下列叙述正确的是(Cu-64 O-16)
表示阿伏加德罗常数的值,下列叙述正确的是(Cu-64 O-16)
A.1mol![]() 晶体中阴离子的个数为2
晶体中阴离子的个数为2![]()
B.标准状况下,2.24L苯所含的分子总数为0.1![]()
C.32gO2和32g O3的所含的氧原子数都是为2![]()
D.6.4g铜与过量的浓硝酸完全反应转移的电子数是0.1![]()
22.下列液体均处于25℃,有关叙述正确的是
A.某物质的溶液pH< 7,则该物质可能是酸或强酸弱碱盐
B.pH = 4的番茄汁中c(H+)是pH = 6的牛奶中c(H+)的20倍
C.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同
D.pH=7的CH3COOH与CH3COONa混合溶液中,c(Na+) = c(CH3COO-)
23. 物质中杂质(括号内为杂质)的检验、除杂的试剂或方法都正确的是
| 物质及其杂质 | 检验 | 除杂 | |
| A | Cl2(HCl) | 湿润的淀粉KI试纸 | 饱和食盐水 |
| B | NO(NO2) | 观察颜色或湿润的淀粉KI试纸 | 水 |
| C | CO2(HCl) | AgNO3溶液(含稀硝酸) | 饱和NaHCO3溶液 |
| D | NaHCO3溶液(Na2CO3) | Ca(OH)2溶液 | 过量CO2 |
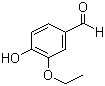 30.(16分)乙基香兰素是一种合成香料,其结构简式如图:
30.(16分)乙基香兰素是一种合成香料,其结构简式如图:
(1)以下推测正确的是
a.从分子结构上看,它属于芳香烃
b.该物质能与FeCl3溶液发生显色反应
c.该物质能与碳酸钠溶液反应产生CO2气体
d.一定条件下,1mol该物质最多能与4molH2发生加成反应
(2) R物质是乙基香兰素的同分异构体,性质如下:
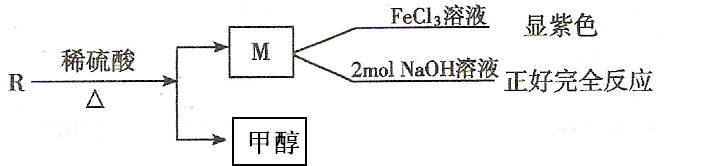
试写出任意一种符合上述条件的R的同分异构体的结构简式 。
(3)X也是乙基香兰素的同分异构体,其可以发生如下反应:
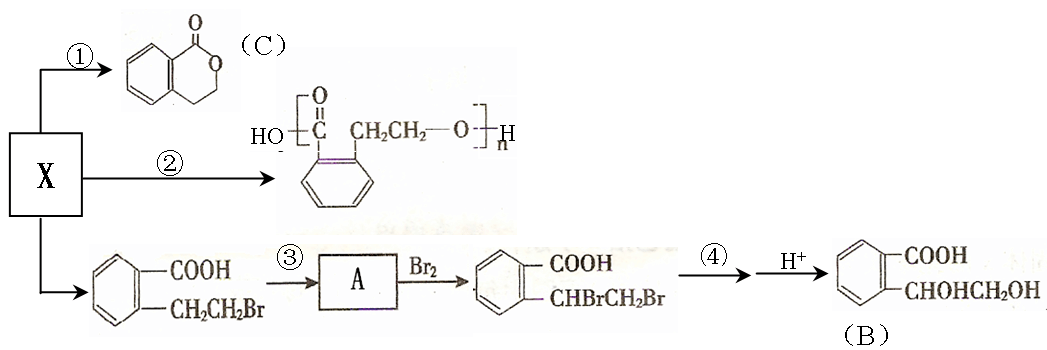
(Ⅰ)X的结构简式 ; B中含氧官能团的名称 ;
(Ⅱ)反应①的反应类型 、化合物C的分子式为 ;
(Ⅲ)反应④的试剂是NaOH的水溶液;反应④的化学方程式为 。
31. (16分)一定条件下,在一容积为4 L的密闭容器中通入0.4 molN2和1.2 molH2,发生反应:N2(g)+3H2(g)![]() 2NH3(g ) △H<0;
2NH3(g ) △H<0;
(1)当进行到第4分钟时达到平衡,生成NH3为0.4 mol,则从开始到达平衡时NH3的平均速率v(NH3)=_____________(注明单位)。
(2)该条件下,反应的平衡常数表达式K = ______ ,若降低温度,K值将_____(填“增大”“减小”“不变”)
(3)达到平衡后,若其它条件不变,把容器体积缩小一半,平衡将_____移动(“向逆反应方向”、“向正反应方向”或“不”).
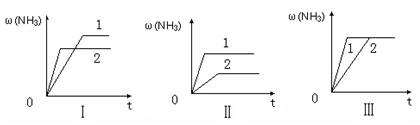
(4)在三个相同的容器中各充入1 molN2和3molH2,在不同条件下分别达到平衡,氨的体积分数随时间变化如图。下列说法正确的是
a.图Ⅰ可能是不同压强对反应的影响,且P2>P1
b.图Ⅱ可能是不同温度对反应的影响,且T1>T2
c.图Ⅲ可能是同温同压下,催化剂性能,1>2
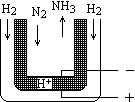 (5)常压下,把H2和用氦气(He)稀释的N2分别通入一个加热
(5)常压下,把H2和用氦气(He)稀释的N2分别通入一个加热
到570℃的电解池装置,H2和N2便可在电极上合成氨,
装置中所用的电解质(图中黑细点)能传导H+,则阴极的电极
反应式为___________________________。
32.(16分)制备多晶硅(硅单质的一种)的副产物以SiCl4为主,其对环境污染很大,遇水强烈水解,放出大量热量。研究人员利用SiCl4水解生成的盐酸和钡矿粉(主要成份为BaCO3,含有钙、铁、镁等离子)制备BaCl2·2H2O,流程为:
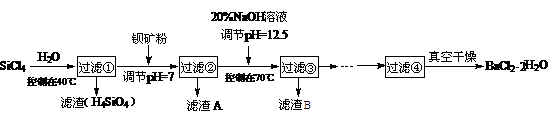
已知常温下Fe3+、Mg2+完全沉淀的pH分别是3.4和12.4;
(1) ① SiCl4水解控制在40℃以下的原因是 。
② 已知:SiCl4(s)+H2(g)=SiHCl3(s)+HCl(g) ΔH1=47 kJ/mol
SiHCl3(s)+H2(g)=Si(s)+3HCl(g) ΔH2=189 kJ/mol
则SiCl4被H2还原制备硅的热化学方程式 。
(2)加钡矿粉时生成BaCl2的离子反应方程式 。
(3)过滤②的滤渣A的成分化学式为 ;接着往滤液中加20% NaOH调节pH=12.5,控制温度70℃时,滤渣B的主要成分的化学式 ,控制温度70℃的目的 。
(4)滤液③经 、过滤等操作,再经真空干燥后得到BaCl2·2H2O。
33.(16分)某小组通过实验研究Na2O2与水的反应。
| 操作 | 现象 |
| 向盛有4gNa2O2的烧杯中加入50mL蒸馏水得到溶液a | 剧列反应,产生能使带火星木条复燃的气体 |
| 取5mL溶液a于试管中,滴入两滴酚酞 | ⅰ.溶液变红 ⅱ.10分种后溶液颜色明显变浅,稍后,溶液变为无色 |
(1)Na2O2与水反应的化学方程式 。
(2)ⅱ中溶液褪色可能是溶液a中存在较多的H2O2与酚酞发生了反应。
Ⅰ.甲同学通过实验证实了H2O2的存在:取少量溶液a,加入试剂 (填化学式),有气体产生。
Ⅱ.乙同学查资料获悉:用KMnO4可以测定H2O2含量: 取15.00mL溶液a,用稀H2SO4酸化,逐滴加入0.003mol·L-1KMnO4溶液,产生气体,溶液褪色速率开始较慢后变快,至终点时共消耗20.00 mL KMnO4溶液。
① 请配平: MnO4-+ H2O2+ H+== Mn2++ O2↑+ H2O
② 溶液a中c(H2O2)= mol·L-1。
③ 溶液褪色速率开始较慢后变快的原因可能是 。
(3)为探究现象ⅱ产生的原因,同学们继续实验:
Ⅲ.向H2O2溶液中滴入两滴酚酞,振荡,加入5滴0.1mol·L-1NaOH溶液,溶液变红又迅速变无色且产生气体,10分钟后溶液变无色。
Ⅳ.向0.1mol·L-1NaOH溶液中滴入两滴酚酞的,振荡,溶液变红,10分钟后溶液颜色无明显变化;向该溶液中通入O2,溶液颜色无明显变化。
① 从实验Ⅲ和Ⅳ中,可得出的结论 。
② 同学们通过进一步实验证实了溶液a中滴入酚酞后,H2O2与酚酞发生了化学反应。实验方案是:取少量溶液a于试管中, 。
2015年惠州市高三4月模拟考试
理科综合化学参考答案和评分标准
单选题:7.C 8.D 9.C 10.B 11.C 12.C(每题4分) ;
双选题:22.AD 23.BC(每题6分,选一个对的给3分)
30. (共16分)。
(1)bd(4分,选一个对的给2分))
(2) (或其它合理答案中的一种,2分)
(Ⅰ)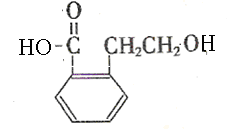 (2分) ; 羟基、 羧基 (2分,各1分)
(2分) ; 羟基、 羧基 (2分,各1分)
(Ⅱ)酯化反应或取代反应(1分); C9H8O2(2分,写成C9O2H8给1分)
(3)
(Ⅲ)
(3分,没有配平扣1分)
31.(16分)
(1)0.025 mol/(L·min)(数据2分,单位1分,共3分)
(2)![]() (3分) ;增大(2分)
(3分) ;增大(2分)
(3) 向正反应方向(2分);
(4)C(3分);(5)N2+6e-+6H+=2NH3(3分,没有配平扣1分)
32.(16分)
(1)(共2分)① 防止HCl挥发污染环境(1分);控制SiCl4的水解速率,防止反应过于剧烈(1分).
② SiCl4(s)+2H2(g)=Si(s)+4HCl(g) ΔH=236kJ/mol(4分,热量计算错误扣3分,没有标明状态扣1分,没有配平扣1分,没有单位扣1分,扣完为止)
(2)BaCO3+2H+=Ba2++CO2↑+H2O(2分,没有配平扣1分)
(3)Fe(OH)3(2分);Mg(OH)2、Ca(OH)2(2分)
确保钙离子完全除去(或温度越高,Ca(OH)2溶解度越小)。(2分)
(4)蒸发浓缩、降温结晶(2分)
33.(16分)
(1) 2Na2O2 + 2H2O =4NaOH+ O2↑(3分,没有配平扣1分)
(2)Ⅰ.MnO2(2分)
Ⅱ. ① 2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O(3分)
② 0.010(或0.01,2分)
③ 反应生成的Mn2+作催化剂(2分)
(3) ① 碱性条件下,H2O2能与酚酞反应而O2不能(2分);
② 加入MnO2,充分反应后,向上层清液中滴入2滴酚酞后变红,10分钟后,溶液颜色无明显变化(或10分钟后,看溶液的红色是否仍保持不变(2分)