
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日

可能用到的相对原子质量:H-1Li-7C-12N-14O-16Al-27Si-28S-32Cu-64
第Ⅰ卷
7.化学与社会密切相关,下列说法正确的是()
A.硝铵与草木灰不能混合使用,否则将使前者失去肥效,而后者仍有肥效
B.绿色化学的核心是应用化学原理对环境污染进行治理
C.可用于制作航天服的聚酯纤维是新型无机非金属材料
D.采用“静电除尘”、“原煤脱硫”、“汽车尾气催化净化”等方法,可提高空气质量
8.下列关于有机化合物的说法正确的是()
A.可用饱和碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯
B.苯与甲苯互为同系物,均能使酸性KMnO4溶液褪色
C.淀粉和纤维素不是同分异构体,但它们水解的最终产物是同分异构体
D.甲烷和氯气按体积比1∶2的比例混合后光照,生成的有机物全部是CH2Cl2
9.下列实验方案中,不能达到实验目的的是()
| 选项 | 实验目的 | 实验方案 |
| 资*源%库A | 验证Cl2的氧化性强于I2 | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,可观察到溶液变成蓝色 |
| B | 配制100mL 1.0 mol·L-1CuSO4溶液 | 将25gCuSO4·5H2O溶于100mL蒸馏水中 |
| C | 比较水与乙醇中氢的活泼性 | 分別将少量钠投入到盛有水和乙醇的烧杯中 |
| D | 验证Cu(OH)2的溶解度小于Mg(OH)2 | 将0.1mol·L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1 mol·L-1CuSO4溶液,可观察到先有白色沉淀生成,后变为浅蓝色沉淀 |
10.设NA为阿伏加德罗常数值,下列有关叙述正确的是()
A.46g组成为C2H6O的有机物.所含有的C-H 键数目为6NA
B.0℃l8mL冰含有质子数为10NA
C.氢氧燃料电池正极消耗22.4L气体时,电路中通过的电子数目为4NA
D.0.3molZn与一定量浓硫酸恰好完全反应,生成气体的分子数为0.3NA
11.电化学降解法可用于治理水中硝酸盐的污染,其工作原理如图所示。下列说法正确的是()
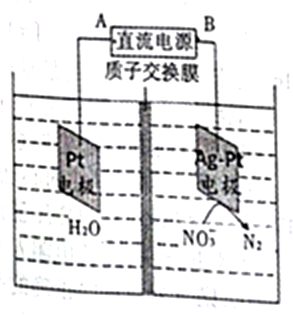
A.A极为负极,电子从铂电极流向该极
B.Pt电极上发生还原反应
C.Ag-Pt电极发生的反应是:2NO3-+6H2O+10e-=N2↑+12OH-
D.电解一段时间后,两地减少的质量一样多
12.短周期元素W、X、Y、Z、Q的原子序数依次增大,已知A、B、C、D是它们两种或三种元素间形成的化合物,且A、B、C均含有Z元素。A的焰色反应呈黄色,水溶液呈弱碱性;B是两性氢氧化物;D是由W与Q形成的化合物,0.1mol·L-1D溶液的pH为1。在一定条件下它们之间的相互转化关系如图所示。下列说法正确的是()
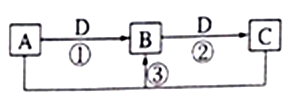
A.X、Y、Z元素的离子半径大小是X>Y>Z资*源%库
B.x元素的氢化物沸点比同主族元素的氢化物低
C.Y与Q和W与Q元素形成的化合物化学键类型相同
D.q的最高价氧化物对应的水化物和氢化物的酸性在同主族元素中是最强的
13.织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都只有漂白作用,但ClO2是有毒气体。25℃时,各组分浓度随pH变化情况如图所示(Cl-没有画出)。下列说法不正确的是()

A.25℃时,ClO2-的水解平衡常数Ka=10-6
B.在pH约为4.0~4.5范围内使用该漂白剂较好
C.25℃时,等浓度的HClO2溶液和NaClO2溶液等体积混合后,混合溶液中:
c(HClO2)+c(H+)+c(Na+)=c(ClO2-)+2c(OH-)
D.当pH=5时往NaClO2溶液中滴入稀氢氧化钠溶液,溶液中主要反应的离子方程式是:HClO2+OH-=H2O+ClO2-
26.(14分)据报道:研究人员破解了北京及华北地区雾霾主要成分硫酸盐的形成之谜,发现在大气细颗粒物吸附的水分中NO2与SO2的化学反应是当前雾霾期间硫酸盐的主要生成路径。某实验小组对NO2和SO2的反应进行探究。
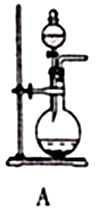
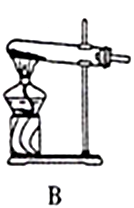

 资*源%库
资*源%库
图Ⅰ图Ⅱ
(1)SO2的发生装置可以选择图Ⅰ中的(填字母),反应的化学方程式为。
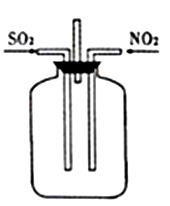
(2)按图Ⅱ所示进行实验。
①实验时往集气瓶中通入等体积的SO2和NO2,观察到集气瓶中有白烟产生,通入的NO2气体颜色变浅,该反应的化学方程式为。如果集气瓶中有少量水,则可能观察不到白烟,其原因是。
②请指出图Ⅱ装置设计的不合理之处。
(3)硫酸铵是我国pm2.5雾霾的主要成分,收集一定量的雾霾固体进行验证:
| 操作步骤 | 实验现象 | 结论 |
| 取一定量的雾霾固体于试管中,加入适量的水溶解,把溶液分成两份。 | ||
| 一份。 | 有白色沉淀生成。 | 证明雾霾固体中含有SO42- |
| 另一份。 | 。 | 证明雾霾固体中含有NH4+。综合上面实验,说明雾霾固体颗粒中含有(NH4)2SO4。 |
27.(14分)下图是氮元素在煤粉使用过程中的转化关系:
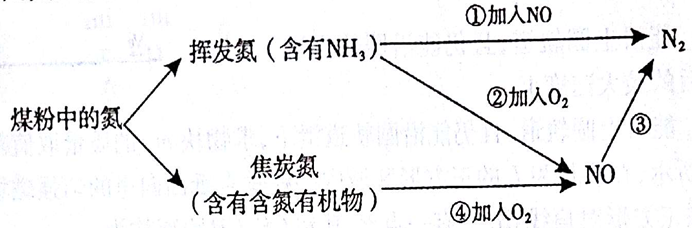
(1)③中加入的物质可以是(填标号)。
a.空气b.CO c.KNO3d.NH3
已知:N2(g) +O2(g)=2NO(g)△H = a kJ·mol-1
N2(g)+3H2(g)=2NH3(g)△H = b kJ·mol-1
2H2(g)+O2(g)=2H2O(l)△H = c kJ·mol-1
2CO(g)+O2(g)=2CO2(g)△H = d kJ·mol-1
上面转化关系反应后恢复至常温常压,根据以上信息写出③中你所选物质参与反应的热化学方程
式(如果所选物质不只一种,则只要写出其中一个热化学方程式即可)。
(2)将烟气中的氮氧化物(NOx)转化为无害物质,这个过程称为脱硝。下面反应为处理方法之一:
4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)△H = -1625.5kJ·mol-1
4N2(g)+6H2O(g)△H = -1625.5kJ·mol-1
①若反应生成1molN2,则反应中转移的电子数为mol。
②使上述反应速率增大且平衡向右移动的措施是。
③氨氮比会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,反应物X的转化率与氨氮比的关系如图所示,则X是(填化学式)。在体积为2L的容器中模拟进行上述反应,初始时加入8molNO和3.5molO2,氨氮比为0.5时,该反应的平衡常数K =(保留二位小数)。当n(NH3)/n(NO)>1.0 时,烟气中NO浓度反而增大,主要原因是(用化学方程式表示)。
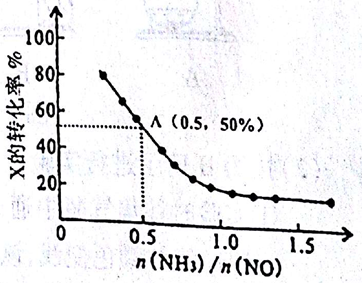
④若上述反应在与外界绝热的容器中进行,氨氮比由0.5增加到1.0时,在此过程中该反应的平衡常数(填“增大”、“减小”或“不变”)。
28.(15分)钛矿工业中会排放出酸性废水。含石TiO2+、Fe2+、Fe3+离子,其综合利用如下:
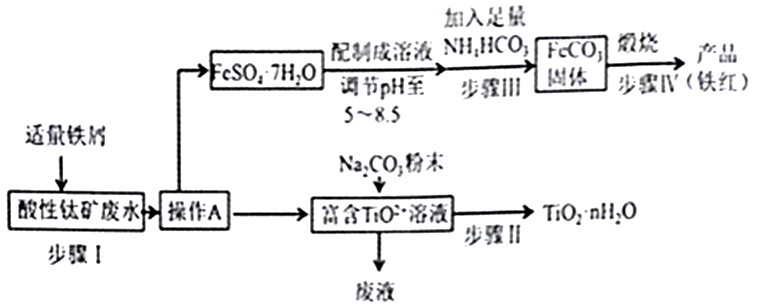
已知:TiO2+易水解,只能存在于强酸性溶液中。
(1)写出步骤Ⅰ发生反应的离子方程式。
(2)步骤Ⅰ后所得溶液中Fe2+的检验方法是。
(3)从溶液中得到FeSO4·7H2O的操作是、、过滤、洗涤。步骤Ⅲ中反应温度
一般需控制在35℃以下,其目的是。
(4)步骤Ⅳ发生反应的化学方程式为。
(5)步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5,c(Fe2+)=1×10-6mol·L-1。试判断所得的FeCO3中(填“有”或“没有”)F(OH)2(己知Fe(OH)2(已知Fe(OH)2的Ksp为8×10-16)
(6)向“富TiO2+溶液”中加入Na2CO3粉末得到固体TiO2·nH2O。请用化学原理解释其原因。
35.(15分)
(1)盐酸中加入六次甲基四胺对钢铁有一定缓蚀作用,右图为其结构简式,其分子式为(CH2)6N4,其中碳原子采用杂化,其缓蚀作用是因为分子中原子的孤对电子能与铁原子形成配位键,覆盖在钢铁表面。

(2)CO与N2属于等电子体,1个CO分子中含有的π键数目是个。
C、N、O三种元素的笫一电离能最大的是。
(3)右图是某化合物的晶胞示意图,硅原子与铝原子之间都以共价键连接。

①该化合物的化学式是。
②Si元素基态原子的电子排布式是。
③已知晶胞边长为5.93×10-8cm,Si与A1之间的共价键键长是cm(只要求列算式,不必计算出数值,下同),晶体的密度是g·cm-3
36.(15分)
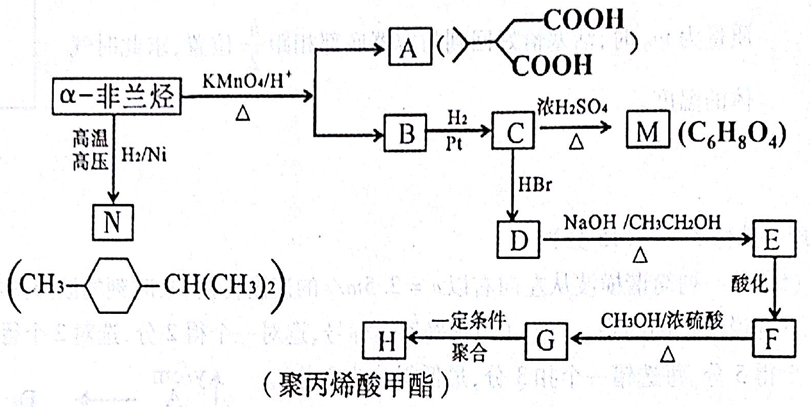
薄荷油中含有少量的a-非兰烃可以通过下列过程制得聚丙烯酸甲酯(H):
![]()
![]()
![]()
![]() +RˊCOOH
+RˊCOOH
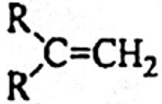
![]()
![]() +CO2
+CO2
(1)写出a-非兰烃的结构简式。写出C—M的反应类型。
(2)下面是对于A、B、C、D的性质描述,其中正确的是(填标号)。
a.lmol A 可与molNaHCO3反应放出2molCO2
b.lmolB可与2molH2发生加成反应
c.C可以发生缩聚反应
d.检验D的卤素原子种类可与NaOH水溶液共热后再加AgNO3溶液
(3)N的同分异构体中能同时满足下列两个条件的共有种(不含立体异构);其中核磁共振氢谱显示4组峰,且峰面积之比为4∶3∶2∶1的是(写结构简式)。
①含有一个六元环
②六元环上只有两个取代基,且环上每个碳原子最多只能有一个取代基
(4)E在一定条件下发生聚合反应可得到一种高级吸水树脂,写出生成该树脂反应的
化学方程式。
(5)写出F→G反应的化学方程式。
(6)BrCH2CH2CH2OH和甲醇也可以用来合成聚丙烯酸甲酯(H),写出合成路线(无机试剂任选,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件,合成路线常用的表示方式为:A![]() B……
B……![]() 目标产物)。
目标产物)。

一、选择题
7-10 DABD 11-13 CAC
二、非选择题
26.(14分)
(1)A(或C )(1分)
Na2SO3+H2SO4=Na2SO4+SO2↑+H2O(2分)
(2)①SO2+NO2=SO3+NO(2分) 生成的SO3与水反应生成硫酸(2分)
②没有进行尾气处理,会导致环境污染(2分)
(3)
| 操作步骤 | 实验现象 |
| $来&源:加入足量稀盐酸后,再加入BaCl2溶液(2分) | |
| 加入适量的NaOH浓溶液并加热(2分) | 产生使湿润的红色石蕊试纸变蓝色的气体(1分) |
27.(14分)
(1) bd(2分) 4NH3(g)+6NO(g)=5N2(g)+6H2O(l) ΔH= ( 3c-3a-2b) kJ·mol-1
(2分)
(2)①3(2分)
②增大反应物浓度(1分)
③NH3(1分) 0.09(3分) 4NH3+5O2![]() 4NO+6H2O(2分)
4NO+6H2O(2分)
④减小(1分)
28.(15分)
(1)2Fe3++Fe=3Fe2+(2分)
(2)取少量溶液于试管中,滴入几滴KSCN溶液,振荡,溶液不变色;再加入几滴氯水,溶液变红色(或取少量溶液于试管中,滴入几滴铁氰化钾溶液,生成蓝色沉淀)(3分)
(3) 蒸发浓缩(1分) 冷却结晶(1分) 防止NH4HCO3受热分解(1分)
(4)4FeCO3+O22Fe2O3+4CO2(2分)
(5)没有(2分)
(6) 因为存在TiO2++(n+1) H2O![]() TiO2·nH2O+2H+,当加入Na2CO3后,CO
TiO2·nH2O+2H+,当加入Na2CO3后,CO![]() 结合H+,c(H+)减小,TiO2+水解平衡正向移动(3分)
结合H+,c(H+)减小,TiO2+水解平衡正向移动(3分)
35.(15分)
(1)sp3杂化(2分) 氮(1分)
(2) 2(2分) N(1分)
(3)①LiAlSi(2分)
②1s22s22p63s23p2(2分)
③×5.93×10-8/4(2分)
(3分)
36.(15分)
(1)
![]() (2分) 酯化反应(或取代反应)(1分)
(2分) 酯化反应(或取代反应)(1分)
(2) ac(2分)
(3)9(2分) (1分)
(4)(2分)
(5)
(2分)
(6)
(3分,合理酌情给分)