
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2007年江苏省高等学校招生考试
化学试题
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28
S 32 Cl 35.5 K 39 Ca 40 Fe 56 Cu 64 Br 80
一、单项选择题:本题包括8小题,每小题4分。共计32分。每小题只有一个选项符合题意。
1.据估计,地球上的绿色植物通过光合作用每年能结合来自CO2中的碳1500亿吨和来自水中
的氢250亿吨,并释放4000亿吨氧气。光合作用的过程一般可用下式表示:
CO2+H2O + 微量元素(P、N等) (蛋白质、碳水化台物、脂肪等)+O2
下列说法不正确的是
A.某些无机物通过光合作用可转化为有机物
B.碳水化合物就是碳和水组成的化合物
C.叶绿素是光合作用的催化剂
D.增加植被,保护环境是人类生存的需要
2.下列叙述正确的是
A.聚丙烯的结构简式为: CH2-CH2-CH2
B.石英的化学式为:CaSiO3
C.在CS2、PCl3中各原子最外层均能达到8电子的稳定结构
D.Ar原子的结构示意图为![]()
![]()
3.三聚氰酸[C3N3(OH)3]可用于消除汽车尾气中的NO2。其反应原理为:
C3N3(OH)3 3HNCO; 8HNCO+6NO27N2+8CO2+4H2O
下列说法正确的是
A.C3N3(OH)3与HNCO为同一物质 B.HNCO是一种很强的氧化剂
C.1 molNO2在反应中转移的电子为4mol D.反应中NO2是还原剂
4.下列说法正确的是
A.原子晶体中只存在非极性共价键
B.稀有气体形成的晶体属于分子晶体
C.干冰升华时,分子内共价键会发生断裂
D.金属元素和非金属元素形成的化合物一定是离子化合物
5.下列有关实验的说法正确的是
A.除去铁粉中混有的少量铝粉。可加人过量的氢氧化钠溶液,完全反应后过滤
B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量
C.制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中
D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32-
6.向存在大量Na+、Cl-的溶液中通入足量的NH3后,该溶液中还可能大量存在的离子组是
A.K+、Br-、CO32-
B.Al3+、H+、MnO4-
C.NH4+、Fe3+、SO42-
D.Ag+、Cu2+、NO3-
7.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g); △H= + 49.0 kJ·mol-1
②CH3OH(g)+O2(g)=CO2(g)+2H2(g); △H=-192.9 kJ·mol-1
下列说法正确的是
A.CH3OH的燃烧热为192.9 kJ·mol-1
B.反应①中的能量变化如右图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l)+O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ·mol-1
8.阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是
A.2.24LCO2中含有的原子数为0.3 ×6.02×1023
B.0.1L3 mol·L-1的NH4NO3溶液中含有的NH4+数目为0.3 ×6.02×1023
C.5.6g铁粉与硝酸反应失去的电子数一定为0.3 ×6.02×1023
D.4.5 SiO2晶体中含有的硅氧键数目为0.3 ×6.02×1023
二、不定项选择题:本题包括8小题.每小题4分。共计32分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时该题为0分;若正确答案包括两个选项,只选一个且正确的
得2分,选两个且都正确的得满分,但只要选错一个,该小题就为0分。
9.下列离子方程式书写正确的是
A.过量的SO2通入NaOH溶液中:SO2+2OH-=SO32-+H2O
B.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2
C.NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O
D.NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32-
10.用下列实验装置完成对应的实验(部分仪器巳省略),能达到实验目的的是
A B C D
11.某同学按右图所示的装置进行电解实验。下列说法正确的是
A.电解过程中,铜电极上有H2产生
B.电解初期,主反应方程式为:Cu+H2SO4![]() CuSO4+H2↑
CuSO4+H2↑
C.电解一定时间后,石墨电极上有铜析出
D.整个电解过程中,H+的浓度不断增大
12.花青苷是引起花果呈颜色的一种花色素,广泛存在于植物中。它的主要结构在不同pH条件下
有以下存在形式:
下列有关花青苷说法不正确的是
A.花青苷可作为一种酸碱指示剂
B.I和Ⅱ中均含有二个苯环
C.I和Ⅱ中除了葡萄糖基外,所有碳原子可能共平面
D.I和Ⅱ均能与FeCl3溶液发生显色反应
13.一定温度下可逆反应:A(s)+2B(g)![]() 2C(g)+D(g);△H<0。现将1mol A和2molB加入甲容器中,
2C(g)+D(g);△H<0。现将1mol A和2molB加入甲容器中,
将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达
到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
A.保持温度和活塞位置不变,在甲中再加入1molA和2molB,达到新的平衡后,甲中C的浓度
是乙中C的浓度的2倍
B.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增人
C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数
是甲中C的体积分数的2倍
D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速
率变化情况分别如图2和图3所示(t1前的反应速率变化已省略)
14.有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同
(选项中m、n均为正整数)。下列说法正确的是
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+m,则X的最高正价一定为+m
15.下列溶液中各微粒的浓度关系不正确的是
A.0.1 mol·L-1HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+)
B.1 L 0.l mol·L-1CuSO4·(NH4)2SO4·6H2O的溶液中:c(SO42-)>c(NH4+))>c(Cu2+)>c(H+)>c(OH-)
C.0.1 mol·L-1NaHCO3溶液中: c(Na+)+c(H+)+c(H2CO3)=c(HCO3-)+c(CO32-)+c(OH-)
D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>(OH-)
16.某合金(仅含铜、铁)中铜和铁的物质的量之和为ymol,其中Cu的物质的量分数为a ,将其全部
投入50mLbmol·L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。
下列说法正确的是
A.若金属有剩余,在溶液中再滴入硫酸后,金属又开始溶解
B.若金属全部溶解,则溶液中一定含有Fe3+
C.若金属全部溶解,且产生336mL气体(标准状况),则b=0.3
D.当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80y(1-)
三、本题包括2小题.共计22分。
17.(10分)实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:
4NH4++6HCHO=3H++6H2O+(CH2)6N4H+[滴定时,1 mol(CH2)6N4H+与 l mol H+相当],
然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤I 称取样品1.500g。
步骤II 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置
5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。
按上述操作方法再重复2次。
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | ||
| 滴定前刻度/mL | 滴定后刻度/mL | |||
| 1 | 25.00 | 1.02 | 21.03 | |
| 2 | 25.00 | 2.00 | 21.99 | |
| 3 | 25.00 | 0.20 | 20.20 | |
| 同一反应时间 | 同一反应温度 | ||||
| 反应温度/℃ | 转化率(%) | 选择性(%) * | 反应时间/h | 转化率(%) | 选择性(%) * |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
| *选择性100 % 表示反应生成的产物是乙酸乙酯和水 | |||||
 BCDEF
BCDEF
(2)试通过计算确定该钠块中钠元素的质量分数。
25.(10分)钢铁工业是国家工业的基础。2006年我国粗钢产量突破4亿吨,居世界首位。
某中学社会实践活动小组利用假期对当地钢铁厂进行了调研,对从矿石开始到钢铁产出的工
艺流程有了全面的感性认识。请您对社会实践活动小组感兴趣的问题进行计算:
(1)将6.62 g铁矿石样品投入适量的盐酸中(充分反应),过滤,然后在滤液中加过量的NaOH 溶液,
充分反应后,过滤、洗涤、灼烧得4.80g Fe2O3。现以该铁矿石为原料炼铁,若生产过程中铁
元素损失4%,计算每生产1.00t生铁(含铁96%),至少需要这种铁矿石多少吨?
(保留两位小数)
(2)取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况)。
① 计算此钢样粉术中铁和碳的物质的量之比。
②再取三份不同质量的钢样粉末 分别加到100mL相通浓度的H2SO4溶液中,充分反 应后,
测得的实验数据如下表所示:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.812 | 5.624 | 8.436 |
| 生成气体的体积/L(标准状况) | 1.120 | 2.240 | 2.800 |
计算硫酸溶液的物质的量浓度。
③若在实验Ⅱ中继续加入mg钢样粉末,计算反应结束后剩余的固体质量为多少?
(用含m的代数式表示)
化学习题参考答案
一、单项选择题:本题包括8小题,每小题4分。共计32分。
1.B 2.C 3.C 4.B 5.A 6.A 7.D 8.D
二、不定项选择题:本题包括8小题.每小题4分。共计32分。
9.C 10.D 11.BC 12.B 13.BD 14.A 15.CD 16.AD
三、本题包括2小题.共计22分。
17.(10分)(1)①偏高 ②无影响 ③ B ④ 无 粉红(或浅红) (2) 18.85%
18.(12)分(1)增大乙醇的浓度 移去生成物
(2)原料来不及反应就蒸出 温度过高发生了副反应 冷凝效果不好,部分产物挥发了(任填两种)
(3)产生大量酸性废液(或造成环境污染) 部分原料炭化 催化剂重复使用困难 催化效果不理想 (任填两种)
(4)①C ②乙醇脱水生成了乙醚
四、本题包括2小题,共计18分
19.(8分)
(1)H2O NH3NH4+OH-
(2)Al3++3NH3+3H2O===Al(OH)3↓+3NH4+
Mg2++2NH3+2H2O===Mg(OH)2↓+2NH4+
20.(10分)
(1)NH4Cl 氯化钙 电子式
(2)Ca3N2+6H2O===3Ca(OH)2+2NH3↑
(3)3Cl2+2OH-===ClO-+Cl-+H2O
五、本题包括1小题,共计10分
21.(10分)(1)2H2SO3+O2===2H2SO42(NH4)2SO3+O2===2(NH4)2SO4
2NH4HSO3+O2===2NH4HSO4(任填两个)
(2)①反应吸热 ②(NH4)2SO3·H2O③防止亚硫酸铵被氧化
(3)BC
六、本题包括2小题,共计18分
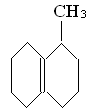
22.(8分)
(1)加成反应 氧化反应 还原反应
(2)2CH3CHOCH3CH=CHCHO+H2O
(3)H3C-O-![]() -C≡CH ,H3C-
-C≡CH ,H3C-![]() -O-C≡CH
-O-C≡CH
七、本题包括2小题.共计18分
24.(8分)
(1) ①2Na+2H2O===2NaOH+H2↑
②Na2O+H2O=2NaOH
③2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(2)n(Al)=(2)n(Al)==0.010 mol
根据反应③可得由铝消耗NaOH的物质的量为n(NaOH)=0.010mol
生成的氢气的物质的量为n(H2)=0.015mol
那么有金属钠生成的氢气的物质的量为n(H2)=n(H2)=-0.015mol=0.035mol根据反应①可得金属钠的物质的量n(Na)=2×0.035mol=0.070mol
又因为反应后溶液中的NaOH的物质的量为
n(NaOH)=2.0L×0.050mol·L-1=0.10mol
所以溶液中Na+的总物质的量即原金属钠的物质的量为
n(Na+)=0.10mol+0.010mol=0.11moln(Na2O)=n(Na2O)==0.020mol
该钠块中钠元素的质量分数为:
×100%≈89%
答:该钠块中钠元素的质量分数约为89%。
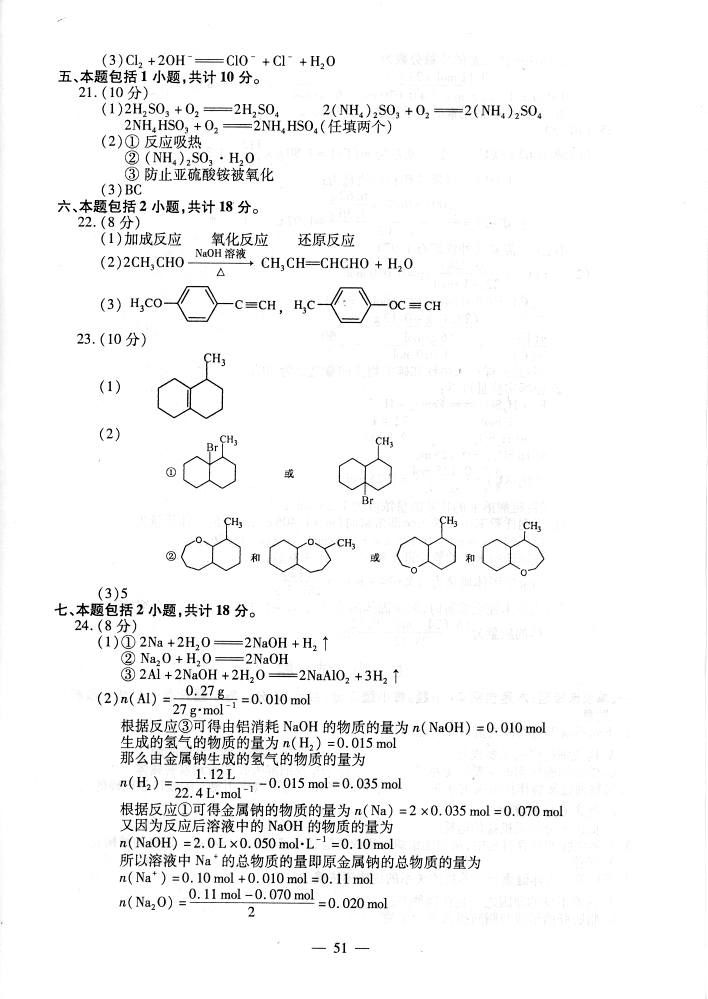
25.(10分)
(1)解:6.62g铁矿石中铁的质量为m(Fe)=4.80g×(1)解:6.62g铁矿石中铁的质量为m(Fe)=4.80g×=3.36g
生产1.00t生铁需铁矿石的质量为:
m(铁矿石)=1.00t×96%×m(铁矿石)= ≈ 1.97t
答:至少需要这种铁矿石1.97t。
(2)①n(C)=(2)①n(C)==0.010mol
m(C)=0.010mol×12g·mol-1=0.12g
= =
答:此钢样粉末中铁和C的物质的量之比为50:1 。②根据实验Ⅲ可得:
Fe+H2SO4=FeSO4+H2↑
1mol 22.4L
n(H2SO4) 2.800L
n(H2SO4)=1.125mol
c(H2SO4)=c(H2SO4)==1.25mol·L-1
答:硫酸溶液的物质的量浓度为1.25mol·L-1。
③当钢样粉末中的铁未全部溶解时(m>1.406g),剩余的固体质量为:
(5.624g+m g)-0.125mol×56g·mol-1=(m-1.376)g
当钢样粉末中的铁全部溶解时(m≤1.406g),剩余的固体质量为:
(5.624+m)g×
答:当铁未完全溶解时,剩余固体的质量为(m-1.376)g;
当铁完全溶解时,剩余固体质量为(5.624+m)g×