
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
![]()
![]() 2018年青岛市高三统一质量检测
2018年青岛市高三统一质量检测
理综化学2018.03
7.华夏文明源远流长,勤劳智慧的中国人民探索认知世界,创造美好生活的过程贯穿始终。以下说法从化学视角理解,错误的是
| A | 日照澄洲江雾开,淘金女伴满江隈(唐) | 诗中包含了丁达尔现象 |
| B | 高奴出脂水,颇似淳漆,燃之如麻(宋) | 文中提到的“脂水”是指油脂 |
| C | 水银乃至阴毒物,因火煅丹砂而出(明) | 这段记载中,涉及氧化还原反应 |
| D | 百宝都从海舶来,玻璃大镜比门排(清) | 制玻璃的某成分可用于制造光导纤维 |
8.设阿伏加德罗常数值用 NA表示,下列说法正确的是
A.标准状况下, 11.2L 乙醇中所含氧原子数大于 0.5NA
B. 18 g D2O 和 18 g H2O 中含有的质子数均为 10 NA
C. 25℃时, pH=7 的醋酸与醋酸钠混合溶液中, H+的个数为 1×10-7NA
D.向 100mL1mol·L-1Fe(NO3)3 溶液中滴加足量 HI 溶液,转移 0.1NA个电子
9. 中成药连花清瘟胶囊在对抗 H1N1病毒中发挥重大作用,其有效成分绿原酸的结构简式如图,下列有关说法错误的是
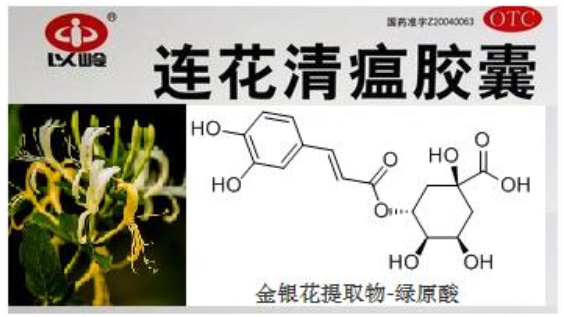
A.绿原酸属于芳香族化合物
B.分子中至少有 7 个碳原子共面
C. 1mol 绿原酸最多可消耗 5mol NaOH
D.与绿原酸苯环上取代基种类及个数均相同的有机物有5 种
10.短周期主族元素 W、X、Y、Z的原子序数依次增大,WX2为红棕色气体,Y的单质既能与强酸又能与强碱反应,W、Z 最外层电子数之和是X最外层电子数的2 倍。下列说法中错误的是
A.Y 与X、Y与Z均形成离子化合物
B.对应简单离子的半径:W>X>Y
C.Z 对应的最高价含氧酸是一元强酸
D.ZX2是一种消毒能力强于氯气且更加安全的自来水消毒剂
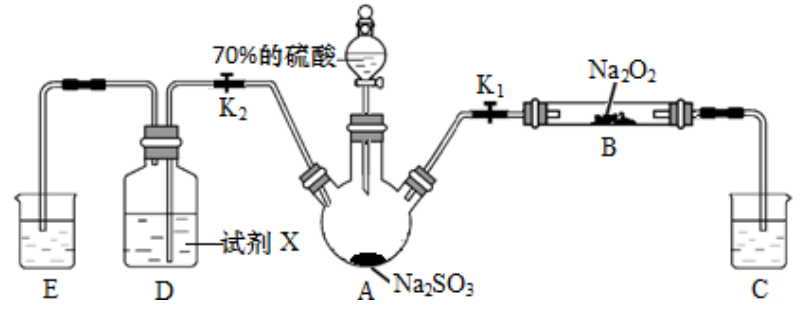
11. 如图是实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。下列有关说法正确的是
c.单位时间内生成 CO 和 NO 的物质的量相等 d. CO 和 CH3ONO 的浓度比不再变化
②10min 内该反应的速率 ν(NO)=____________;该温度下化学平衡常数 K=_________。若此时向容器中再通入0.4 mol NO,一段时间后,达到新平衡时 NO的体积分数与原平衡时相比______(填“增大”“相等”“减小”或“不能确定”)。
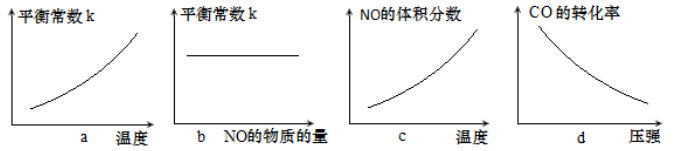
③若该反应△H<0,在恒容的密闭容器中,反应达平衡后,改变某一条件,下列示意图正确的是____________(填字母)。
27.(16 分)
碳酸镧咀嚼片是一种不含钙和铝的磷酸盐结合剂,用于慢性肾衰患者高磷血症的治疗。碳酸镧可由 LaCl3为原料来制备,整个反应在较低的pH条件下进行,避免生成碱式碳酸镧[La(OH)CO3]。
(1)化学兴趣小组利用下列装置在实验室中用碳酸氢铵制备碳酸镧。
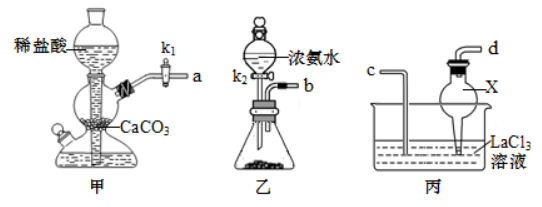
①仪器 X 的名称为________;检验装置甲气密性良好的方法是___________。
②实验中 K1、 K2打开的先后顺序为________;为保证碳酸镧的纯度,实验过程中需要注意的问题有____________。
(2)碳酸钠或碳酸氢钠与氯化镧反应均可生成碳酸镧。
①为了高磷血症患者的安全,通常选用碳酸氢钠溶液,过程中会发生两个平行反应,其离子方程式为_______和____________。
②选择碳酸氢钠溶液制备碳酸镧的优点是___________(任写一条)。
③T℃时,碳酸镧的溶解度为1.0×10-7mol·L-1, HCO3-的电离平衡常数为 6.0×10-11。请计算反应 2LaCl3+3NaHCO3![]() La2(CO3)3↓+3NaCl+3HCl 的平衡常数 K=_________。
La2(CO3)3↓+3NaCl+3HCl 的平衡常数 K=_________。
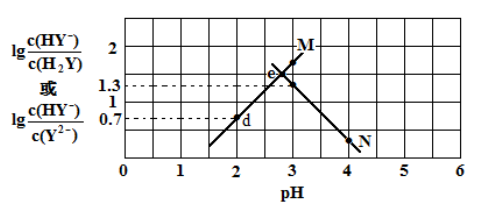
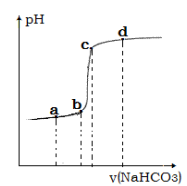
④利用手持技术测定溶液的 pH 从而监控反应过程,得到如图曲线。请说明 bc 段变化的原因__________。
(3)碳酸镧(式量为 458)质量分数的测定:准确称取15.0g产品试样,溶于10.0mL 稀盐酸中,加入 10mLNH3-NH4Cl 缓冲溶液,加入 0.2g 紫脲酸铵混合指示剂,用 0.5 mol·L-1EDTA(Na2H2Y)标准溶液滴定至呈蓝紫色(La3++H2Y2-= LaY-+2H+),消耗 EDTA 溶液 60.00mL。则产品中碳酸镧的质量分数 w=________。
28.(14 分)
锰主要用于钢铁工业生产锰合金钢,锰的化合物有+2、+4、+6、+7 等多种变价,以菱锰矿(主要成分为 MnCO3,还含有少量铁、镍、 钴等碳酸盐杂质)为原料经过一系列反应生产金属锰和高锰酸钾的工艺流程如下:
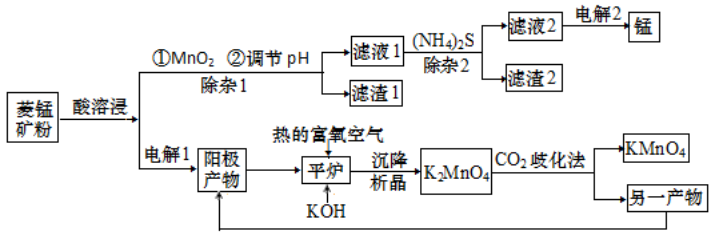
已知 25 ℃时,部分物质的溶度积常数如下:
| 物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(1)酸溶浸过程中,硫酸需稍过量,除保证反应充分进行外,其他作用还有_________(任写一条)。
(2)除杂1过程加入MnO2后,发生氧化还原反应的离子方程式为_________;滤渣2 的主要成分是____________________________。
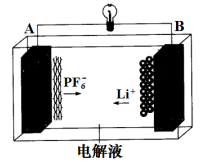
(3)为加快过滤速度,选择如图抽滤装置完成。下列有关操作和说法正确的是______。
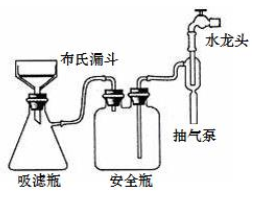
a. 抽滤的本质是加压过滤
b. 抽滤成功的关键在于合理控制水的流速
c. 微粒直径大于滤纸孔径的物质进入吸滤瓶中
(4)电解1过程阳极电极反应式为____________。
(5)H2O2 是一种常用的绿色氧化剂,在平炉反应中不用 H2O2的原因是__________。
(6)“CO2歧化法” 制备 KMnO4是传统工艺,写出该歧化反应的化学方程式_____________。
35.【物质结构与性质】 (15 分)
第四周期过渡元素如铁、锰、铜、锌等在太阳能电池、磁性材料等科技方面有广泛的应用,回答下列问题:
(1)在现代化学中,常利用______上的特征谱线来鉴定元素,称为光谱分析。
(2)写出 Cu2+的外围电子排布式__________;比较铁与锰的第三电离能(I3):铁____锰(填“>”、 “=”或“<”),原因是________________。
(3)已知 [Zn(CN)4]2-与甲醛在水溶液中发生反应可生成一种新物质 HOCH2CN,试判断新物质中碳原子的杂化方式___________;1mol[Zn(CN)4]2-中的 σ 键数为__________。
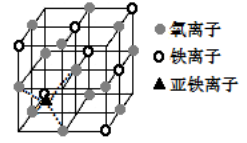
(4)如图是晶体 Fe3O4 的晶胞,该晶体是一种磁性材料, 能导电。
①晶胞中二价铁离子处于氧离子围成的______(填空间结构)空隙。
②晶胞中氧离子的堆积方式与某金属晶体原子堆积方式相同,该堆积方式名称为________。
③解释 Fe3O4 晶体能导电的原因_________________;若晶胞的体对角线长为 a nm,则 Fe3O4晶体的密度为________g·cm-3(阿伏加德罗常数用 NA表示)。
36.【有机化学基础】(15 分)
蜂胶是蜜蜂从植物芽孢或树干上采集的树脂。在蜂胶众多的功效成分中,咖啡酸苯乙酯(CAPE) 已经被鉴定为蜂胶中的主要活性组分之一。
已知:①A的核磁共振氢谱有三个波峰,红外光谱显示咖啡酸分子中存在碳碳双键。
②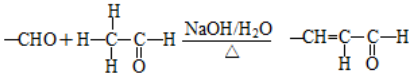
③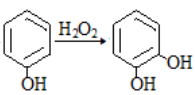
合成咖啡酸苯乙酯的路线设计如下:
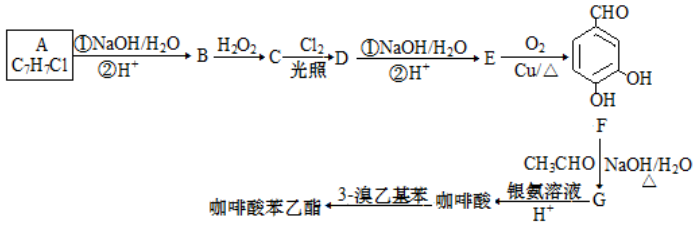
请回答下列各题:
(1)物质 A 的名称为________。
(2)由B生成C和C 生成 D 的反应类型分别是________、________。
(3) E 的结构简式为________。
(4)咖啡酸生成咖啡酸苯乙酯的化学方程式为________。
(5)芳香化合物X是G(C9H8O3)的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2,且与新制 Cu(OH)2反应生成砖红色沉淀,其核磁共振氢谱显示有5 种不同化学环境的氢,峰面积比为2:2:2:1:1,写出两种符合要求的X的结构简式________。
(6) 参照上述合成路线,以丙醛和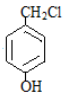 为原料(其他试剂任选),设计制备
为原料(其他试剂任选),设计制备 的合成路线。
的合成路线。
7.B 8.A 9.C 10.A 11.B 12.C 13.D
26. (13 分)
(1) 4H2(g)+2CO(g)+1/2O2(g)![]() HOCH2CH2OH(1)+2H2O(g) △H3=(1/2a+b+c)kJ·mol-1
HOCH2CH2OH(1)+2H2O(g) △H3=(1/2a+b+c)kJ·mol-1
(2 分) ;<(1 分)
(2) ① a bc(2 分)② 0.01mol··L-1·min-1(2 分);100(2 分);增大(2 分)③ b(2 分)
27. (16 分)
(1)①球形干燥管(1分) 关闭活塞 K1,向球形漏斗中加水至漏斗内外形成液面差,一段时间后,液面差保持不变,说明气密性良好。(2 分)
②先打开 K2 再打开 K1(1 分);控制氨气(或CO2)通入量(1分)
(2) ①2La2++3HCO3- = La2(CO3)3+3H+ (2 分) H++HCO3-=CO2+H2O(2 分)
②碳酸氢钠碱性相对较弱,可防止生成碱式碳酸镧[La(OH)CO3] (1 分)
③200(2 分)
④La3+完全沉淀, 再滴入碳酸氢钠,水解使溶液的碱性增强,pH发生突跃。(2分)
(3)45.8%(2 分)
28.(14 分)
(1)提供除杂 1 时所需要的酸性环境、抑制 Mn2+的水解(任写一种)(2 分)
(2) MnO2+2Fe2++4H+===Mn2++2Fe3++2H2O(2 分) CoS 和 NiS(2 分)
(3) b(2 分)
(4) Mn2++2H2O -2e-= MnO2+4H+(2 分)
(5) 锰的化合物可催化 H2O2 的分解,使消耗的 H2O2 增多(2 分)
(6) 3K2MnO4+4CO2+2H2O=2KMnO4+MnO2+4KHCO3或3K2MnO4+2CO2=2KMnO4+MnO2+2K2CO3(2 分)
35.(15 分)
(1) 原子光谱 (1 分)
(2) 3d9(1 分) 小于 (1 分) Mn2+、 Fe2+的价电子排布式分别为 3d5、 3d6, Mn2+处于 3d5半满较稳定结构,再失去一个电子所需能量较高, 所以第三电离能 Fe 小于 Mn。(2 分)
(3) sp3、 sp(1 分) 8NA(1 分)
(4) ①正四面体(2 分);②面心立方堆积 (2 分) ;③ 电子可在两种不同价态的铁离子间快速发生转移(2 分);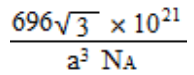 (2 分)
(2 分)
36.(15 分)
(1) 4-氯甲苯或对氯甲苯(2 分)
(2)氧化反应(1 分);取代反应(1 分)
(3)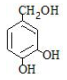 (2 分)
(2 分)
(4)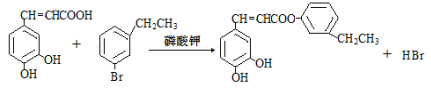 (2 分)
(2 分)
(5)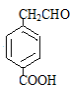 ;
;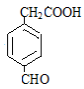 (4 分)
(4 分)
(6)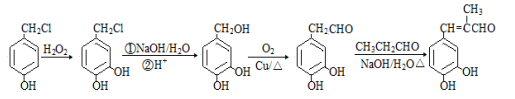 (3分)
(3分)