
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2016学年度第二学期
高一级化学科第一次段考试卷
本试题可能用到的相对原子质量是:H-1,N-14,O-16,Si-28, Fe-56, Cl-35.5, Cu-64,Ag-108
命题人:苏华虹 温培娴 审题人:郑章福
第Ⅰ卷(共60分)
一、单选题(本题包括20小题,每小题只有一个选项符合题意,各3分,共60分)
2.下列氯化物中,既能跟金属和氯气直接反应制得,又能由盐酸和金属反应制得的是( )
3. 下列操作不能用于检验NH3的是( )
A.气体使酚酞试液变红 B.气体能使湿润的红色石蕊试纸变蓝
C.气体与蘸有浓H2SO4的玻璃棒靠近 D.气体与蘸有浓盐酸的玻璃棒靠近
4. 将SO2和X气体分别通入BaCl2溶液中,未见沉淀生成,若同时通入,有沉淀生成,则X气体不可能是( )
A.CO2 B. NH3 C. Cl2 D. H2S
5.已知NH4CuSO3与足量的1mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断下列说法合理的是( )
A.NH4CuSO3中硫元素被氧化B.刺激性气味的气体是二氧化硫
C.刺激性气味的气体是氨气D.该反应中硫酸作氧化剂
6. 设阿伏加德罗常数的数值为NA,下列说法正确的是( )
C.1mol Cl2溶于水反应,转移的电子数目为NA
D. 1mol Cu与浓硝酸恰好完全反应,转移的电子数目为2NA
7.下列化学反应的离子方程式正确的是( )
A.在稀氨水中通入过量CO2:NH3·H2O+CO2===NH4++HCO3-
B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-===CaSO3↓+2HClO
C.用稀HNO3溶解FeS固体:FeS+2H+===Fe2++H2S↑
D.氢氧化钙溶液与等物质的量的稀硫酸混合: Ca2++OH-+H++SO42-===CaSO4↓+H2O
8. 14g铜银合金与足量的某浓度的硝酸反应,将放出的气体与1.12L(标况下)的O2混合,通入水中,恰好被全部吸收,则合金中铜的质量为( )
A.1.4g B.2.4g C.3.2g D.6.4g
9.已知SO2通入溴水中,能使溴水褪色。将SO2通入下列溶液中,溶液能褪色且褪色原理与溴水褪色原理类似的是( )
Na2CO3溶液 Na2SiO3溶液 稀盐酸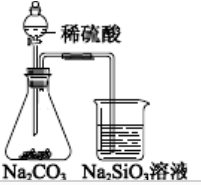
C.一段时间后②中有胶冻状物质生成
D.该实验能证明酸性强弱的顺序是:盐酸>碳酸>硅酸
 11.右图是产生和收集气体的实验装置,该装置适合于
11.右图是产生和收集气体的实验装置,该装置适合于
A.用浓盐酸和MnO2反应制取Cl2
B.用浓硝酸与Cu反应制取NO2
C.用稀硝酸和Cu反应制取NO
D.用浓氨水与生石灰反应制取NH3
12. 下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 向新制氯水中滴入紫色石蕊试液,溶液变红 | 新制氯水中含有H+ |
| B | 浓硫酸有吸水性 | 浓硫酸可用于干燥H2和NH3 |
| C | 常温下铝制贮罐贮运浓硫酸 | 常温下浓硫酸能使铝不反应 |
| D | 向FeCl2溶液中滴入几滴KSCN溶液,再滴加新制氯水,溶液由浅绿色变为血红色 | 新制氯水中的Cl2将Fe2+氧化 |
13.下列物质中,既有离子键,又有共价键的是 ( )
A.H2O B.CaCl2 C.KOH D.Cl2
4.下列说法正确的是( )
A.氢键是一种化学键 B.同种非金属元素间不可能形成离子键 $来&源:
C.非金属元素间不可能形成离子化合物 D.离子化合物中一定不存在共价键
15. 最新科技报导,美国夏威夷联合天文中心的科学家发现了新型氢微粒,这种新微粒是由 3个氢原子核(只含质子)和2个电子构成,对于这种微粒,下列说法中正确的是( )
A.是氢的一种新的同素异形体 B.是氢的一种新的同位素
C.它的组成可用H3表示 D.它比一个普通H2分子多一个氢原子核
16.下列说法正确的是( )
A.形成离子键的阴阳离子间只存在静电吸引力
B.HF、HCl、HBr、HI的熔、沸点随着相对分子量的增大而增大
C.第三周期非金属元素含氧酸的酸性从左到右依次增强
D.元素周期律是元素原子核外电子排布周期性变化的结果
17.下列各组微粒半径大小比较中,不正确的是( )
C. r( Na+)>r(Mg2+)>r(Al3+) D. r(Cl-)>r(F-)>r(F)
18.元素周期表里金属元素和非金属元素分界线附近能找到( )
A.新制农药元素 B.制催化剂元素
C.制半导体元素D.制耐高温合金元素
 19. 下列电子式中,正确的是 ( )
19. 下列电子式中,正确的是 ( )
A.![]() B.
B.![]() C. D.
C. D.![]()
20. 短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数是其电子层数的2倍,X、Y的核电荷数之比为3:4。W−的最外层为8电子结构。金属单质Z在空气中燃烧生成的化合物可与水发生氧化还原反应。下列说法正确的是 ( )
第Ⅱ卷(共40分)
二、非选择题:共3题,共40分。
21.下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
| 周期 族 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)②③⑦的最高价含氧酸的酸性由弱到强的顺序是(用化学式表示) _______ ,
(3)写出由以上①④⑤元素构成的化合物的电子式______________________;该化合物含有的化学键类型有__________________。
(3)用电子式表示⑤元素的单质和⑧元素的单质形成化合物的过程。
22. (16分)(1)工业上通过高温分解FeSO4的方法制备Fe2O3,化学方程式为:
2FeSO4Fe2O3+ SO3↑ + SO2↑
为检验FeSO4高温分解的产物,进行如下实验:
检验FeSO4高温分解产生的气体,将FeSO4高温分解产生的气体通入下图装置中。
 $来&源:
$来&源:
A B C
① 装置A试管可选用的试剂是________________(填标号)。
② 装置C的作用是防止尾气污染环境,试管中应加入的试剂是 。
③ 若装置B试管中溶液改为酸性KMnO4溶液,可以观察到溶液紫色褪去,反应的离子方程式为 。
(2)工业上在一定温度和催化剂条件下用NH3将NO2还原生成N2,某同学在实验室中对NH3与NO2反应进行了探究。

①实验室可以用A、B或C装置制取氨气,如果用C装置,则该装置中烧瓶所盛放的试剂为________(写名称);反应的化学方程式是________ ;
② 预收集一瓶干燥的氨气,选择下图中的装置,其气体收集和尾气处理装置连接顺序依次为:发生装置→ (用字母表示)

D E F G H
③ 将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按下图装置进行实验。打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中,Y管观察到的实验现象是 ,反应的化学方程式为 。

23.(12分)将32.0 gCu投入50mL 12moL/L的浓硝酸中,充分反应后,收集到4.48L(标准状况)NO和NO2的混合气体。
2016学年度第二学期
高一级化学科第一次段考答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | A | B | C | A | C | D | A | C | D | D |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | C | D | C | B | C | D | D | C | A | D |
①氧化钙(或碱石灰、固体氢氧化钠等) (2分);
NH3·H2O==NH3+H2O (2分,没有加热符号或气体符号扣一分)
② D F H (2分)
③ 红棕色气体逐渐褪色 (2分)
8NH3+6NO27N2+12H2O (2分)
(3)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O(4分,离子方程式2分,单线桥2分);
6e-