
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
巍山一中2015~2016学年上学期高二年级期末考化学试题
说明: 1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,本试卷满分100分,考试时间120分钟;
2.第Ⅰ卷(选择题)答在机读卡上的相应位置, 第Ⅱ卷要求用碳素笔在答题卡上规定区域作答。
可能用到的相对原子质量:H-1 C-12 O-16 Ca-40
第Ⅰ卷(48分)
一.选择题(本题共24个小题,每小题只有一个选项是符合题意,每小题2分。)
由此得出的正确结论是( )
A.O2比O3稳定,由O2变O3为放热反应
B.O3比O2稳定,由O2变O3为吸热反应
C.等质量的O2比O3能量低,由O2变O3为吸热反应
D.等质量的O2比O3能量高,由O2变O3为放热反应
8. 已知298 K时,合成氨反应N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.2 kJ/mol,此温度下,将1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)( )
2NH3(g) ΔH=-92.2 kJ/mol,此温度下,将1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)( )
A.一定大于92.2 kJ B.一定等于92.2 kJ
C.一定小于92.2 kJ D.无法确定
9. 有一处于平衡状态的反应:X(g)+3Y(g)![]() 2Z(g)(正反应是放热反应)。为了使平衡向生成Z的方向移动,应选择的条件是( )
2Z(g)(正反应是放热反应)。为了使平衡向生成Z的方向移动,应选择的条件是( )
①升高温度 ②降低温度 ③增大压强 ④降低压强
⑤加入正催化剂 ⑥分离出Z
A.①③⑤ B.②③⑤ C.②③⑥ D.②④⑥
10. 关于铅蓄电池的说法正确的是( )
A.在放电时,正极发生的反应是:Pb(s)+SO(aq)= ==PbSO4(s)+2e-
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是:PbSO4(s)+2e-===Pb(s)+SO(aq)
11. 氨水的下列性质中,不能证明它是弱电解质的是( )
A.1 mol·L-1的氨水溶液中c(OH-)=0.01 mol·L-1
B.常温下,将PH为12的氨水溶液加水稀释100倍,稀释后的溶液PH大于10
C.10 mL 1 mol·L-1的氨水溶液恰好与10 mL 1 mol·L-1的盐酸完全反应
D.在相同条件下,氨水溶液的导电性比NaOH溶液弱
12.对于反应:2X(g)+Y(g)![]() 2Z(g)在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量n(Z)和反应时间t的关系如图所示,下列判断正确的是( )
2Z(g)在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量n(Z)和反应时间t的关系如图所示,下列判断正确的是( )
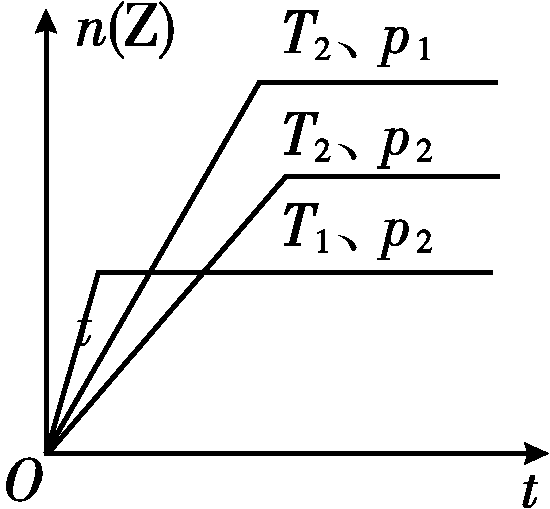 A.T1>T2,p1>p2,正反应为放热反应
A.T1>T2,p1>p2,正反应为放热反应
B.T1
C.T1
D.T1>T2,p1
13.用惰性电极电解AgNO3溶液,下列说法不正确的是( )
A.电解过程中阴极质量不断增加
B.电解过程中溶液的pH不断降低
C.此时向溶液中加入适量的Ag2O固体可使溶液恢复到电解前的状况
D.电解后两极产生的气体体积比为2∶1
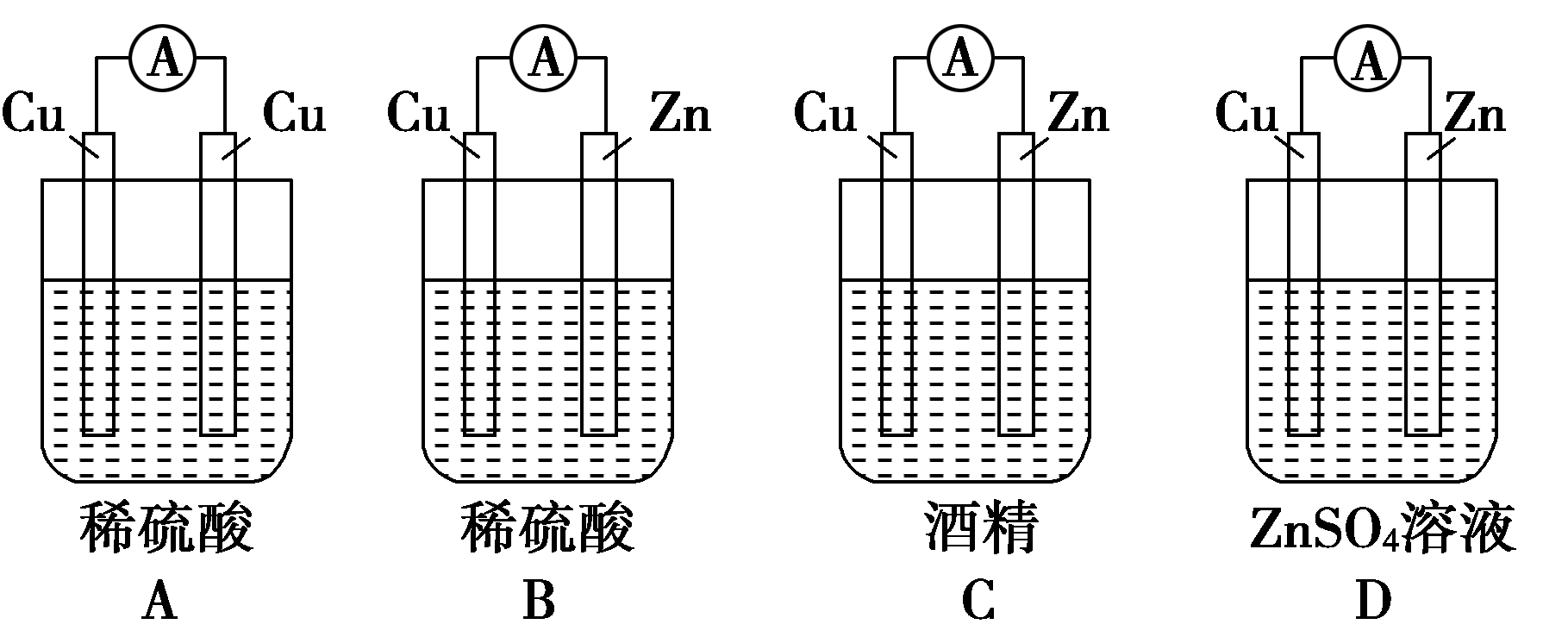
14. X、Y、Z、W四块金属板分别用导线两两相连浸入稀硫酸中构成原电池。X、Y相连时,X为负极;Z、W相连时,外电路电流方向是W→Z;X、Z相连时,Z极上产生大量气泡;W、Y相连时,W极发生氧化反应。据此判断四种金属的活动性顺序是 ( )
A.X>Z>W>Y B.Z>X>Y>W C.X>Y>Z>WD.Y>W>Z>X
15. 将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g) = 3C(g)。若2 s末测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3 mol·L-1·s-1;
②用物质B表示的反应的平均速率为0.1 mol·L-1·s-1;
③2 s末,物质A的转化率为30%; ④2 s末,物质B的浓度为0.8 mol·L-1。
其中正确的是( )
A.①③ B.②④ C.①④ D.③④
16. 2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1
现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应热为3 695 kJ。则原混合气体中H2与CH4的物质的量之比是( )
A.1∶1 B.1∶3 C.1∶4 D.2∶3
17.常温下0.1 mol·L-1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是( )
A.将溶液稀释到原体积的10倍
B.加入适量的醋酸钠固体
C.加入等体积0.2 mol·L-1盐酸
D.提高溶液的温度
18. 下列关于电解质溶液的判断正确的是( )
A.在pH=12的溶液中,K+、Cl-、HCO、Na+可以大量共存
B.在pH=0的溶液中,Na+、NO、SO、K+可以大量共存
C.由0.1mol·L-1一元碱BOH溶液的PH=10,可推知BOH在溶液中的电离是BOH=B++OH-
D.由0.1 mol·L-1一元酸HA溶液的PH=3,可推知NaA溶液中存在A-+H2O![]() HA+OH-
HA+OH-
19.(2014·天津高考)下列有关电解质溶液中粒子浓度关系正确的是( )
A.pH=1的NaHSO4溶液:c(H+)=c(SO)+c(OH-)
B.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-)
C.CO2的水溶液:c(H+)>c(HCO)=2c(CO)
D.含等物质的量的NaHC2O4和Na2C2O4的溶液: 3c(Na+)=2[c(HC2O)+c(C2O)+c(H2C2O4)]
20. (2015·新课标重庆卷)黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为: S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol-1
已知碳的燃烧热ΔH1=a kJ·mol-1
S(s)+2K(s) =K2S(s) ΔH2=bkJ·mol-1
2K(s)+ N2(g)+ 3O2(g) = 2KNO3(s) ΔH3=ckJ·mol-1
则为
A.3a+b-cB.c+3a-b C.a+b-c D.c+a-b
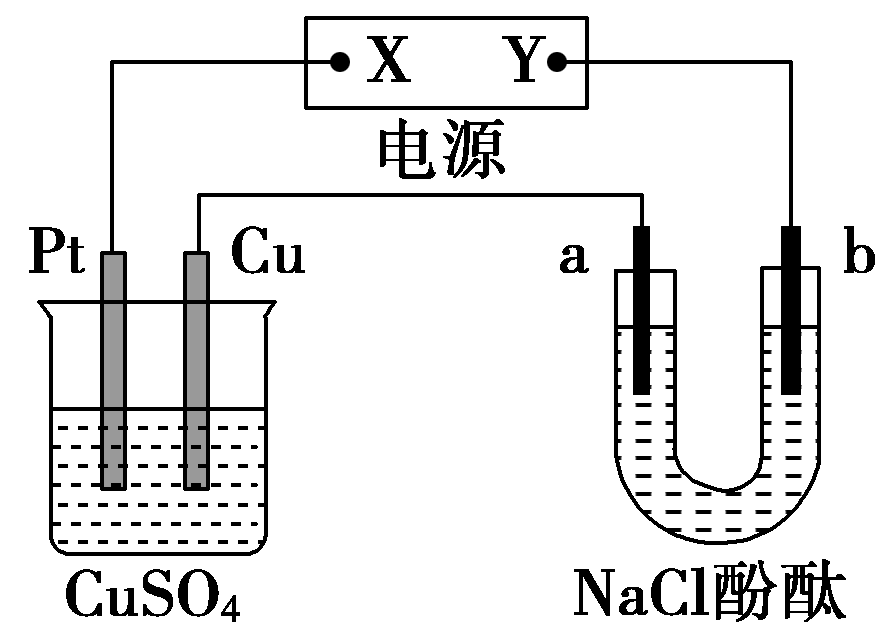 21.如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色。下列说法正确的是( )
21.如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色。下列说法正确的是( )
①X是正极,Y是负极 ②X是负极,Y是正极
③CuSO4溶液的pH逐渐减小 ④CuSO4溶液的pH不变
A.①③ B.①④ C.②③ D.②④
22. 为了提纯下表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
| 编号 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 乙烷(乙烯) | 酸性KMnO4溶液 | 分液 |
| B | 淀粉溶液(NaCl) | 水 | 过滤 |
| C | 苯(甲苯) | NaOH溶液 | 分液 |
| D | 甲烷(乙烯) | 溴水 | 洗气 |
23. 在碱性锌锰干电池中,已知氢氧化钾为电解质,发生的电池总反应为:Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2。下列该电池的电极反应,正确的是( )
A.负极反应为Zn-2e-===Zn2+
B.负极反应为Zn+2H2O-2e-===Zn(OH)2+2H+
C.正极反应为2MnO2+2H++2e-===2MnOOH
D.正极反应为2MnO2+2H2O+2e-===2MnOOH+2OH-
24. 某有机样品3.1 g完全燃烧,燃烧后的混合物通入过量的澄清石灰水中,石灰水共增重7.1 g,经过滤得到10 g沉淀。该有机样品可能是( )
A.甲醇 B.乙醇 C.乙二醇 D.乙醛
第Ⅱ卷 (52分)
25.(8分) (1)写出下列反应的化学方程式
①铝与氢氧化钠溶液反应:_______________________________________
②二氧化硫通入氯水的反应:_______________________________________
(2)写出下列反应的离子方程式
①碳酸钠溶液显碱性的原因:_______________________________________
②小苏打溶液中滴加硫酸铝溶液:_______________________________________
26. (8分) (1)氢氧燃料电池的电极反应式随电解质溶液的不同而不同。电池的负极通的应是________,如果电解质溶液为KOH,则负极电极反应式为_____________________。如果电解质溶液为稀H2SO4则正极电极反应式为____________________________________。
(2)甲烷燃料电池,KOH作电解质溶液,负极电极反应式为:______________。
 27.(8分) 已知某原电池的电极反应是Fe-2e-===Fe2+,Cu2++2e-===Cu,据此设计该原电池,并回答问题。
27.(8分) 已知某原电池的电极反应是Fe-2e-===Fe2+,Cu2++2e-===Cu,据此设计该原电池,并回答问题。
①电极材料X可以是________(填序号,下同)。
a.铁 b.铜 c.石墨
②电解质Y是________。
a.FeSO4 b.CuSO4 c.CuCl2
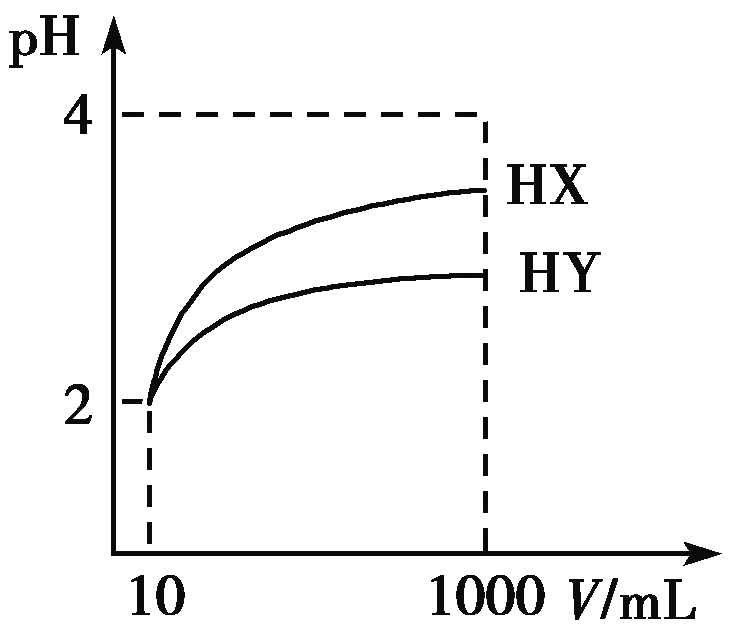
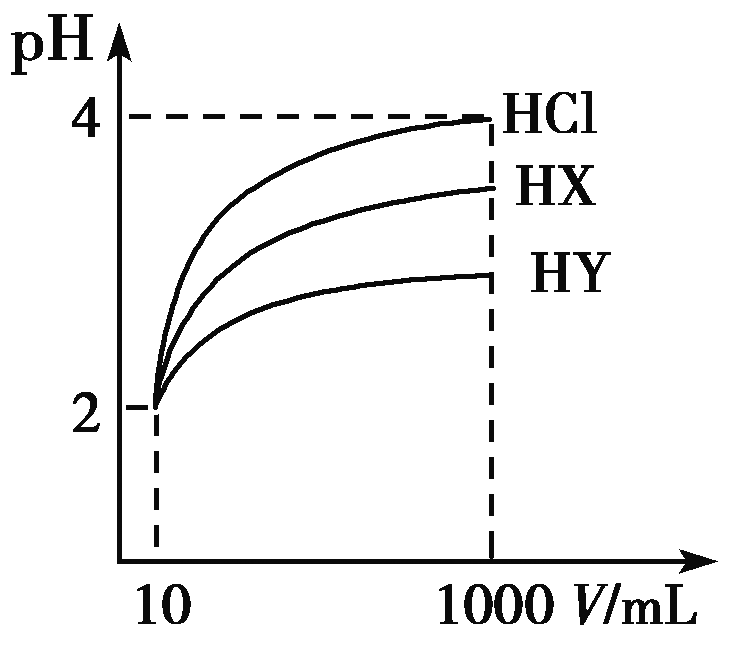
28. (8分)常温下,10 mL pH均为2的HX、HY两种一元酸溶液,加水稀释过程中溶液的pH随溶液体积变化曲线如图所示。
请回答下列问题:
29. (10分) 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| 实验步骤 | 解释或实验结论 |
| 试通过计算填空:(1)A的相对分子质量为:________。 |
| (2)将此9.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g | (2)A的分子式为:________。 |
| (3)另取A 9.0 g,跟足量的NaHCO3粉末反应,生成2.24 L CO2(标准状况),若与足量金属钠反应则生成2.24 L H2(标准状况) | (3)写出A中含有的官能团的结构简式:_______________ ______________ |
(4)A的核磁共振氢谱如下图: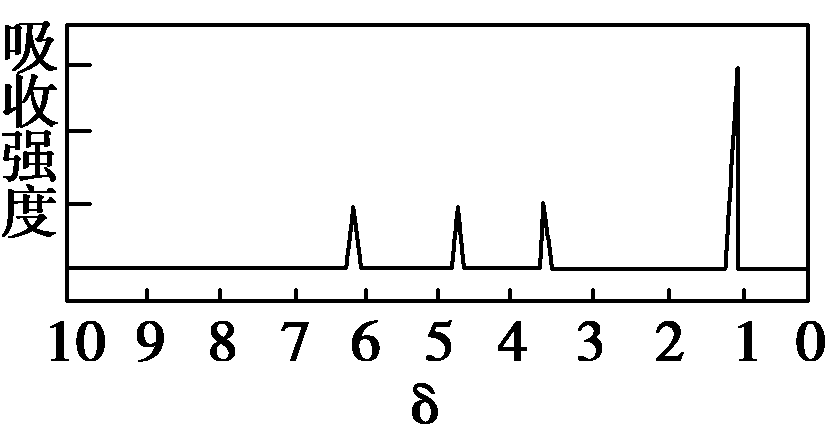 | (4)A中含有__________种氢原子。 |
| (5)综上所述,A的结构简式为________。 | |
30.(10分)
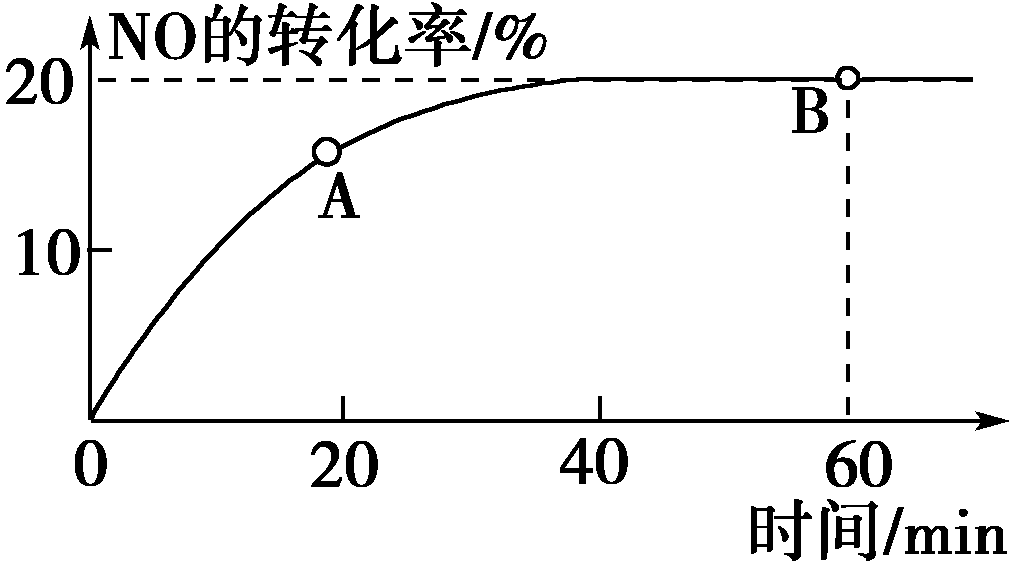
① H2O(l)===H2O(g) ΔH=+44 kJ·mol-1,写出液态肼与液态双氧水反应生成N2和液态水的热化学方程式:_________________________________________________________。
②以N2和H2为原料通过一定途径可制得N2H4,已知断裂1 mol N—N键、N≡N键、N—H键、H—H键所需的能量分别为193 kJ·mol-1、946 kJ·mol-1、390.8 kJ·mol-1、
436 kJ·mol-1,试写出由N2、H2合成气态肼(N2H4)的热化学方程式为______________________。
巍山一中2015~2016学年上学期高二年级期中考
化学参考答案
第Ⅰ卷 单选题(每题2分,共48分)
| 题 号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答 案 | B | D | D | C | B | A | C | C | C | B | C | A |
| 题 号 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 |
| 答 案 | D | A | B | B | B | D | A | A | A | D | D | C |
第Ⅱ卷 非选择题(共52分)
25.(8分) (1)写出下列反应的化学方程式
①2Al+2NaOH+22NaAlO2+3H2↑ ②SO2+Cl2+2H2O=H2SO4+2HCl
(2)写出下列反应的离子方程式
①CO32-+H2O![]() HCO3-+OH-(使用等号不给分!) ②3HCO3-+Al3+=Al(OH)3↓+3CO2↑
HCO3-+OH-(使用等号不给分!) ②3HCO3-+Al3+=Al(OH)3↓+3CO2↑
26. (8分) (1)H2 负极:2H2+4OH--4e-===4H2O O2+4H++4e-===2H2O
(2) CH4+10OH--8e-===CO+7H2O
 27.(8分)
27.(8分)
29. (10分)【答案】 (1)90 (2)C3H6O3(3)—COOH —OH
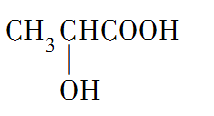 (4)4 (5)
(4)4 (5)
30.(10分)
②N2(g)+2H2(g)===N2H4(g) ΔH=+61.8 kJ·mol-1