
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
海南省国兴中学2017届高三第三次月考
化学试卷
可能用到的相对原子质量:H~1 O~16 C~12 N~14 Na~23 Cl~35.5 Br~80
第一卷选择题(36分)
一、选择题(本题共6小题,每小题2分,共12分。在每小题给出的四个选项中,只有一个是正确的。)
1.对于易燃、易爆、有毒的化学物质,往往会在其包装上贴上危险警告标签。下面所列物质,包装标签贴错了的是( )
| A | B | C | D | |
| 物质化学式 | 浓HNO3 | C2H6O | CO2 | KClO3 |
| 危险警告标签 | 腐蚀性 | 易燃性 | 有毒性 | 爆炸性 |
2.下列仪器的名称,正确的是()
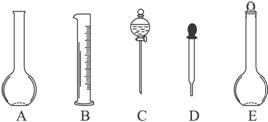
A.①:容量瓶②:量筒③:分液漏斗④:胶头滴管⑤:平底烧瓶
B①:平底烧瓶②:容量瓶③:分液漏斗④:胶头滴管⑤:量筒
C①:平底烧瓶②:量筒③:分液漏斗④:胶头滴管⑤:容量瓶
D①:平底烧瓶②:容量瓶③:分液漏斗④:胶头滴管⑤:量筒
3.下列各组物质反应不能产生O2的是( )
A.过氧化钠与水 B. 金属钠与水
C.二氧化锰与过氧化氢 溶液 D.二氧化锰与氯酸钾
4.下列有关金属铝及其化合物的叙述正确的是
$来&源:B.实验室可用氯化铝溶液与氢氧化钠溶液制备氢氧化铝
C.铝可用于冶炼某些熔点较高的金属 D.氧化铝只能与酸反应,不能与碱反应
5.在氯化铁、氯化铜和盐酸混合溶液中加入铁粉,待反应结束,所剩余的固体滤出后能被磁铁吸引,则反应后溶液中存在较多的阳离子是( )
A.Cu2+ B.Fe3+ C.Fe2+ D.H+
6.下列对物质用途的描述,错误的是( )
A.浓硫酸可用于干燥SO2、H2、O2等气体
B.二氧化硫可用来漂白纸浆、毛、丝等
C.一氧化二氮可用做医学麻醉剂D.铝制容器可用来盛放及运输稀硝酸
二、选择题(本题共6小题,每小题4分,共24分,每小题有1~2个选项符合题意。若正确答案只包括一个选项,多选的0分,若正确答案包括两个选项,只选一个且正确得2分,选两个且正确得4分,但只要选错一个就得0分。)
7.已知KMnO4与浓HCl在常温下反应能产生Cl2。若用图2所示的实验装置来制备纯净、干燥的氯气,并试验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是( )
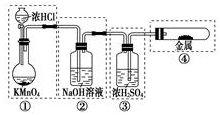
A.只有①和②处 B.只有②处C.只有②和③处 D.只有②③④处
8.下列实验操作中,错误的是( )
A.倾倒液体时试剂瓶标签面向手心
B玻璃棒蘸取溶液滴到放在表面皿上湿润的pH试纸上
C.用HCl溶液洗涤并灼烧铂丝后,再进行焰色反应
D.KOH溶液保存在带磨口玻璃塞的试剂瓶中。
9.下列分离或提纯物质的方法正确的是( )
A.用过滤的方法分离氢氧化铁胶体和氯化铁溶液B.用汽油萃取溴水中的溴
C.用溶解、过滤的方法提纯含有少量硫酸钡的碳酸钾
D.用分液可分离乙酸乙酯和乙醇混合物
10.分子式为C5H12的有机化合物的一氯代物有()
A.5种B.8种C.6种D.7种
11、对于某些离子的检验及结论一定正确的是
A、加入硫氰化钾溶液,溶液显血红色,一定有Fe3+
B、加入足量的氨水,有白色沉淀产生,一定有Al3+
C、加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
D、加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
12.常温下,下列各组物质能用一种试剂通过化学反应区别的是( )
A.MgO CuO FeO B. Na2CO3 K2SO4 NH4Cl
资*源%库C.AgNO3 KNO3 Na2CO3D.Na2CO3 NaHCO3 K2CO3
$来&源:
第二卷非选择题(64分)
本卷共6题
13.(8分)下图每一字母代表一种反应物或生成物。已知在常温下A是含氧酸盐固体,B、E、F、G均为气态化合物,X为气态单质。根据反应框图完成下列问题(有些反应条件已略去)。
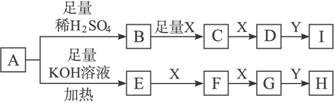
(1)A物质的化学式为____________________。
(2)写出A→E转化的离子方程式:
(3)写出发生下列转化的化学方程式:
A→B___________________________________________________________。
F→G __________________________________________________________;
(4)将B通入H的浓溶液中,会有红棕色的G生成,反应的化学方程式:
14.(10分)某钠盐溶液可能含有阴离子CO32-,SO32-,SO42-,NO3-,Cl-,Br-,I-。为鉴定这些离子,分别取少量溶液进行以下实验:
①加HCl后,生成无色无味气体。该气体能使饱和石灰水溶液变浑浊;
②加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀能完全溶解;
③加CCl4,滴加少量氯水,振荡后,CCl4层未变色;
④加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
⑤加铜片后,再滴加适量浓硫酸,有红棕色气体生成。
分析上述5个实验,填写
(1)肯定存在的阴离子是,肯定不存在的阴离子是,
(2)请分析实验③所得的结论及理由
(3)写出实验②所有的离子方程式是 。
(4)写出实验⑤反应的离子方程式是 。
15.(10分) A、B、C、D、E、F、G、H和I是中学化学中常见的气体,它们均由短周期元素组成,具有如下性质:
①将足量I通入硝酸银溶液中,开始有白色沉淀生成,后沉淀又溶解。
②A能使湿润的蓝色石蕊试纸变红,也可用来做喷泉试验;
③E能使品红溶液褪色,加热又恢复红色。
④B能使湿润的碘化钾淀粉试纸变蓝,也能使湿的红布条褪色。
⑤将点燃的镁条放入装有F的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
⑥D能使带火星的木条复燃;
⑦G是非金属性最强的单质
$来&源:⑧将B和H在瓶中混合后于亮处放置几分钟,瓶内壁出现油状液滴并产生A。
⑨C为密度最小的气体
回答下列问题:
资*源%库(1)A的化学式是___,C的化学式是____;F的化学式是______ H的化学式是____
(2)G与水发生反应的化学方程式是___________________________________;
(3)将湿润的B和E混合,彼此的漂白能力会减弱,原因为(用化学方程式表达)
(4)工厂中,可用B检测是否有I泄漏。若有,会看得白色烟雾。用化学方程式表达该检测原理
16.(8分)以乙炔为主要原料合成聚氯乙烯的流程为下图。
资*源%库(1)乙炔的实验室制法是分子空间构型是
(2)写出①步的化学反应方程式
(3)已知乙炔在一定条件下能发生如下反应:
A.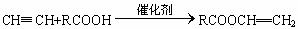
B.能与水反应生成乙醛
现以乙炔为原料(无机试剂任选)合成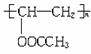 ,写出各步反应的化学方程式。
,写出各步反应的化学方程式。
17.(8分)由某校化学小组学生利用图1-2装置进行“氨的催化氧化及其产物验证”实验。(图中夹持装置已略去)
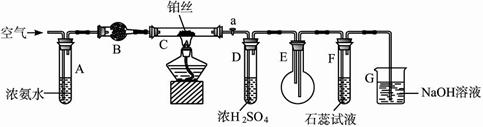
。
(6)写出氨气的实验室制法的化学方程式
(7)实验室中,还可用下列方法制备氨气()
a.加热浓氨水 b.加热氯化铵固体
c.浓氨水 与氢氧化钠 固体混合 d.用氢气和氮气反应
18-Ⅰ(6分)糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述正确的是( )
A.油脂不能使溴的四氯化碳溶液褪色B.淀粉水解的最终产物是葡萄糖
C.葡萄糖能发生氧化反应和银镜反应
D.蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水
18-Ⅱ(14分)化合物C和E都是医用功能高分子材料,且有相同的元素百分组成,均可由化合物A(C4H8O3)制得,如下图所示,B和D互为同分异构体。
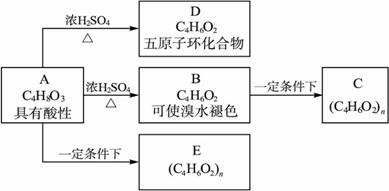
请写出:
(1)A的结构简式是其蒸气密度是O2(相同状况)的倍
(2)B分子中的含氧官能团名称是 ,B→C的的反应类型是
(3)写出化学方程式A→D: ,
A→E ;
(4)符合下列条件的A的同分异构体的结构简式为 ,
a.能水解,也能发生银镜反应。b.能与金属钠反应放出气体
c.核磁共振氢谱有三组峰,且峰面积之比为1:1:6
海南省国兴中学2017届高三第三次月考
化学试卷答案
1答案:C2答案:C3答案:B 4答案:C 5答案:C 6答案:D
7答案 D 8答案为:B D 9答案为:B C 10答案为:B
11答案为:AC 12答案为:A C
13.答案:
(1)(NH4)2SO3或NH4H SO3
(2)
(3)3NO2+3H2O![]() 2H NO3+ NO
2H NO3+ NO
(4)SO2+ 2H NO3=== H2SO4 + 2NO2
14.答案:
(1)①肯定存在是CO32-、、NO3-、Cl-
肯定不存在是SO42-SO32-Br-,I-
②
③
15答案:
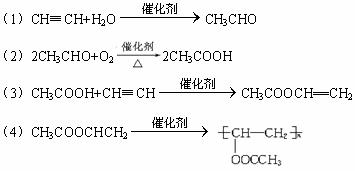
17.答案:
(3)吸收水蒸汽及反应剩余的氨气
(4)红棕 NO2(5)3NO2+H2O=2HNO3+NO
(6) (7) ac
18-Ⅰ答案: B C
18-Ⅱ