
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
闵行区2014学年第二学期高三年级质量调研考试
化学试卷
考生注意:
1.答卷前,考生务必在答题纸上将学校、姓名及准考证号填写清楚,并在规定的区域填涂相关信息。答题时客观题用2B铅笔涂写,主观题用黑色水笔填写。
2.本试卷共有56题,共8页。满分150分,考试时间120分钟。
3.请将答案写在答题纸上,考试后只交答题纸,试卷由考生自己保留。
相对原子质量:H-1 C-12 N-14 O-16 Na-23 Al-27
一、选择题(本题共10分,每小题2分,每题只有一个正确选项)
1.化学与人类生活密切相关。下列说法正确的是
A.矿物油和植物油都可以通过石油分馏来获取
B.硫酸亚铁可作补血剂组成成分
C.蛋白质的水解产物都是α-氨基酸
D.造成PM2.5的直接原因是土壤沙漠化
2.下列化学用语使用正确是
A.氧原子能量最高的电子的电子云图:![]() B.35Cl与37Cl互为同素异形体
B.35Cl与37Cl互为同素异形体
C.CH4分子的比例模型:![]() D.
D.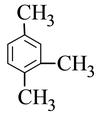 的命名:1,3,4-三甲苯
的命名:1,3,4-三甲苯
3.与溴水反应不会产生沉淀的是
A.乙烯 B.AgNO3溶液 C.H2S D.苯酚
4.结构片段为…―CH2―CH=CH―CH2―…的高分子化合物的单体是
A.乙烯 B.乙炔 C.正丁烯 D.1,3-丁二烯
5.2015年2月,科学家首次观测到化学键的形成。化学键不存在于
A.原子与原子之间 B.分子与分子之间
C.离子与离子之间 D.离子与电子之间
二、选择题(本题共36分,每小题3分,每题只有一个正确选项)
6.下列事实能用元素周期律解释的是
A.沸点:H2O>H2Se>H2S B.酸性:H2SO4>H2CO3>HClO
C.硬度:I2>Br2>Cl2D.碱性:KOH>NaOH>Al(OH)3
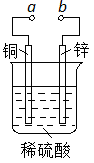 7.右图可设计成多种用途的电化学装置。下列分析正确的是
7.右图可设计成多种用途的电化学装置。下列分析正确的是
A.当a和b用导线连接时,溶液中的SO42-向铜片附近移动
B.将a与电源正极相连可以保护锌片,这叫牺牲阳极的阴极保护法
C.当a和b用导线连接时,铜片上发生的反应为:2H++2e →H2↑
D.a和b用导线连接后,电路中通过0.02mol电子时,产生0.02mol气体
8.常温下,往饱和石灰水中加入一定量的生石灰,一段时间后恢复到原温度,以下叙述错误的是
A.有溶质析出 B.溶液中Ca2+的数目不变
C.溶剂的质量减小 D.溶液的pH不变
9.液态氨中可电离出极少量的NH2-和NH4+。下列说法正确的是
A.NH3属于离子化合物 B.常温下,液氨的电离平衡常数为10-14
C.液态氨与氨水的组成相同 D.液氨中的微粒含相同的电子数
10.将燃着的H2S不断通入盛有一定量O2的集气瓶中。当火焰熄灭后继续通入H2S,发生的主要反应是
A.2H2S+O2→2S+2H2O B.2H2S+3O2→2SO2+2H2O
C.2H2S+SO2→3S+2H2O D.2SO2+O2→2SO3
11.右图是用于制取、收集并吸收多余气体的装置,下列方案正确的是
| 选项 | X | Y | 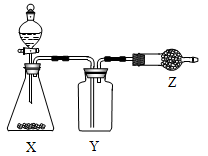 Z Z |
| A | 食盐、浓硫酸 | HCl | 碱石灰 |
| B | CaO、浓氨水 | NH3 | 无水CaCl2 |
| C | Cu、浓硝酸 | NO2 | 碱石灰 |
| D | 电石、食盐水 | C2H2 | 含溴水的棉花 |
12.下列工业生产过程中涉及到反应热再利用的是
A.接触法制硫酸 B.联合法制纯碱
C.铁矿石炼铁 D.石油的裂化和裂解
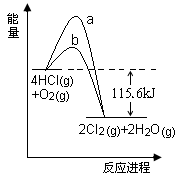
13.在催化剂、400℃时可实现氯的循环利用,右图是其能量关系图,下列分析正确的是
A.曲线a是使用了催化剂的能量变化曲线
B.反应物的总键能高于生成物的总键能
C.反应的热化学方程式为:
4HCl(g) + O2(g)![]() 2Cl2+2H2O(g)-115.6 kJ
2Cl2+2H2O(g)-115.6 kJ
D.若反应生成2mol液态水,放出的热量高于115.6kJ
14.某未知溶液可能含Na+、NH4+、Fe2+、I-、Cl-、CO32-、SO32-。将该溶液加少量新制氯水,溶液变黄色。再向上述反应后溶液中加入BaCl2溶液或淀粉溶液,均无明显现象。下列推断合理的是
A.一定存在Fe2+、Na+、Cl-B.一定不存在I-、SO32-
C.一定呈碱性 D.一定存在NH4+
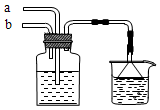 15.模拟侯氏制碱法原理,在CaCl2浓溶液中通入NH3和CO2可制得纳米级材料,装置见图示。下列说法正确的是
15.模拟侯氏制碱法原理,在CaCl2浓溶液中通入NH3和CO2可制得纳米级材料,装置见图示。下列说法正确的是
A.a通入适量的CO2,b通入足量的NH3,纳米材料为Ca(HCO3)2
B.a通入足量的NH3,b通入适量的CO2,纳米材料为Ca(HCO3)2
C.a通入适量的CO2,b通入足量的NH3,纳米材料为CaCO3
D.a通入少量的NH3,b通入足量的CO2,纳米材料为CaCO3
16.反应2NO2(g)![]() N2O4(g) + 57 kJ,若保持气体总质量不变。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
N2O4(g) + 57 kJ,若保持气体总质量不变。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
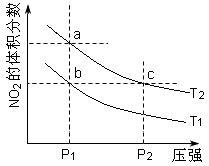 A.a、c两点气体的颜色:a浅,c深
A.a、c两点气体的颜色:a浅,c深
B.a、c两点气体的平均相对分子质量:a>c
C.b、c两点的平衡常数:Kb=Kc
D.状态a通过升高温度可变成状态b
17.在高温高压的水溶液中,AuS-与Fe2+发生反应沉积出磁铁矿(主要成分Fe3O4)和金矿(含Au),并伴有H2S气体生成。对于该反应的说法一定正确的是
A.氧化剂和还原剂的物质的量之比2:3
B.AuS-既作氧化剂又作还原剂
C.每生成2.24 L气体,转移电子数为0.1mol
D.反应后溶液的pH值降低
三、选择题(本题共20分,每小题4分,每小题只有一个或两个正确选项。只有一个正确选项的,多选不给分;有两个正确选项的,选对一个给2分,选错一个,该小题不给分)
18.下列各选项中对应的实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现 象 | 结 论 |
| A | 在试管中滴入适量C2H5X与NaOH溶液,振荡、加热、静置分层后,取水层加稀硝酸酸化,再滴加数滴AgNO3溶液 | 淡黄色沉淀 | 证明卤代烃中含有溴元素 |
| B | 将蘸有浓氨水的玻璃棒置于某无机酸浓溶液的试剂瓶口 | 有大量白烟 | 该无机酸一定为盐酸 |
| C | 在大试管中依次加入适量丁醇、过量乙酸、几滴浓硫酸,混合后塞上带长导管的试管塞,放在石棉网上方空气中加热至120℃左右 | 反应液沸腾,冷却静置,上层油状透明液体有水果香味 | 该油状液体为乙酸丁酯 |
| D | 在简易启普发生器中向石灰石中加入浓醋酸,将产生的气体直接通入苯酚钠溶液中 | 苯酚钠溶液产生浑浊 | 酸性:醋酸>碳酸>苯酚 |
19.混合下列各组物质使之充分反应,将所得混合物加热蒸干,并在300℃灼烧至质量不变为止,最终残留固体为纯净物的是
A.向CuSO4溶液中加入适量铁粉 B.等浓度等体积的(NH4)2SO4和BaCl2
C.等物质的量的NaHCO3和Na2O2D.在NaBr溶液中通入过量的Cl2
20.向等物质的量浓度的NaOH和Ca(OH)2的混合液中通入一定量CO2。下列离子方程式与事实不相符的是
A.OH-+CO2→ HCO3-
B.2OH-+CO2→ CO32-+H2O
C.Ca2++2OH-+CO2→ CaCO3↓+H2O
D.Ca2++4OH-+2CO2→ CaCO3↓+CO32-+2H2O
21.25℃时,NH3·H2O和CH3COOH的电离常数K相等。下列说法正确的是
A.常温下,CH3COONH4溶液的pH=7,与纯水中H2O的电离程度相同
B.向CH3COONH4溶液加入CH3COONa固体时,c(NH4+)、c(CH3COO-)均会增大
C.常温下,等浓度的NH4Cl和CH3COONa两溶液的pH之和为14
D.等温等浓度的氨水和醋酸两溶液加水稀释到相同体积,溶液pH的变化值一定相同
22.向含1 mol NaOH、2 mol NaAl(OH)4、1 mol Ba(OH)2的混合液中加入稀硫酸充分反应,加入溶质H2SO4的量和生成沉淀的量的关系正确的是
| 选项 | A | B | C | D |
| n(H2SO4)/mol | 2 | 3 | 4 | 5 |
| n(沉淀) /mol | 2 | 3 | 2 | 1.5 |
四、(本题共12分)
TiCl4是一种重要的化工原料,其工业生产过程如下:
2FeTiO3(s) + 7Cl2(g) + 6C (s) ![]() 2TiCl4(g) + 2FeCl3(g) + 6CO(g) – Q (Q>0)
2TiCl4(g) + 2FeCl3(g) + 6CO(g) – Q (Q>0)
23.该反应达到平衡后,若使正反应速率增大可采取的方法有_________。(选填编号)
24.若上述反应在固定体积的密闭容器中发生,一定能说明反应已达平衡的是_______。(选填编号)
a. 反应物不再转化为生成物 b. 炉内FeTiO3与TiCl4的质量比保持不变
c. 反应的热效应不再改变 d. 单位时间内,n(FeTiO3)消耗:n(FeCl3)生成=1:1
25.上述反应中所有非金属元素原子的半径从大到小的顺序为_____________;其中不属于同周期又不属于相邻族的两元素形成____________分子(填“极性”或“非极性”),通过比较____________可以判断这两种元素的非金属性。
26.上述反应中,非金属性最弱的元素原子的电子共占据_______个原子轨道,最外层电子排布式为____________。它形成的固态单质中只含一种强烈的相互作用力,则该单质属于______晶体。
27.为方便获得氯气,工业制TiCl4厂可以和氯碱厂进行联合生产。CO可合成甲醇,若不考虑损失,上述联合生产在充分利用各种副产品的前提下,合成192 kg甲醇,至少需补充H2mol。
五、(本题共12分)
含硫化合物在生产、生活中有广泛应用,其吸收和处理也十分重要。
28.SO2具有还原性,写出将SO2气体通入 FeCl3溶液中的离子方程式,并标出电子转移的数目及方向。
______________________________________________________________________
29.在Na2SO3溶液中滴加酚酞,溶液变红色,若在该溶液中滴入过量的BaCl2溶液,现象是___________________________________,请结合离子方程式,运用平衡原理进行解释_______________________________________________________。
30.等体积等物质的量浓度的 NaClO溶液与Na2SO3溶液混合后,溶液显______性。
此时溶液中浓度相等的微粒是___________________________________________。
31.已知:H2S:Ki1=1.3×10-7Ki2=7.1×10-15H2CO3:Ki1=4.3×10-7Ki2=5.6×10-11
含H2S尾气用足量的Na2CO3溶液来吸收。写出离子反应方程式。
______________________________________________________________________
常温时,等体积等浓度的Na2S和Na2CO3溶液的离子总数:N前___N后(填“>”或“<”)。
六、(本题共12分)
碘及其化合物可广泛用于医药和工业生产等。
32.实验室用海带提取I2时操作步骤依次为:灼烧、溶解、过滤、_______、_______及蒸馏。
33.灼烧海带时除需要三脚架、酒精灯、玻璃棒外,还需要的实验仪器是______________。
34.“过滤”后溶液中含一定量硫酸盐和碳酸盐。现要检验溶液中的I-,需选择的试剂组合及其先后顺序是_____________。(选填编号)
a.AgNO3溶液 b.Ba(NO3)2溶液 c.BaCl2溶液 d.CaCl2溶液
35.在海带灰滤液中加入适量氯水后一定存在I2,可能存在IO。
请补充完整检验含I2溶液中是否含有IO的实验方案(可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液):
①取适量含I2溶液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在;
②_____________________________________________________________________。
36.分解水可用SO2/I2循环法。该法共涉及三步化学反应。
___________________;2H2SO4![]() 2SO2↑+ O2↑+ 2H2O;____________________。
2SO2↑+ O2↑+ 2H2O;____________________。
与传统的分解水的方法相比,本法的优点是____________;缺点是_____________。
七、(本题共12分)
某兴趣小组用合金铝、铁、铜的废弃合金为原料制取硝酸铜晶体和氢氧化铝,并测定硝酸铜晶体的结晶水含量和氢氧化铝的纯度,设计的主要流程如下:
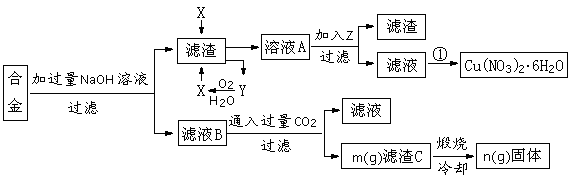
已知:Fe2+沉淀的pH范围为7.0~9.0;Fe3+沉淀的pH范围为1.9~3.2;
Cu2+沉淀的pH范围为4.7~6.7
37.写出合金中加入NaOH溶液后所发生的离子反应方程式_______________________。
试剂X的名称为______________。
38.加入Z的作用是调节溶液的pH,pH范围应为_____;下列可作为试剂Z的是_______。
a.铜粉 b.氨水 c.氧化铜 d.硫酸铜
39.实验操作①依次是_________、_________、过滤洗涤即可得硝酸铜晶体。
40.测定硝酸铜晶体的结晶水含量,下列方案中肯定不可行的是 。(选填编号)
a.称量样品→加热→冷却→称量CuO
b.称量样品→加热→冷却→称量Cu(NO3)2
c.称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量
d.称量样品→加过量已知量的NaOH溶液→选用酚酞指示剂用标准盐酸滴定
41.根据流程图内数据计算:滤渣C中氢氧化铝的质量分数为______________________。(用m、n的代数式表示)
42.按该流程的操作步骤,氢氧化铝质量分数的测定结果偏高的可能性是最大的,原因有_______________________________;____________________________________。
八、(本题共8分)
有机物聚合物M:![]() 是锂电池正负极之间锂离子迁移的介质。由烃C4H8合成M的合成路线如下:
是锂电池正负极之间锂离子迁移的介质。由烃C4H8合成M的合成路线如下:
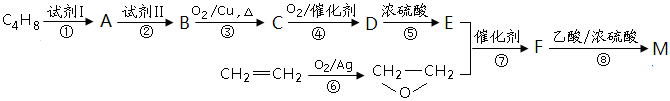
43.C4H8的结构简式为_________________,试剂II是________________。
44.检验B反应生成了C的方法是___________________________________________。
45.D在一定条件下能发生缩聚反应生成高分子化合物,反应的化学方程式为___________________________________________;
46.反应步骤③④⑤不可以为⑤③④的主要理由是_______________________________。
九、(本题共14分)
以下是由甲苯合成乙酰水杨酸和酚酞的合成路线。
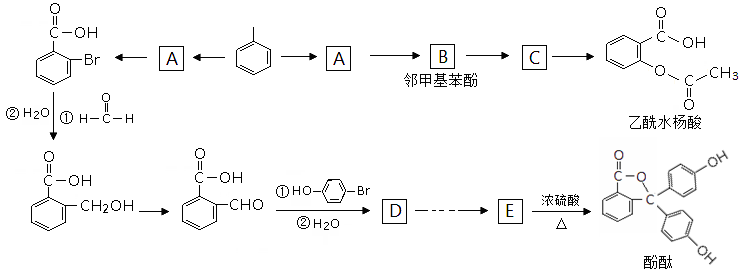
47.写出“甲苯→A”的化学方程式___________________________________________。
48.写出C的结构简式___________,E分子中的含氧官能团名称为__________________;
49.上述涉及反应中,“E→酚酞”发生的反应类型是______________。
50.写出符合下列条件的乙酰水杨酸的一种同分异构体的结构简式_________________。
(1)遇FeCl3溶液显紫色, (2)能与碳酸氢钠反应,
(3)苯环上只有2个取代基的, (4)能使溴的CCl4溶液褪色。
51.写出乙酰水杨酸和NaOH溶液完全反应的化学方程式:
____________________________________________________________________。
52.由D合成E有多步,请设计出D→E的合成路线(有机物均用结构简式表示)。
(合成路线常用的表示方式为:D![]() ……
……![]() E)
E)
十、(本题共14分)
工业上用氨气与空气混合,通过“氨的催化氧化”等反应工业合成硝酸及其他产品。
53.将NH3与O2在一定条件下充分反应后全部转化为硝酸溶液,则此硝酸溶液中溶质的质量分数为_________________,若所得硝酸密度为ρg/cm3,则其物质的量浓度为 (保留两位小数)。
54.某化肥厂以氨为原料制备 NH4NO3,已知由氨制 NO 的产率是 96%,NO 制硝酸的产率是 92%,氨被硝酸的吸收率为100%,则制备80吨 NH4NO3所需氨的体积(标准状况)为 m3(保留两位小数)。
55.一定量的浓硝酸与铜反应生成NO、NO2、N2O4混合气体。测出混合气体密度是同温同压下氢气的28倍。再将气体通过足量水充分吸收后,体积变为原来的2/3(相同条件下测定)。计算混合气体中NO2的体积分数。
56.合成氨原料气由CH4在高温下与水蒸气、空气反应而得。反应原理如下:
CH4+2H2O→CO2+4H22CH4+O2+2H2O→2CO2+6H2
将反应后的混合气中CO2、H2O (g)通过吸收和干燥除去后,只含N2和H2。为使进入合成氨反应塔两者体积比为1∶3。计算起始气体中CH4和空气的比例。
(已知空气中O2和N2的体积比为1∶4)。
闵行区2014学年第二学期高三化学质量调研试卷
参考答案和评分标准
一、选择题(共10分,每题2分)
| 题号 | 1 | 2 | 3 | 4 | 5 |
| 选项 | B | C | A | D | B |
二、选择题(共36分,每题3分)
| 题号 | 6 | 7 | 8 | 9 | 10 | 11 |
| 选项 | D | C | B | D | C | C |
| 题号 | 12 | 13 | 14 | 15 | 16 | 17 |
| 选项 | A | D | B | C | A | D |
三、选择题(共20分,每题4分,只答1个且正确给2分,有错不给分)
| 题号 | 18 | 19 | 20 | 21 | 22 |
| 选项 | AC | BD | BD | C | A |
四、(共12分)
23.(2分)ac
24.(2分)bc
25.(3分)Cl>C>O;非极性;最高价氧化物对应水化物的酸性(合理即给分)
26.(3分)4;2s22p2;原子
27.(2分)5000
五、(共12分)
28.(3分)2Fe3++SO2+2H2O→2Fe2++4H++SO42- (2分) ![]() (1分)
(1分)
29.(3分)有白色沉淀生成,溶液红色褪去(1分)
亚硫酸钠溶液水解成碱性,滴入酚酞成红色。SO32-+ H2O![]() HSO3-+ OH-,加入氯化钡后,Ba2++SO32-→BaSO3↓,降低了SO32-的浓度,使得水解平衡往左移动,导致溶液中OH-浓度降低,因此溶液红色褪去(2分)
HSO3-+ OH-,加入氯化钡后,Ba2++SO32-→BaSO3↓,降低了SO32-的浓度,使得水解平衡往左移动,导致溶液中OH-浓度降低,因此溶液红色褪去(2分)
30.(3分)中;H+与OH-、SO42-与Cl-
31.(3分)H2S + CO32-→HS-+ HCO3-(2分)>(1分)
六、(共12分)
32.(2分)氧化;萃取(或萃取分液)
33.(2分)坩埚(或瓷坩埚)、泥三角
34.(2分)ba (写a b得1分)
35.(2分)从水层取少量溶液,加入1~2 mL淀粉溶液,加盐酸酸化,滴加Na2SO3溶液,若溶液变蓝,说明滤液中含有IO;若溶液不变蓝,说明滤液中不含有IO(合理即给分)
36.(4分)SO2 + I2+ 2H2O → 2HI + H2SO4;2HI![]() H2 + I2
H2 + I2
节约电能;使用能造成污染环境的SO2。
七、(共12分)
37.(2分)2Al + 2OH¯+ 2H2O →2 AlO2¯ + 3H2↑稀硝酸(或硝酸)
38.(2分)3.2≤pH<4.7 c
39.(2分)蒸发浓缩、降温结晶
40.(2分)bc
41.(2分)26(m-n)/9m,
42.(2分)滤渣C没有洗涤,混有NaHCO3,煅烧后失重偏大;滤渣C洗涤后未烘干或烘干不达标,混有微量水,煅烧后失重偏大(各1分,合理给分)
八、(本题共8分)
43.(2分)![]() ,NaOH水溶液
,NaOH水溶液
44.(2分)取样,加入新配Cu(OH)2悬浊液,加热至沸,产生砖红色沉淀,证明生成C。
或取样,加入银氨溶液,水浴加热,产生银镜,证明生成C
45.(2分)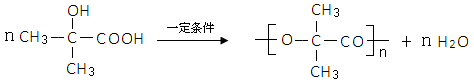
46.(2分)保护碳碳双键不被氧化
九、(本题共14分)
47.(2分)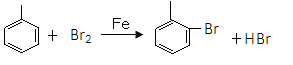
48.(4分)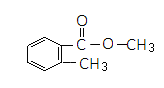 (2分)
(2分)
羧基、羟基(2分)
49.(1分)取代或酯化
50.(2分) 或
或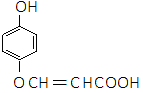 的邻、间、对的任意一种
的邻、间、对的任意一种
51.(2分)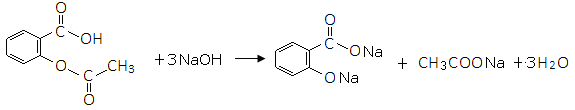
52.(3分)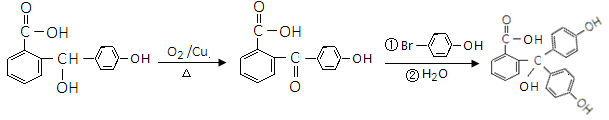 (写出D的结构简式即给1分)
(写出D的结构简式即给1分)
十、(共14分)
53.(4分)77.78%(或0.78),12.35ρmol/L
54.(2分)47435.29
解析:根据合成 NH4NO3 的反应:NH3+ HNO3→NH4NO3
合成 80 t NH4NO3 时,需要用 63 t HNO3 吸收 17 t 的 NH3。
制备 63 t HNO3 需要m(NH3)
NH3 ~ HNO3
17 63
m(NH3)×96%×92% 63 t
m(NH3)=19 t。
V(NH3)=![]() = 47435.29(m3)
= 47435.29(m3)
55.(4分)设NOx mol NO2ymol N2O4zmol
30x + 46y + 92z= 2×28(x+ y + z)
2/3(x+y+z)= x +1/3y+ 2/3z(2分)
x=y=z则φ(NO2)=1/3(或33.33%)(2分)
55.(4分)设起始气体中CH4xmol空气ymol,则N2为0.8ymol,O2为0.2ymol
CH4+2H2O→CO2+4H2①2CH4+O2+2H2O→2CO2+6H2②
反应②生成的H2为0.2ymol×6/1=1.2ymol,消耗CH40.2ymol×2/1=0.4ymol,(1分)
反应①生成的H2为(x-0.4y) mol×4/1=4(x-0.4y) mol(1分)
0.8y: [1.2y+4(x-0.4y)]=1:3 x:y=7:10 V(CH4):V(空气)=7:10(2分)