
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
乾安七中2016-2017学年度高三第一次模拟考试
化学试题
本试卷分第一部分(选择题)和第二部分(非选择题),满分100分,考试时间90分钟。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cu 64 S 32 Cl 35.5 Al 27
资*源%库第I卷(选择题共60分)
一、单选题(本大题20小题,每小题3分,共60分)
1.下列表格中各项都正确的一组是( )
| 类别选项 | 碱 | 盐 | 电解质 | 非电解质 |
| A | 资*源%库烧碱 | 小苏打 | BaSO4 | 干冰 |
| B | 纯碱 | CaCO3 | NH3•H2O | Fe |
| C | 胆矾 | 食盐 | 石墨 | 醋酸 |
| D | KOH | 资*源%库CuSO4 | Na2SO4 | KClO3 |
2.某溶液中只含有Na+、Al3+、Cl-、SO42-四种离子,已知前三种离子的个数比为3∶2∶1,则溶液中Al3+和 SO42-的离子个数比为
A.1∶2B.1∶4C.3∶4D.3∶2
3.设NA为阿伏加德罗常数,下列叙述中正确的是
A.足量铁在氯气中反应,l mol铁失去的电子数为2 NA
B.标准状况下22.4 L H2中含中子数为2 NA
C.1 L Imol/L的盐酸溶液中,所含氯化氢分子数为NA
D.常温下46 g NO2和N2O4混合气体中含有原子数为3NA
4.下列说法正确的是()
A.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口倒出
B.使用容量瓶的第一步操作是先将容量瓶用蒸馏水洗涤后烘干
C.用10 mL量筒量取9.2 mL NaCl溶液
D.检验某溶液是否含有SO时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸
5.设NA为阿伏加德罗常数的值,下列说法正确的是()
A.标准状况下,22.4 L的CCl4中含CCl4分子数为NA
B.5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等
C.0.1 mo1·L-1MgCl2溶液中含Cl-数为0.2NA
D.3.9 g Na2O2晶体中含有的离子总数为0.2NA
6.下列配制的溶液浓度偏高的是( )
A.配制盐酸用量筒量取盐酸时俯视刻度线
B.配制盐酸定容时,仰视容量瓶刻度线
C.称量4 g NaOH配制0.1 mol·L-1NaOH溶液1 000 mL时,砝码错放左盘
D.NaOH溶解后未经冷却即注入容量瓶至刻度线
7.使用容量瓶配制溶液,下列操作不正确的是()
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.盖好瓶塞,用食指顶住瓶塞,用另一只手指托住瓶底,把容量瓶倒转和摇动几次
D.容量瓶不能长期存放配制好的溶液
8.离子反应方程式H++OH—=H2O,可表示的化学反应是
A.Cu(OH)2和稀H2SO4反应B.HNO3和Mg(OH)2反应
C.Ba(OH)2溶液和HCl溶液混合D.NaOH和CH3COOH反应
9.下列物质在空气中久置会发生变质,且在变质过程中,既有氧化还原反应发生,又有非氧化还原反应发生的是
A.氢氧化钠固体 B.氯化钠固体 C.金属钠 D.生石灰
10.下列离子方程式中不正确的是( )
A.氢氧化钡溶液与硫酸混合:Ba2++2OH﹣+2H++SO42﹣═BaSO4↓+2H2O
B.铁粉与硝酸银溶液反应:Fe + 2Ag+ == Fe2+ + 2Ag
C.氯化铝溶液与过量的氨水反应:Al3++4NH3•H2O═AlO2﹣+4NH4++2H2O
D.氯气通入冷的氢氧化钠溶液中:Cl2+2OH﹣═Cl﹣+ClO﹣+H2O
11.下列各组离子中的离子,能在溶液中大量共存的是( )
A.Na+、Mg2+、Cl-、OH-B.H+、Ca2+、CO32-、NO3-
C.Cu2+、K+、SO42-、NO3-D.Na+、H+、OH-、Ca2+
12.下列说法正确的是
A.氧化还原反应一定有氧元素参加 B.失电子难的原子其得电子的能力一定强
C.金属单质只具有还原性 D.失电子越多,该物质的还原性就越强
13.反应:Al2O3+N2+3C![]() 2AlN+3CO,下列有关该反应叙述正确的是()
2AlN+3CO,下列有关该反应叙述正确的是()
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.AlN的摩尔质量为41 g
C.AlN中氮元素的化合价为+3
D.上述反应中,每生成1 mol AlN需转移3 mol电子
14.体积比为1 : 2 : 3所组成的N2、O2和CO2混合气体100 g在标准状况下体积为
A.60 L B.30 L C.11.2 L D.112 L
15.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.pH=1的溶液中:Na+、K+、MnO、CO
B.c(H+)=1×10-13mol·L-1的溶液中:Mg2+、Cu2+、SO、NO
C.0.1 mol·L-1NH4HCO3溶液中:K+、Na+、NO、Cl-
D.0.1 mol·L-1FeCl3溶液中:Fe2+、NH、SCN-、SO
16.24mL浓度为0.05mol/L的Na2SO3溶液恰好与20mL浓度为0.02 mol/L的K2Cr2O7溶液完全反应;已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
A、+2 B、+3 C、+4D、+5
17.将含有0.1 mol氯化铁的饱和溶液逐滴加入到沸水中,并继续加热至溶液呈红棕色,下列说法不正确的是 ( )
A.所得红棕色液体为氢氧化铁胶体
B.向该液体中逐滴加盐酸,开始时产生沉淀,盐酸足量时,沉淀消失
C.该液体含分散质微粒0.1 mol
D.该液体具有丁达尔现象
18.实验室里需要配制480 mL 0.10 mol·L-1的硫酸铜溶液,下列实验用品及实验操作都正确的是( )
| 选项 | 容量瓶容积 | 固体质量 | 实验操作 |
| A | 480 mL | 硫酸铜:7.68 g | 加入500 mL水 |
| B | 480 mL | 胆矾:12.0 g | 配成500 mL溶液 |
| C | 500 mL | 硫酸铜:8.0 g | 加入500 mL水 |
| D | 500 mL | 胆矾:12.5 g | 配成500 mL溶液 |
19.制备(NH4)2Fe(SO4)2·6H2O的实验中,需对过滤出产品的母液(pH<1)进行处理。常温下,分别取母液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是()
A.通入过量Cl2:Fe2+、H+、NH、Cl-、SO
B.加入少量NaClO溶液:NH、Fe2+、H+、SO、ClO-
C.加入过量NaOH溶液:Na+、Fe2+、NH、SO、OH-
D.加入过量NaClO和NaOH的混合溶液:Na+、SO、Cl-、ClO-、OH-
20.甲、乙、丙、丁是由H+、Na+、Al3+、Ba2+、OH-、Cl-、HCO离子中的两种组成,可以发生如图转化,下列说法不正确的是()
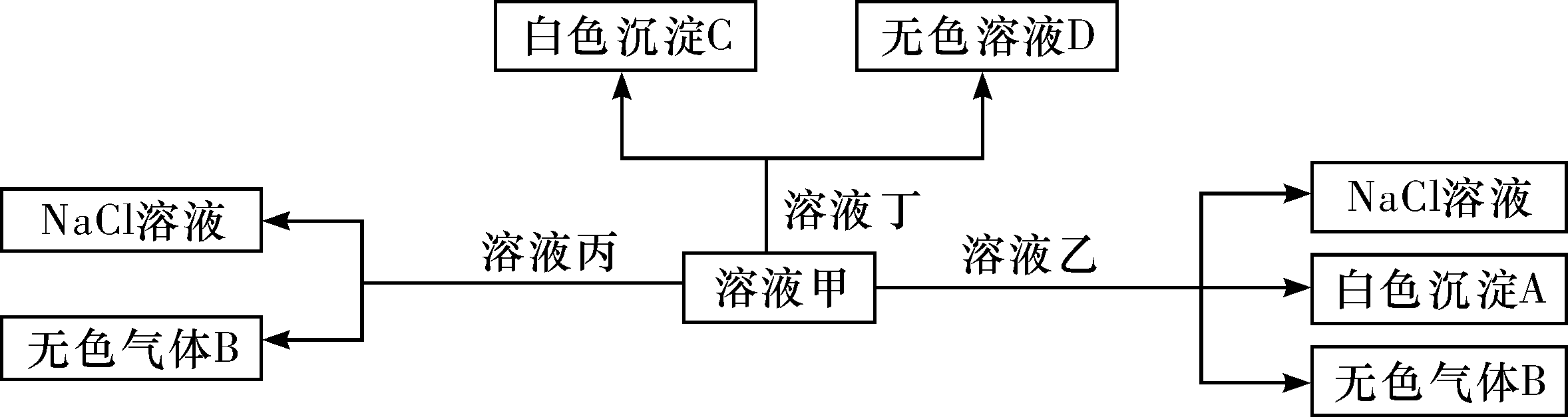
A.在甲中滴加丁可能发生反应:HCO+Ba2++OH-===BaCO3↓+H2O
B.溶液丙中还可以大量共存的离子有:I-、NO、SO
C.白色沉淀A可能溶解在溶液D中
D.甲为NaHCO3,乙为 AlCl3
第II卷(非选择题)
二、填空题(40分)
21、(9分)(1)已知下列反应:①HPO3+H2O===H3PO4;②2Na2O2+2H2O===4NaOH+O2↑;
③2F2+2H2O===4HF+O2;④2K+2H2O===2KOH+H2↑;
⑤Cl2+H2O![]() HCl+HClO;⑥2H2O2H2↑+O2↑。
HCl+HClO;⑥2H2O2H2↑+O2↑。
其中,H2O只作氧化剂的是_____;H2O只作还原剂的是_____;H2O既作氧化剂,又作还原剂的是____;H2O既不是氧化剂,又不是还原剂的是_____,其中不属于氧化还原反应的是______。
(2)根据反应8NH3+3Cl2===6NH4Cl+N2,回答下列问题:
①氧化剂是________,还原剂是__________。
②氧化剂与还原剂的分子个数比为________。
③当有68 g NH3参加反应时,被氧化的物质为____________ g。
22.(12分)关于溶液配制的有关问题,请回答:
(1)下列有关容量瓶的使用方法的操作中,错误的是_________。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.定容时,将蒸馏水小心倒入容量瓶中到刻度线齐平处
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中定容
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复上下颠倒、摇匀。
(2)实验室中需2mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是______________。
A.1000mL; 212g B.950mL;543.4g
C.任意规格; 572g D.500mL; 106g
(3)现用98%、密度为1.8g/mL的浓硫酸配制500mL的稀硫酸。请回答下列问题:
①配制稀硫酸时,需要的玻璃仪器有玻璃棒、烧杯、量筒,还缺少的玻璃仪器有_______(填写仪器名称)。
资*源%库②经计算,配制500mL0.2mol/L的稀硫酸需要上述浓硫酸的体积为___________。
③稀浓硫酸时,实验操作步骤:____________________。
(4)误差分析:
①用量筒量取浓硫酸时仰视读数,导致最终结果____________;(填“偏大”“偏小”或“不变”)
②定容时仰视读数,导致最终结果_________________;(填“偏大”“偏小”或“不变”
23.(12分)要准确掌握化学基本概念和研究方法。按要求回答下列问题:
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| 第一组 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
| 第二组 | NaOH | HCl | NaCl | Na2O | CO |
| 第三组 | NaOH | CH3COOH | CaF2 | Al2O3 | SO2 |
| 物质 | M | N | Q | P |
| 反应前质量(g) | 50 | 1 | 3 | 12 |
| 反应后质量(g) | X | 26 | 3 | 30 |
①该变化的基本反应类型是________反应;
②物质Q在反应中起的作用是________。
24.(7分)有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
| 阳离子 | K+Na+Cu2+Al3+ |
| 阴离子 | SO42﹣HCO3﹣NO3﹣OH﹣ |
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出B、D的化学式:B,D.
(2)将含1mol A的溶液与含1mol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为.
(3)在A溶液中加少入量澄清石灰水,其离子方程式为.
(4)C常用作净水剂,用离子方程式表示其净水原理.
第一次模拟考试化学答案
一、选择题:
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| A | A | D | C | B | D | B | C | C | C | C | C | D | A | C | B | C | D | D | B |
二、非选择题
21、(1)④ ; ③ ; ⑥ ; ①②⑤ ; ① 。
(2)① Cl2;NH3 ② 3:2 ③ 17
22、(1)BCD (2)A
(3) ①胶头滴管、500ml容量瓶 ②5.6 ml
③ 把浓硫酸缓缓注入水中,同时用玻璃棒不断搅拌
(4) ① 偏大 ② 偏小
23、(1)Na2CO3、CO、Al2O3
(2)分散质粒子直径大小不同;丁达尔现象。
(3)① 16 ② 22.4 ③ 1
(4)① 分解反应 ② 催化剂
24、
(1)KNO3 ;CuSO4
(2)Na2CO3
(3) 2HCO3- + Ca2+ + 2OH- == CaCO3↓+2H2O + CO32-
(4)Al3+ + 3H2O![]() Al(OH)3 + 3H+
Al(OH)3 + 3H+