
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
四川省阆中市2016届高三第五次模拟练习
化学试题
第I卷(选择题)
一、单选题
1.中国科学技术名词审定委员会已确定第116号元素Lv的名称为![]() 。关于Lv的叙述错误的是
。关于Lv的叙述错误的是
A.原子序数 116B.中子数 177C.核外电子数 116D.相对原子质量 293
2.用你所学的有机化学知识判断,下列表述中正确的是
A.汽油是纯净物,乙醇汽油是混合物
B.苯、乙烯、乙酸和乙酸乙酯都能发生加成反应
C.石油的分馏和煤的干馏都发生了化学变化
D.除去乙酸乙酯中少量的乙酸,用饱和碳酸钠溶液洗涤后分液
3.已知反应mX(g)+nY(g)![]() qZ(g) ΔH<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
qZ(g) ΔH<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
A.通入稀有气体使压强增大,平衡将正向移动
B.X的正反应速率是Y 的逆反应速率的m/n倍
C.降低温度,混合气体的平均相对分子质量变小
D.增加X的物质的量,平衡常数增大
4.下列离子方程式书写正确的是
A.铜与浓硫酸反应放出SO2:Cu + 4H++ ![]() Cu2++SO2↑+2H2O
Cu2++SO2↑+2H2O
B.加热NH4Cl和氢氧化钠固体混合物: + OH-![]() NH3↑ + H2O
NH3↑ + H2O
C.稀硝酸与过量的铁屑反应:Fe + 4H+ + ![]() Fe3+ + NO↑ + 2H2O
Fe3+ + NO↑ + 2H2O
D.氯气通入FeCl2溶液中:Cl2 + 2Fe2+![]() 2Fe3+ + 2Cl-
2Fe3+ + 2Cl-
5.下列说法正确的是
A.凡是分子组成相差一个或若干个CH2原子团的物质,彼此一定是同系物
B.两种化合物组成元素相同,各元素的质量分数也相同,则二者一定是同分异构体
C.相对分子质量相同的几种化合物互为同分异构体
D.组成元素及其质量分数相同,且相对分子质量也相同的不同化合物,互为同分异构体
6.下列有关化学反应中能量变化的说法正确的是
A.已知:2C2H2(g)+5O2(g)![]() 4CO2(g)+2H2O(l) ΔH=-2 596.6 kJ·mol-1,则2 mol C2H2(g)完全燃烧生成气态水时放出的热量大于2 596.6 kJ
4CO2(g)+2H2O(l) ΔH=-2 596.6 kJ·mol-1,则2 mol C2H2(g)完全燃烧生成气态水时放出的热量大于2 596.6 kJ
B.1 g氢气燃烧生成液态水时放出142.9 kJ热量,则表示氢气燃烧热的热化学方程式为2H2(g)+O2(g)![]() 2H2O(l) ΔH =-142.9 kJ·mol-1
2H2O(l) ΔH =-142.9 kJ·mol-1
C.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,则其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
D.已知:①C(s,石墨)+O2(g)![]() CO2(g) ΔH=-393.5 kJ·mol-1;②C(s,金刚石)+O2(g)
CO2(g) ΔH=-393.5 kJ·mol-1;②C(s,金刚石)+O2(g)![]() CO2(g)ΔH=-395.0 kJ·mol-1。则C(s,金刚石)
CO2(g)ΔH=-395.0 kJ·mol-1。则C(s,金刚石)![]() C(s,石墨) ΔH=-1.5 kJ·mol-1
C(s,石墨) ΔH=-1.5 kJ·mol-1
7.下列无色溶液中,各组离子能大量共存的是
A.Ca2+、H+、HC、Cl-B.Ba2+、K+、OH-、N
C.Cu2+、Na+、Mn、SD.Fe3+、Al3+、SCN-、HC
第II卷(非选择题)
二、实验题
8.某研究性学习小组为测定某含镁3%~5%的铝镁合金(不含其他元素)中镁的质量分数,设计了下列三种不同实验方案进行探究,请根据他们的设计回答有关问题。
【探究一】实验方案:铝镁合金![]() 测定剩余固体质量。问题讨论:
测定剩余固体质量。问题讨论:
【探究二】实验方案:称量x g铝镁合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧。
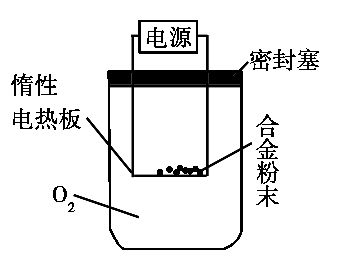
问题讨论: (4)欲计算Mg的质量分数,该实验中还需测定的数据是 。
(5)假设实验中测出该数据为y g,则原铝镁合金粉末中镁的质量分数为 (用含x、y的代数式表示)。
【探究三】实验方案:铝镁合金![]() 测定生成气体的体积。
测定生成气体的体积。
问题讨论:
(6)同学们拟选用下边的实验装置完成实验,你认为最简易的装置的连接顺序是a接 。(填接口字母,仪器不一定全选)
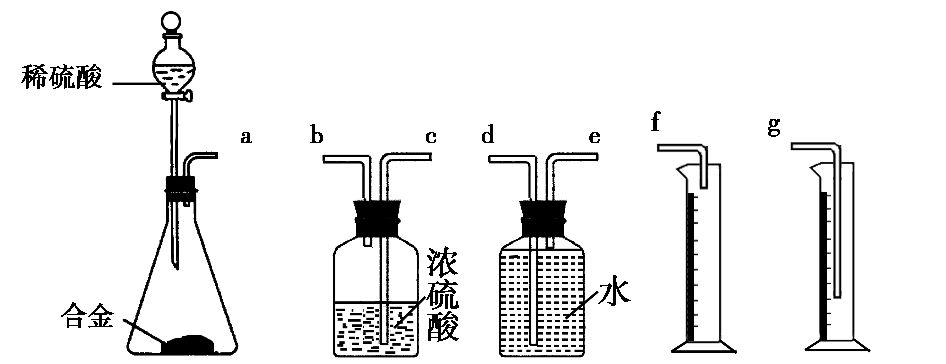
(7)同学们仔细分析(6)中连接的实验装置后,又设计了下图所示的实验装置。
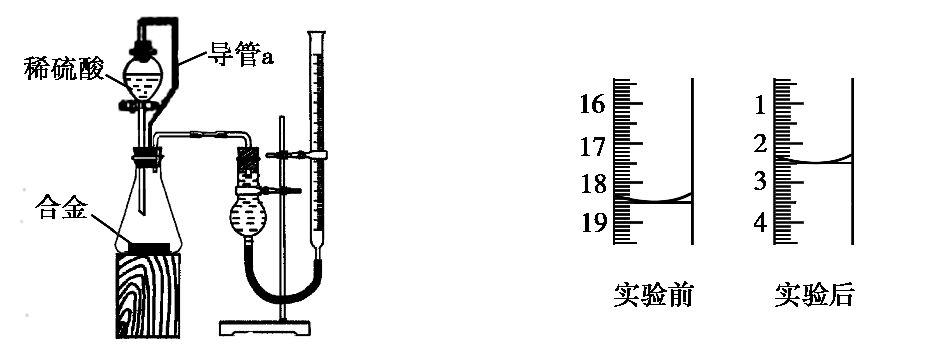
①装置中导管a的作用是 。
②实验前后碱式滴定管中液面读数分别如上右图,则产生氢气的体积为 mL。
资*源%库 ③与上左图装置相比,用(6)中连接的装置进行实验时,容易引起误差的原因是 (任写一点)。
三、综合题
9.硫酸亚锡(SnSO4)可用于镀锡工业。某小组设计的SnSO4制备路线如下:
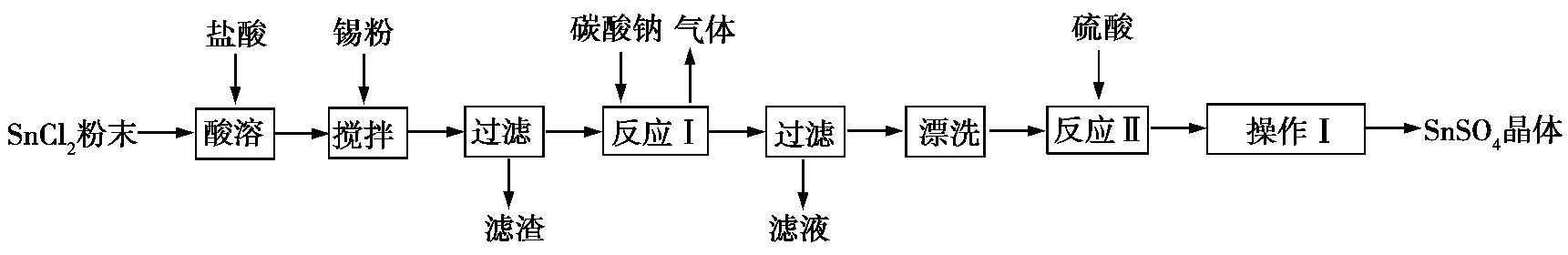
已知:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡。
(7)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于过量的盐酸中,发生的反应为Sn+2HCl![]() SnCl2+H2↑;
SnCl2+H2↑;
②加入过量的FeCl3溶液;
③用已知浓度的K2Cr2O7溶液滴定②中生成的Fe2+,再计算锡粉的纯度。
请配平方程式:
![]()
10.金刚石、SiC具有优良的耐磨、耐腐蚀特性,应用广泛。
②Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
③钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比均为1∶2
④水晶、干冰熔化时克服粒子间作用力的类型相同
11.J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
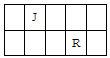 M的离子结构示意图为 ;元素T在周期表中位于第 族。
M的离子结构示意图为 ;元素T在周期表中位于第 族。
四、填空题
12.在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g) ΔH,随温度升高,混合气体的颜色变深。
2NO2(g) ΔH,随温度升高,混合气体的颜色变深。
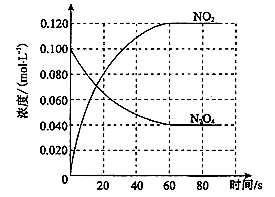
回答下列问题:


ΔH=-215 kJ·mol-1
12.(1)> 0.0020或2.0×10-3 0.36或0.36mol·L-1
(2)大于
(3)深;
原因是N2O4(无色)![]() 2NO2(红棕色) ΔH>0,是吸热反应,而双氧水的分解反应是放热反应。当右边双氧水分解时,放出的热量会使B瓶升温,从而使瓶中反应朝正反应方向移动,即向生成NO2移动,故B瓶颜色更深。
2NO2(红棕色) ΔH>0,是吸热反应,而双氧水的分解反应是放热反应。当右边双氧水分解时,放出的热量会使B瓶升温,从而使瓶中反应朝正反应方向移动,即向生成NO2移动,故B瓶颜色更深。