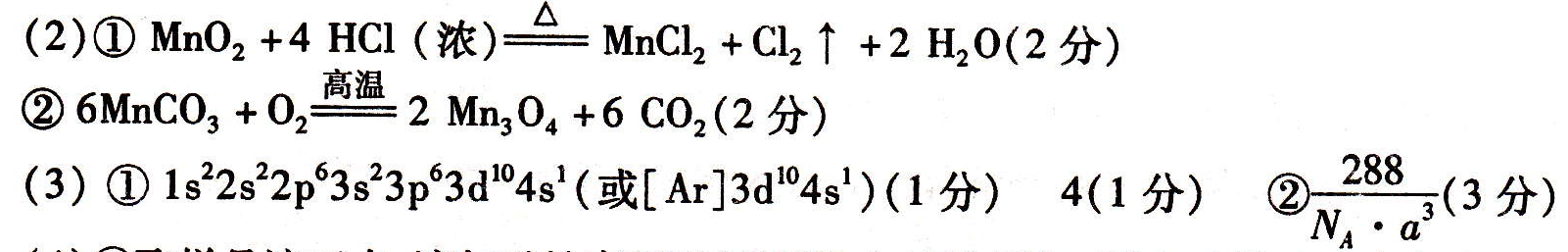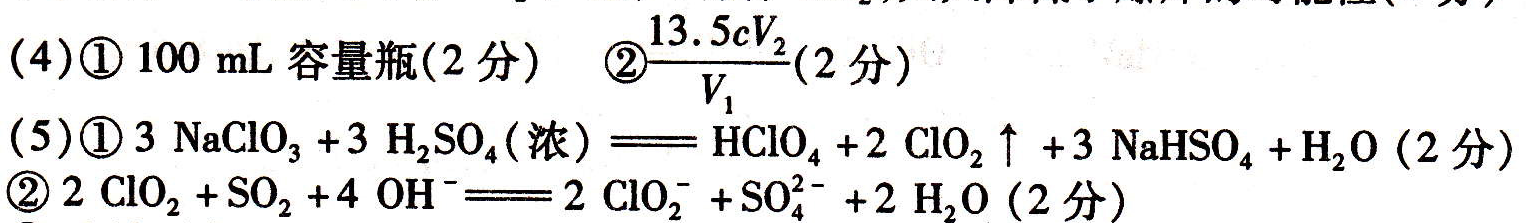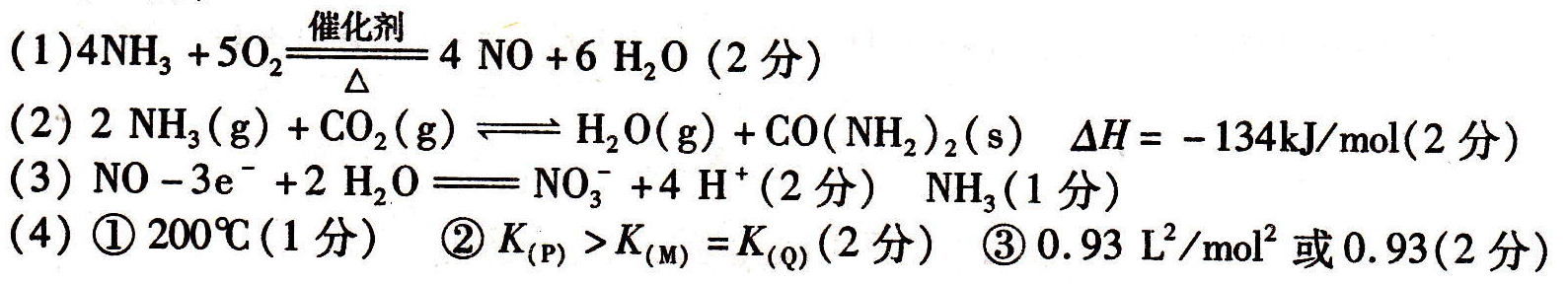湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
内江市高中2016届第四次模拟考试题
化 学
第I卷(选择题共42分)
可能用到的相对原子质量:0-16 S1-28 Cl-35.5 Cu-64
一、选择题(本大题包括7小题,每小题6分,共42分o在每小题给出的四个选项中,只有
一个选项符合题目要求)。
1.化学与社会、生产、生活密切相关。下列说法正确的是
A.为延长食品保质期,可向其中大量添加苯甲酸钠等防腐剂
B.催化转化机动车尾气为无害气体,能消除酸雨和雾霾的发生
C.PM2.5是指空气中氮氧化物和硫氧化物含量之和
D.“地沟油”可以制成肥皂,从而提高资源的利用率
2.下列有关NaHS03溶液的叙述正确的是
A.该溶液中,K+、Ca2+、Cl2、Br-可以大量共存
B.与足量Ca( OH)2溶液反应的离子方程式:Ca2++OH-+ HS03一CaS03J,+H20
C.与FeCI3溶液反应的离子方程式:SO32-+2 Fe3++H20=SO42-+2Fe2++2H+
D.能使含I2的淀粉溶液蓝色褪去,说明NaHSO3溶液具有漂白性
3.设NA为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,22.4 L HF中含HF分子数目为NA
B.60 g石英晶体中含有的Si-O键数目为2 NA
C.标准状况下,11.2 L Cl2通人足量的石灰乳中制备漂白粉,转移的电子数为0.5 NA
D.l L 0.1 mol/L的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1 NA
 4.右图是邵分短周期元素的原子序数与其某种常见
4.右图是邵分短周期元素的原子序数与其某种常见
化合价的关系图,若用原子序数代表所对应的元素,则下
列说法正确的是
A.31d和33d属于同种核素
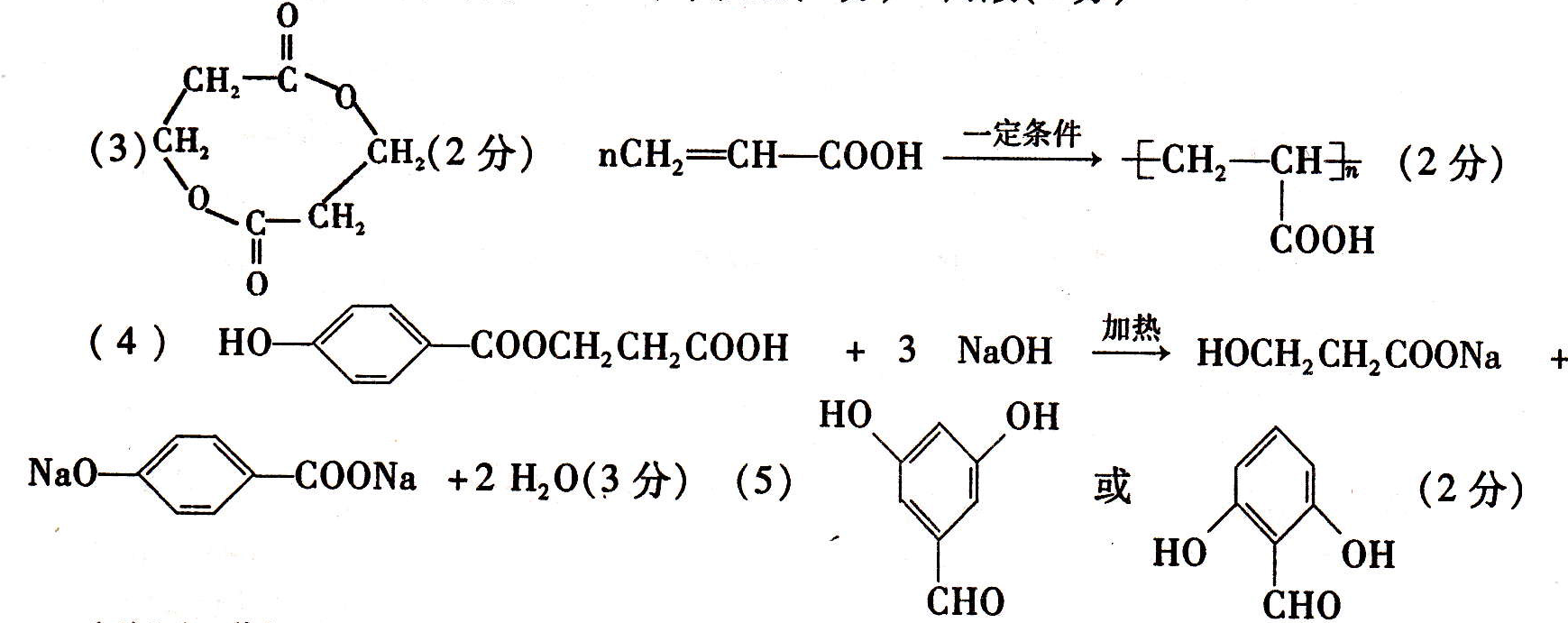
B.第一电离能d>e,电负性d C.气态氢化物的稳定性:a>d>e D.a和b形成的化合物不可能含共价键 5.用无机矿物资源生产部分材料,其生产流程如下图。下列有关说法不正确的是 B.生产过程中均涉及氧化还原反应 C.石英可用于制光导纤维,晶体Si常用 做半导体材料 D.黄铜矿冶炼铜时产生的SO2可用于生 产硫酸,FeO可用于冶炼铁 6.下列实验中,对应的现象以及解释或结论都正确且两者具有因果关系的是 7.常温下,用0.1 mol/LNaOH溶液滴定10 mL 0.1 mol/LH2A溶液,溶液的pH与 A.A点溶液中加入少量水: B.B点:c( HA -)>c(H+)>c(A2一)>c(H2A) C.C点:c(Na+) =c(HA-)+2c( A2-) D.水电离出来的c(OH-):B点>D点 第Ⅱ卷(非选择题共58分) 二、筒答题(共58分) 8.(16分)Fe、Cu、Mn三种元素的单质及化合物在生产、生活中有广泛应用。 (l) MnO2是一种多功能材料,工业上常以Mn(NO3)2.6H2O和尿素[CO(NH2)2]、氧化 剂等为原料制备。尿素分子中碳原子的杂化轨道类型为 ,l mol尿素分子中含有的 σ键数为____。 (2)某学习小组拟以废旧于电池为原料制取锰,简易流程如下: ①用浓盐酸溶解二氧化锰需保持通风,原因是 ____(用化学方程式表示)。 ②写出碳酸锰在空气中灼烧生成四氧化三锰的化学方程式____。 (3)①基态铜原子的电子排布式为____,与Cu同周期且原子序数最小的第Ⅷ族 ②右图是Cu20的晶胞结构,晶胞的边长为acm。则Cu2O的密度 为 g/cm3(用NA表示阿伏加德罗常数的值)。 (4)①绿矾(FeS04.7H2O)是补血剂的原料,保存不当易变质。请设 计实验检验绿矾是否完全变质 。 如右图。已知:Fe(s) +5 CO(g) 压下,Fe( CO)s的熔点约为- 20.3℃,沸点为103. 6℃,则 Fe( CO),的晶体类型为 。请用平衡移动原理解释 Ti 9.(14分)ClO2是一种高效水处理剂,某实验小组用下图所示装置制取并收集Cl02。’ 已知:①ClO2为黄绿色气体,极易溶于水,熔点- 59C,沸点11℃,具有强氧化性。 ②ClO2易爆炸,若用“惰性气体”等稀释时,爆炸的可能性大大降低。 ③装置A中发生反应:H2C2O4+H2SO4+2 KC1O3一K2SO4+2 CO2T+2ClO2+2H2O 的工艺流程如右图: ①反应器I中发生反应的化 学方程式为________。 ②反应器Ⅱ中发生反应的离 子方程式为 。 ③在碱性溶液中NaCl02比较稳定,所以反应器Ⅱ中应维持NaOH稍过量,判断NaOH 是否过量的简单实验方法是 。 10.(16分)有机物A的分子式为C10H10O5,能发生如下变化。 NaHC03反应;②只有A .D能与 FeCl3溶液发生显色反应;③A苯 环上只有两个对位的取代基;④F 能使溴水褪色;⑤H能发生银镜反 应。根据题意回答下列问题: 数为400,此温度下,在2L的密闭容器中加入xmol C,反应到某时刻测得各组分的浓度如下: 下列说法正确的是____ 。 a.x= 1.64 b.此时刻正反应速率大于逆反应速率 c.保持温度不变,若起始时加入2x mol C,则达到平衡时C的转化率增大 d.若混合气体的平均摩尔质量不再变化,则说明反应已达到平衡状态 所示: 当反应器中按n(N2):n(H2)=l:3投料,分别在 200C、400℃、600C下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如下图。 ②上图中P、M、Q三点对应的平衡常 数K的大关系为__ ③若N点时c(NH3)=0.2 mol.L-l, 则K(N)=(保留两位有效数字)。 内江市高中2016届第四次模拟考试题 化学参考答案及评分意见 一、选择题(本大题包括7小题,每小题6分,共42分)。 1.D 2.B 3.C 4.B 5.A 6.C 7,D 二、简答题(共58分) 8.(16分) (4)①取样品溶于水,滴加酸性高锰酸钾溶液,如溶液褪色,则表示样品没有完全变质(或 滴加铁氰化钾溶液,产生蓝色沉淀,则样品没有完全变质)(2分) ②分子晶体(1分) 铁粉和一氧化碳化合成羰基合铁时放出热量,低温有利于合成易挥 发的羰基合铁,羰基合铁易挥发,杂质残留在玻璃管左端;当羰基合铁挥发到高温区T2时,即 升温平衡逆向移动,羰基合铁分解,纯铁粉残留在右端,故T1 9.(14分) ③连续测定反应器Ⅱ内溶液的pH(2分) 10.(16分) (6)b(2分) 11.(12分)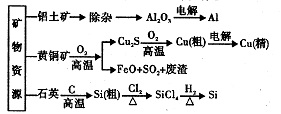 A.Al2O3、SiCl4均为共价化合物
A.Al2O3、SiCl4均为共价化合物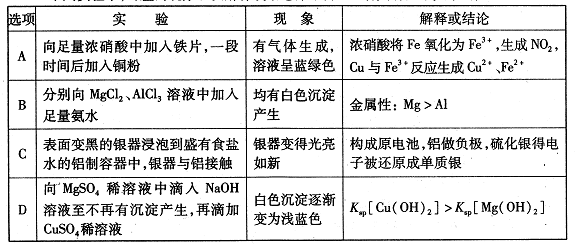
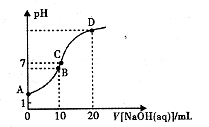 NaOH溶液的体积关系如图所示。下列说法不正确的是
NaOH溶液的体积关系如图所示。下列说法不正确的是![]() 增大
增大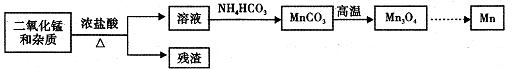
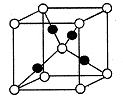 元素,其基态原子核外有 个未成对电子。
元素,其基态原子核外有 个未成对电子。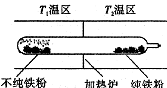 ②以羰基化合物为载体,提纯某纳米级活性铁粉(含有一些不反应的杂质),反应装置
②以羰基化合物为载体,提纯某纳米级活性铁粉(含有一些不反应的杂质),反应装置![]() 'Fe(CO)5(9) △H <0,常
'Fe(CO)5(9) △H <0,常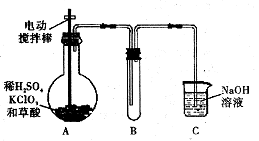 ④HCl02是强酸。
④HCl02是强酸。
最大优点是________。
收得到ClO2溶液。为测定所得溶液中Cl02的含
量,进行下列实验:
步骤1:准确量取V1mL ClO2溶液加入到锥形瓶中。,
步骤2:用稀硫酸调节Cl02溶液的pH ≤2.0,加入足量的KI晶体,静置片刻。
步骤3:加入指示剂,用c mol.L-1 Na2S2O3溶液滴定至终点,消耗Na2S203溶液V2mL。
(已知2 ClO2 +8 H++10I-=2Cl- +5 I2 +4 H2O,2 S2O32-+I2=2I一+S4O62-)
①配制100 mL cmol - L-lNa2S203标准溶液时,用到的玻璃仪器有烧杯、量筒、玻璃
棒、胶头滴管和 。
②原溶液中ClO2的含量为__ g/ L(用含字母的代数式表示)。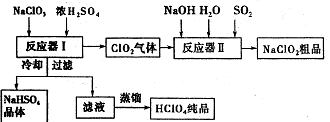 工业上生产ClO2和NaCIO2
工业上生产ClO2和NaCIO2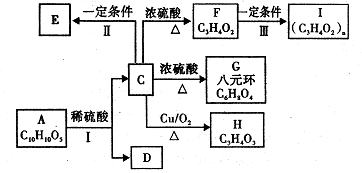 已知:①A、C、D均能与
已知:①A、C、D均能与
①能与FeCl3溶液发生显色反应 ②能发生银镜反应但不能水解
③苯环上的一卤代物只有2种![]() E(g) +H20(g),某温度下该反应的平衡常
E(g) +H20(g),某温度下该反应的平衡常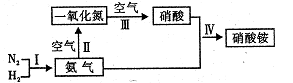 11.(12分)工业生产硝酸铵的流程如右图
11.(12分)工业生产硝酸铵的流程如右图
应,其化学方程式为____。
第一步:![]()
第二步:![]()
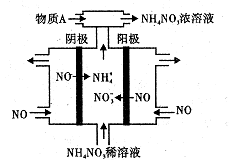 写出工业上以NH3、C02为原料合成尿素的热化学方程
写出工业上以NH3、C02为原料合成尿素的热化学方程
式 。
图所示,电解时阳极的电极反应式为
,为使电解产物全部转化为NH4N03,
需补充物质A,A是 。![]() 2 NH3(g) △H<0,
2 NH3(g) △H<0,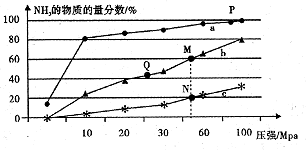 ①曲线a对应的温度是____。
①曲线a对应的温度是____。