
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
皖江区域示范高中2016届高三摸底联考
化 学 学 科 试 题
(本卷满分100分,限时100分钟)
命题人:曹飞(和县二中) 审核人:周国贺(和县二中)
可能用到的相对原子质量:H-1 N-14 O-16 Cl-35.5
第I卷选择题
(第I卷包括14小题,每小题3分,共42分。每小题只有一个选项符合题意)
1.“保护环境”是我国的基本国策。下列做法不应该提倡的是
A.采取低碳、节俭的生活方式 B.按照规定对生活废弃物进行分类放置
C.在田间焚烧大量秸秆 D.深入农村和社区宣传环保知识
2.水溶液中能大量共存的一组离子是
A.NH4+、Ba2+、Br-、CO32-B.K+、Na+、SO42-、MnO4-
C.Na+、H+、NO3-、HCO3- D. Cl-、NO3-、Fe2+、H+
3.设NA为阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,2.24 L己烷含有分子的数目为0.1NA
B.25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA
C.Na2O2与足量H2O反应产生0.1molO2,转移电子的数目为0.2NA
D.1mol甲醇中含有C—H键的数目为4NA
4.二氧化硫能使品红褪色,说明二氧化硫具有
A.还原性B.氧化性C.酸性D.漂白性
5.下列化学反应的离子方程式正确的是
A.氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
B.明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+
C.用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
D.NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O
6.已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示。下列说法正确的是
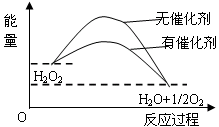 加入催化剂,减小了反应的热效应
加入催化剂,减小了反应的热效应7.下列比较不正确的是
A.氢化物热稳定性:H2S>HCl B.酸性:H2SO4>H3PO4
C.碱性:NaOH>Mg(OH)2D.离子半径:O2->Na+
8.高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理为
2Fe(OH)3 + 3KClO + 4KOH = 2K2FeO4 + 3KCl + 5H2O,下列说法正确的是
A.ClO−做还原剂 B.制备1molK2FeO4时转移3 mol 电子
C.高铁酸钾中铁的化合价为+7 D.Fe(OH)3在反应中被还原,发生还原反应
![]() 9.下列有关化学用语表达正确的是
9.下列有关化学用语表达正确的是
A.HCl的电子式:![]() B.氯离子(Cl-)的结构示意图:
B.氯离子(Cl-)的结构示意图:
C.乙酸的结构简式:C2H4O2D.质子数为17、中子数为20的氯原子:![]()
10.下列关于有机化合物的说法正确的是
A.聚乙烯分子中含碳碳双键B.油脂的皂化反应属于加成反应
C.丁烷有3种同分异构体D.以淀粉为原料可以制备乙醇
11.下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A. | 向AgCl悬浊液中加入稀的NaI溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B. | 在某溶液中加KSCN | 溶液显红色 | 该溶液中有Fe3+,无Fe2+ |
| C. | 在酒精灯上加热铝箔 | 铝箔熔化滴落下来 | 金属铝的熔点较低 |
| D. | 将气体通入澄清石灰水 | 溶液变浑浊 | 该气体一定是CO2 |
12.下列装置能达到实验目的的是
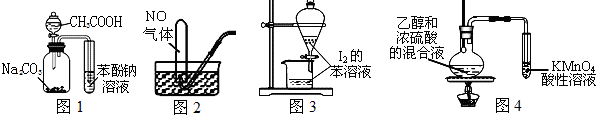
A.图1证明酸性:CH3COOH>H2CO3>苯酚 B.图2用排水法收集NO
C.图3萃取碘水中I2,分出水层后的操作 D.图4验证乙烯的生成
13.下图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录,在卡片上,描述合理的是
实验后的记录: ①Cu为负极,发生氧化反应。 ②H+向负极移动。 ③Cu电极上有气泡产生。 ④电子流动方向是Zn→导线→Cu。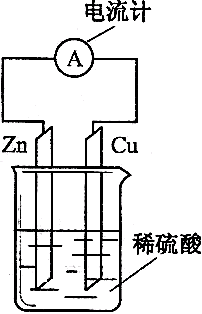
A.①③ B.①④ C.②③ D.③④
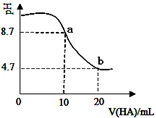 14.室温下向10mL0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。
14.室温下向10mL0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。
下列说法正确的是
A.HA为强酸
B.a、b两点所示溶液中水的电离程度相同
C.b点所示溶液中c(A—)>c(HA)
D.pH=7时,c(Na+)=c(A—)+ c(HA)
第II卷 非选择题
(第II卷包括4小题,共58分)
15.(14分)甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂
的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
回答下列问题:
(1)已知△H1=-99kJ·mol-1,△H3=+41kJ·mol-1,则△H2= kJ·mol-1。
(2)反应①的化学平衡常数K的表达式为 ;图1中能正确反映平衡常数K随温度变化关系的曲线为 (填曲线标记字母),其判断理由是 。
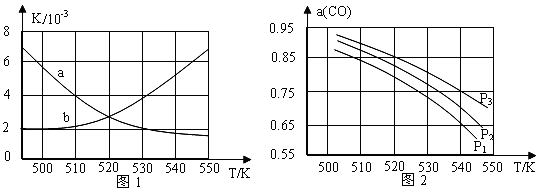
(3)若开始各气体的物质的量一定时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。则α(CO)值随温度升高而 (填“增大”或“减小”);图2中的压强由大到小为 ,其判断理由是 。
16.(14分)硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为Mg2B2O5·H2O,还有少量Fe2O3、FeO、
CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:
已知:Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、4.9、9.7和 12.4。
回答下列问题:
(1)为提高“浸出”速率,除适当增加硫酸浓度外,还可采取的措施有 。
(2)实验室中过滤操作所需要的玻璃仪器有:玻璃棒、 。
(3)“浸渣”中的物质是 (化学式)。
(4)“净化除杂”需先加H2O2溶液,作用是 ,
然后再调节溶液的pH约为5,目的是 。
(5)“粗硼酸”中的主要杂质是 (填名称)。
(6)单质硼可用于生产具有优良抗冲击性能的硼钢。以硼酸和金属镁为原料在加热条件下可制备单质硼,
用化学方程式表示制备过程 。
17.(12分)化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:
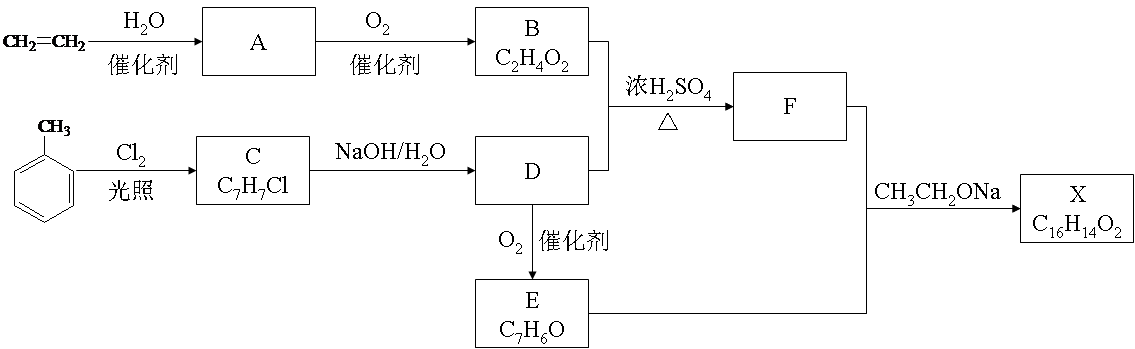
![]() 已知:RCHO+CH3COOR’ RCH=CHCOOR’ 请回答:
已知:RCHO+CH3COOR’ RCH=CHCOOR’ 请回答:
(1)A中官能团的名称是 ;C→D的反应类型为 。
(2)B+D→F的化学方程式 。
(3)E的结构简式 。
(4)对于化合物X,下列说法正确的是 。
A.能发生水解反应 B.能发生银镜反应 C.不与浓硝酸发生取代反应 D.能使Br2的CCl4溶液褪色
(5)F有多种同分异构体,含有酯基和一取代苯结构的同分异构体有五个,其中四个的结构简式是
![]()
请写出另外一个同分异构体的结构简式 。
18.(18分)NH3及其盐都是重要的化工原料。
(1)用NH4Cl和Ca(OH)2制备NH3的化学方程式为 ;
该反应发生、气体收集和尾气处理装置依次为 。
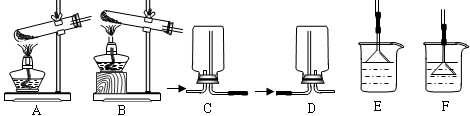
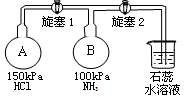 (2)按下图装置进行NH3性质实验。
(2)按下图装置进行NH3性质实验。
先打开旋塞1,B瓶中的现象是 ,
稳定后,关闭旋塞1。再打开旋塞2,B瓶中的现象是 。
。
(3)写出NH4Cl溶液水解的离子方程式 。
设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响。
限选试剂与仪器:固体NH4Cl、蒸馏水、250mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可调控温度)
①实验目的:探究 对溶液中NH4Cl水解程度的影响。
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中“V(溶液)”表示所配制溶液的体积)。
| 物理量 实验序号 | V(溶液)/mL | NH4Cl质量/g | 温度/℃ | …… | |
| 1 | 250 | X | …… | ||
| 2 | 250 | …… |
③按实验序号1所拟数据进行实验,若读取的待测物理量的数值为X,则NH4Cl水解反应的平衡转化率为
(只列出算式,忽略水自身电离的影响)。
皖江区域示范高中2016届高三摸底联考
化学学科参考答案
选择题(每空3分,共42分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| 答案 | C | B | C | D | D | C | A | B | B | D | A | B | D | C |
(1)-58
(2)![]() ; a; 反应①为放热反应,温度升高,平衡左移,平衡常数变小;
; a; 反应①为放热反应,温度升高,平衡左移,平衡常数变小;
(3)减小; P3>P2>P1;
反应①为气体分子数减小的反应,加压,平衡右移,CO的转化率增大;而反应③为气体分子数不变的反应,加压,平衡不移动,CO的转化率不变,故增大压强,CO的转化率增大。
16.(每空2分,共14分)
(1) 提高反应温度(其它答案合理也给分)
(2) 烧杯和漏斗 (3) SiO2和CaSO4
(4) 将Fe2+氧化成Fe3+; 使Fe3+与Al3+形成氢氧化物沉淀而除去。
(5)(七水)硫酸镁
(6) 2H3BO3+3Mg 3MgO+2B+3H2O(或2H3BO3B2O3+3H2O,B2O3+3Mg 2B+3MgO )
17.(每空2分,共12分)
(1) 羟基; 取代反应(或水解反应)
(2)![]()
![]() (3) (4)AD (5)
(3) (4)AD (5)![]()
18.(18分)
(1)2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O;(2分) BDE(3分)
(2)产生白色的烟(2分)
烧杯中的石蕊溶液会倒吸入B瓶,且溶液变为红色。(2分)
(3)NH4+ + H2O![]() NH3·H2O + H+(2分)
NH3·H2O + H+(2分)
① 温度(2分)
②(每空0.5分,共3分)
| 物理量 实验序号 | V(溶液)/mL | NH4Cl质量(g) | 温度(℃) | pH | …… |
| 1 | m | T1 | …… | ||
| 2 | m | T2 | Y | …… |
(其它答案合理也给分)
③(10-X×0.25×53.5)/m(2分)