
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
化 学 试 卷
试卷满分100分,选择题部分共18题,54分。填空题共46分
H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 S:32 Cl:35.5
Ca:40 Mn:55 Fe:56 Cu:64 Zn:65 Br:80 Ag:108
第一部分
一.单项选择题(共18小题,每个小题只有一个选项符合要求,共54分)
1.化学在人类生活中扮演着重要角色,以下应用正确的是
A.用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的
B.为改善食物的色、香、味并防止变质,可在其中加入大量食品添加剂
C.使用无磷洗衣粉,可彻底解决水体富营养化问题
D.天然药物无任何毒副作用,可长期服用
2. 中学化学中很多“规律”都有其使用范围,下列根据有关“规律”推出的结论合理的是
A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大
B.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7
C.根据溶液的pH与溶液酸碱性的关系,推出pH=6.8的溶液一定显酸性
D.根据较强酸可以制取较弱酸的规律,推出![]() 通入NaClO溶液中能生成HclO
通入NaClO溶液中能生成HclO
3.下列有关化学用语表示正确的是
A.N2的电子式:![]()
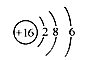
B.S2-的结构示意图:
C.质子数为53,中子数为78的碘原子:53131I
D.邻羟基苯甲酸的结构简式: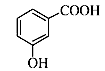
4.将足量![]() 通入下列各溶液中,所含离子还能大量共存的是
通入下列各溶液中,所含离子还能大量共存的是
C.![]() D.
D.![]()
5.浓硫酸的许多性质中,在与含有水分的蔗糖作用过程中不能显示的性质是
A.酸性 B.脱水性 C.强氧化性 D.吸水性
6. 垃圾分类有利于资源回收利用。下列垃圾归类不合理的是
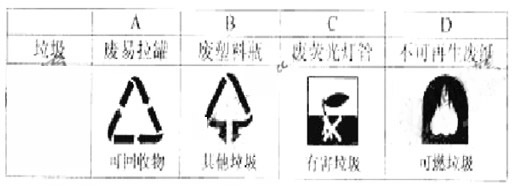
7. 下列有关实验操作、现象和解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 过量的Fe粉中加入 | 溶液呈红色 | 稀 |
| B | Agl沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比Agl更难溶 |
| C | Al箔插入稀 | 无现象 | Al箔表面被 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
8.Al、Fe、Cu都是重要的金属元素。下列说法正确的是
A.三者对应的氧化物均为碱性氧化物
B.三者的单质放置在空气中只生成氧化物
C.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法
D.电解AlCl3、FeCl3、CuCl2的混合溶液是阴极上依次析出Cu、Fe、Al
9.下列表示对应化学反应的离子方程式正确的是
A.FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+
B.NO2与水的反应:3NO2+H2O=2NO3-+NO+2H+
C.醋酸溶液水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑
D.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
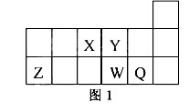 10.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图1所示。下列说法正确的是
10.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图1所示。下列说法正确的是
A.元素X与元素Z的最高正化合价之和的数值等于8
B.原子半径的大小顺序为:rX>rY>rZ>rW>rQ
C.离子Y2-和Z3+的核外电子数和电子层数都不相同
D.元素W的最高价氧化物对应的水化物的酸性比Q的强
11.下列实验方案中,不能测定Na2CO3和NaCHO3,混合物中Na2CO3质量分数的是
A.取a克混合物充分加热,剩余b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体。
12、下列试验现象预测正确的是
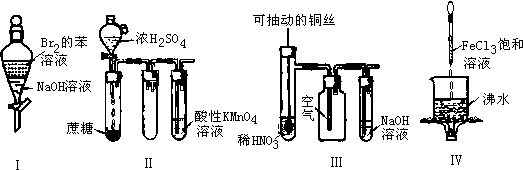
A、实验I:振荡后静置,上层溶液颜色保持不变
B、实验II:酸性KMnO4溶液中出现气泡,且颜色不逐渐褪去
C、实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色
D、实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应
13.褪黑素是一种内源性生物钟调节剂,在人体内由食物中的色氨酸转化得到。
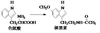
下列说法不正确的是
A.色氨酸分子中存在氨基和羧基,可形成内盐,具有较高的熔点
B.褪黑素与色氨酸结构相似,也具有两性化合物的特性
C.在一定条件下,色氨酸可发生缩聚反应
D.在色氨酸水溶液中,可通过调节溶液的pH使其形成晶体析出
14.25℃时,向10mL 0.01mol/L KOH溶液中滴加0.01mol/L苯酚溶液,混合溶液中粒子浓度关系正确的是
A.pH>7时,c(C6H5O-)>c(K+)>c(H+)>c(OH―)
B. V=20mL时,c(C6H5O-)+c(C6H5OH)=2c(K+)
C.pH<7时,c(K+)>c(C6H5O-)>c(H+)>c(OH―)
D.V=10mL时,c(K+)=c(C6H5O-)>c(OH―)=c(H+)
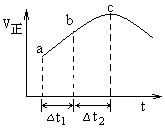 15.向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)
15.向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)![]() SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如右所示。由图可得出的正确结论是
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如右所示。由图可得出的正确结论是
A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.反应物的总能量低于生成物的总能量
D.△t1=△t2时,SO2的转化率:a~b段小于b~c段
16.研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:![]() 下列“水” 电池在海水中放电时的有关说法正确的是:
下列“水” 电池在海水中放电时的有关说法正确的是:
A.![]() 是还原产物
是还原产物
B.正极反应式:![]()
C.每生成1 mol![]() 转移2 mol电子
转移2 mol电子
D.![]() 不断向“水”电池的负极移动
不断向“水”电池的负极移动
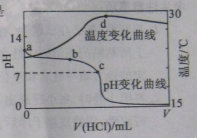 17.室温下,将1.000mol
17.室温下,将1.000mol![]()
![]() 盐酸滴入20.00mL 1.000mol
盐酸滴入20.00mL 1.000mol![]()
![]() 氨水中,溶液pH和温度随加入盐酸体积变化曲线如右图所示。下列有关说法正确的是
氨水中,溶液pH和温度随加入盐酸体积变化曲线如右图所示。下列有关说法正确的是
A. a点由水电离出的![]()
B. b点:![]()
C.c点:![]()
D.d点后,容易温度略下降的主要原因是![]() 电离吸热
电离吸热
18.下列图示与对应的叙述相符的是
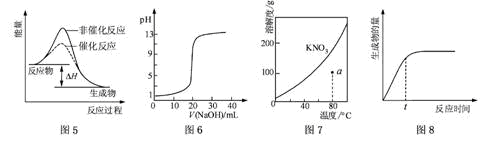
A.图5表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
B.图6表示0.1000 mol·L-1NaOH溶液滴定20.00mL0.1000 mol·L-1CH3COOH溶液所得到的滴定曲线
C.图7表示KNO3的溶解度曲线,图中a点所示的溶液是80 ℃时KNO3的不饱和溶液
D.图8 表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时反应物转化率最大
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
第二部分(共四大题,分值共46分)
19.食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的。已知:
氧化性:![]() >Fe3+>I2;还原性:
>Fe3+>I2;还原性:![]() >I-
>I-
3I2+6OH-![]()
![]() +5I-+3H2O;KI+I2
+5I-+3H2O;KI+I2![]() KI3
KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①加KSCN溶液显红色,该红色物质是_________(用化学式表示);CCl4中显紫红色的物质是___________________(用电子式表示)。
②第二份试液中加入足量KI固体后,反应的离子方程式为___________________________、______________________________________。
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失。
写出潮湿环境下KI与氧气反应的化学方程式:_____________________________。
将I2溶于KI溶液,在低温条件下,可制得KI3·H2O。该物质作为食盐加碘剂是否合适?______(填“是”或“否”),并说明理由________________________________________。
(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失。下列物质中有可能作为稳定剂的是___________________。
A.Na2S2O3B.AlCl3C.Na2CO3D.NaNO2
20.(10分)。氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为个.
(2)H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为。
![]() 的沸点比
的沸点比![]() 高,原因是。
高,原因是。
(3)H+可与H2O形成H3O+,H3O+原子采用杂化。H3O+中H-O-H键角比H2O中H-O-H键角大,原因为。
(4)CaO与NaCl的晶胞同为面心立方结构,已知CaO晶体密度为a g·cm-3,NA表示阿伏伽德罗常数,则CaO晶胞体积为cm3
21.(11分)室安卡因(G)是一种抗心率天常药物,可由下列路线合成;
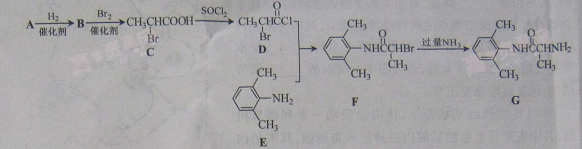
(1)已知A是![]() 的单体,则A中含有的官能团是(写名称)。B的结构简式是。
的单体,则A中含有的官能团是(写名称)。B的结构简式是。
(2)C的名称(系统命名)是,C与足量NaOH醇溶液共热时反应的化学方程式是
。
(3)X是E的同分异构题,X分子中含有苯环,且苯环上一氯代物只有两种,则X所有可能的结构简式有![]() 、、、。
、、、。
(4)F→G的反应类型是。
(5)下列关于室安卡因(G)的说法正确的是。
a.能发生加成反应 b.能使酸性高锰酸钾溶液褪色
c.能与盐酸反应生成盐 d..属于氨基酸
22.(15分)某同学进行试验探究时,欲配制1.0mol•L-1Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2·8H2O试剂(化学式量:315)。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物。为探究原因,该同学查得Ba(OH)2·8H2O在283K、293K和303K时的溶解度(g/100g H2O)分别为2.5、3.9和5.6。
(1)烧杯中未溶物仅为BaCO3,理由是
(2)假设试剂由大量Ba(OH)2·8H2O和少量BaCO3组成,设计试验方案,进行成分检验,在答题卡上写出实验步骤、预期现象和结论。(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。 |  |
| 步骤2:取适量滤液于试管中,滴加稀硫酸。 | |
| 步骤3:取适量步骤1中的沉淀于是试管中, | |
| 步骤4: |
(3)将试剂初步提纯后,准确测定其中Ba(OH)2·8H2O的含量。实验如下:
①配制250ml约0.1mol•L-1Ba(OH)2·8H2O溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水,,将溶液转入,洗涤,定容,摇匀。
②滴定:准确量取25.00ml所配制Ba(OH)2溶液于锥形瓶中,滴加指示剂,将
(填“0.020”、“0.05”、“0.1980”或“1.5”)mol•L-1盐酸装入50ml酸式滴定管,滴定至终点,记录数据。重复滴定2次。平均消耗盐酸Vml。
(4)室温下,(填“能”或“不能”)配制1.0 mol•L-1Ba(OH)2溶液
参考答案
1-18选择题
| A | D | C | B | A | B | D | C | B | A | C | D | B | B | D | A | C | C |
19.
(1)①Fe(SCN)3;(1分)![]() ;(1分)
;(1分)
②![]() +5I-+6H+
+5I-+6H+![]() 3I2+3H2O、2Fe3++2I―
3I2+3H2O、2Fe3++2I―![]() 2Fe2++I2。(各1分)
2Fe2++I2。(各1分)
(2)4KI+O2+2H2O![]() 2I2+4KOH;(1分)
2I2+4KOH;(1分)
否;(1分)KI3受热或潮解后产生KI和I2,KI易被O2氧化,I2易升华。(2分)
(3)AC。(2分)
20.(10分)【解析】(1)氧元素的基态核外电子排布式为:1s22s22p4,4个电子在三个轨道中排布,故未成对的电子个数是两个。
(2)化学键是强烈的相互作用;氢键的作用力比化学键弱,但比范德华力的作用力要强。![]() 可形成分子间的氢键,而
可形成分子间的氢键,而![]() 形成的是分子内的氢键,故前者比后者的沸点要高。
形成的是分子内的氢键,故前者比后者的沸点要高。
(3) H3O+的空间构型为三角锥型,故O原子的杂化方式为sp3;H3O+中O原子只有一对故对电子,排斥力较小,使得键角变大。
(4)根据NaCl的晶胞可知,一个晶胞含有4个CaO,设晶胞的体积为V,则:![]() ×NA×a=56,则V=
×NA×a=56,则V=![]() 。
。
【答案】(1) 2(1分)
(2)O—H键、氢键、范德华力(2分)
![]() 形成的是分子内的氢键,而
形成的是分子内的氢键,而![]() 可形成分子间的氢键,分子间氢键使分子间的作用力增大。(2分)
可形成分子间的氢键,分子间氢键使分子间的作用力增大。(2分)
(3)sp3(1分)H2O中O原子有两对孤对电子,H3O+中O原子只有一对故对电子,排斥力较小(2分)
(4)![]() (2分)
(2分)
21.(11分)【答案】(1)碳碳双键 羧基 (2分)
(2)2-溴丙酸 (1分) ![]() +2NaOH→
+2NaOH→![]() +NaBr+ H2O(2分)
+NaBr+ H2O(2分)
(3)![]()
![]()
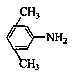 (3分)
(3分)
(4)取代(1分)
(5)abc(2分)
22.(15分)解析:(1)Ba(OH)2·8H2O与CO2作用转化为BaCO3(1分)(2)步骤2:预期现象和结论:有白色沉淀生成,说明有Ba2+。(1分)步骤3:取适量步骤1中的沉淀于是试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气管插入装有澄清石灰水的烧杯中。(2分)预期现象和结论:试管中有气泡生成,烧杯中的澄清石灰水变浑浊,结合步骤2说明沉淀是BaCO3。(2分)步骤4:取适量滤液于烧杯中,用pH计测其pH值。(2分)预期现象和结论:pH>9.6,说明有大量的OH—,综合上面步骤可知试剂由大量Ba(OH)2·8H2O和少量BaCO3组成,假设成立。(2分)(3)①溶解、过滤;250ml的容量瓶中。(2分)②0.1980(2分)思路:0.025x0.1x2=C’x0.05------(盐酸体积最多不能多于50ml)得C’=0.1 mol•L-1所以应该是选大于0.1 mol•L-1而且接近的(4)不能(1分)