清远市一中实验学校高三第一次模拟考试
理科综合(化学试题)
- 选择题:资*源%库
7.设NA为阿伏加德罗常数,下列叙述中正确的是( )
A.标准状况下,11.2L苯中含有C﹣H键的数目为3NA
B.常温下,1.0LPH=13的Ba(OH)2溶液中含有的OH﹣数目为0.1NA
C.常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子
D.电解饱和食盐水,阳极产生22.4L气体时,电路中通过的电子数目为2NA
8.化学与社会、生活密切相关.对下列现象或事实的解释正确的是( )| 选项 | 现象或事实 | 解释 |
| A | 用浸泡过高锰酸钾溶液的硅藻土保鲜水果 | 乙烯能与高锰酸钾发生氧化还原反应 |
| B | 用Na2S除去废水中的Cu2+和Hg2+ | Na2S具有强还原性 |
| C | 用氧化铁制作红色涂料 | 氧化铁能与酸反应 |
| D | 用明矾溶液清除铜镜表面的铜锈 | 明矾溶液中Al3+能与铜锈反应 |
A.AB.BC.CD.D
9.W、X、Y、Z为短周期主族元素,原子序数依次增加,W的一种核素在考古时常用来鉴定一些文物的年代.化合物XZ是重要的调味品,Y原子的最外层电子数等于其电子层数,Z﹣的电子层结构与氩相同.下列说法错误的是( )
A.元素W与氢形成原子比为1:1的化合物有多种
B.元素X的单质能与水、无水乙醇反应
C.离子Y3+与Z﹣的最外层电子数和电子层数都不相同
D.元素W与元素Z可形成含有极性共价键的化合物
资*源%库
10.用CaSO4代替O2与燃料CO反应是一种高效、清洁的新型燃烧技术.反应如下:
①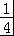 CaSO4(s)+CO(g)⇌
CaSO4(s)+CO(g)⇌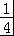 CaS(s)+CO2(g)△H1=﹣47.3 kJ•mol﹣1
CaS(s)+CO2(g)△H1=﹣47.3 kJ•mol﹣1
②CaSO4(s)+CO(g)⇌CaO(s)+CO2(g)+SO2(g)△H2=+210.5kJ•mol﹣1
③CO(g)⇌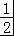 C(s)+
C(s)+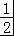 CO2(g)△H3=﹣86.2kJ•mol﹣1.
CO2(g)△H3=﹣86.2kJ•mol﹣1.
下列说法错误的是( )
A.反应①达到平衡时,增大压强平衡不移动
B.反应②的平衡常数表达式为K=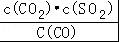
C.反应①和②是主反应,反应③是副反应
D.2CaSO4(s)+7CO(g)⇌CaS(s)+CaO(s)+6CO2(g)+C(s)+SO2(g)是放热反应
11.常温下,下列溶液的离子浓度关系正确的是( )
A.pH=3的醋酸溶液稀释100倍后,溶液的pH=5
B.pH=2的盐酸与等体积0.01 mol·L﹣1醋酸钠混合溶液后,溶液中c(Cl﹣)=c(CH3COO﹣)
C.氨水中通入过量CO2后,溶液中c(H+)+c(NH4+)=c(OH﹣)+c(HCO3﹣)
D.0.1mol AgCl和0.1mol AgI混合后加入1L水中,所得溶液中c(Cl﹣)>c(I﹣)
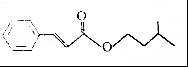
12.肉桂酸异戊酯是一种香料,其结构简式如图.下列有关肉桂酸异戊酯的叙述正确的是( )
 资*源%库
资*源%库
A.不能使溴的四氯化碳溶液褪色B.能与新制的Cu(OH)2共热生成红色沉淀
C.能与FeCl3溶液反应显紫色
D.能与热的浓硝酸和浓硫酸混合液反应
13.利用如图所示装置进行下列实验,能得出相应实验结论的是( )| 项 | ① | ② | ③ | 实验结论 | 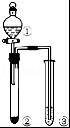 |
| A | 稀盐酸 | Na2SO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
| B | 稀硫酸 | Na2S | 滴加少量AgNO3的KI溶液 | Ksp(AgI)>Ksp(Ag2S) |
| C | 浓盐酸 | KMnO4 | AgNO3和稀硝酸混合溶液 | Cl2溶于水有Cl﹣生成 |
| D | 浓硫酸 | 蔗糖 | Ba(OH)2溶液 | SO2能与碱溶液反应 |
AB.BC.CD.D - 非选择题:
26.(14分)以菱镁矿(主要成分为MgCO3,含少量的Fe2O3等杂质)为原料制备无水氯化镁的一种工艺流程如下:
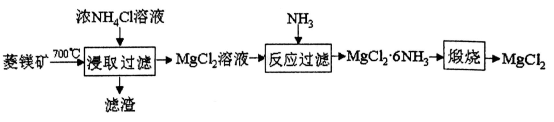
回答下列问题:- 700℃轻烧菱镁矿过程中,碳酸镁分解的化学方程式_____________。
- 浸取过程中主要反应的化学方程式_______________。
- 工艺流程中可循环利用的物质化学式为_________。检验MgCl2·6NH3已完全分解的方法为______________。
- 流程中采用煅烧MgCl2·6NH3而不是煅烧MgCl2·6H2O来获得MgCl2的原因是_________。
- MgCl2在氨水中能与H2O2反应生成漂白剂MgO2.写出该反应的化学方程式________。
27.(14分)乙烯是重要的有机化工原料,某研究性小组研究了不同的制取乙烯的方法。
- 乙烷催化脱氢制乙烯:C2H6(g)
 C2H4(g)+H2(g)
C2H4(g)+H2(g)
已知键能数据如下表:
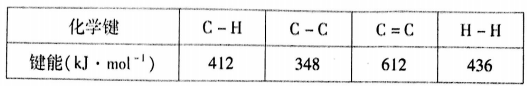
①该反应的△H为________kJ/mol;
②在一定温度和压强下,将0.02mol乙烷投入到容积为1.0L的恒容的密闭反应装置中。在催化剂作用下,C2H4的物质的量随时间变化的曲线如图所示:则0~8s内C2H6的平均反应速率为________mol/(L·min),请计算此条件下该反应的平衡常数Kc为_________。
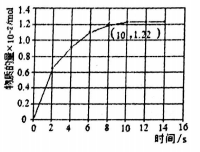
③若采用恒温恒压装置,向平衡混合物中通入适量N2,C2H6的转化率将____(填“减小”、“增大”、“不变”)。 - 氯乙烷制取乙烯C2H5 Cl(g)
 C2H4(g)+HCl(g) △H >0。
C2H4(g)+HCl(g) △H >0。
④其他条件不变,下列与该反应活化能有关的图像正确的是____。
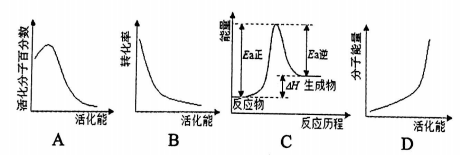
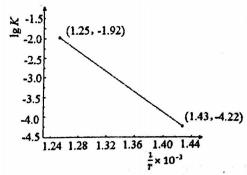
⑤如下图所示,该反应的速率常数K和温度T满足线性方程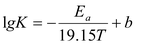 ,则该反应的活化能Ea为______kJ/mol。
,则该反应的活化能Ea为______kJ/mol。
28.(15分)硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]是一种稳定的还原剂,其制备流程如下:

- 硫酸浓度过大,反应过快同时会使FeSO4溶液中混有____(填离子符号)。
- 铁粉中混有少量P、S等元素,反应过程中产生的气体有刺激性气味,实验中应采取的措施_________________。
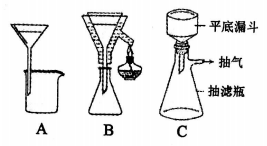
- 铁粉未完全反应,就得趁热过滤,下图中合适的过滤装置是________。
几种物质的溶解度(g /100 gH2O)
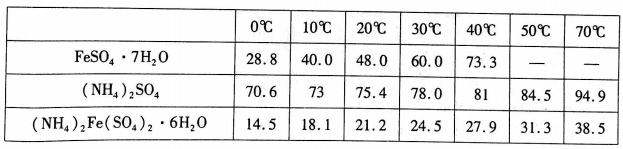
- 利用FeSO4与(NH4)2SO4制备(NH4)2Fe(SO4)2·6H2O的原理是____(用化学方程式及必要的文字说明)。
(5)将(NH4)2SO4晶体加入到FeSO4滤液中,加热搅拌至全部溶解,再_______至溶液表面有晶膜出现时,静置冷却结晶,抽滤,用少量________洗涤晶体2~3次,将晶体放在表面皿上晾干,最终得到的产品质量为19. 6g,本次实验产率为________(本次实验使用4.0g铁粉,剩余0.4g未反应)。
35.【化学-选修2:化学与技术】
三氧化二镍(Ni2O3)是一种重要的电子元件材料和蓄电池材料.工业上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍(NiC2O4•2H2O),再高温煅烧草酸镍制取三氧化二镍.已知草酸的钙、镁、镍盐均难溶于水.工艺流程图如图所示.
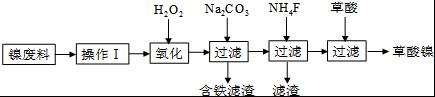
请回答下列问题:
(1)操作Ⅰ为 .
(2)①加入H2O2发生的主要反应的离子方程式为 ;
②加入碳酸钠溶液调pH至4.0~5.0,其目的为 ;
(3)草酸镍(NiC2O4•2H2O)在热空气中干燥脱水后在高温下煅烧,可制得Ni2O3,同时获得混合气体.NiC2O4受热分解的化学方程式为 .
(4)工业上还可用电解法制取Ni2O3,用NaOH溶液调NiCl2溶液的pH至7.5,加入适量Na2SO4后利用惰性电极电解.电解过程中产生的Cl2有80%在弱碱性条件下生成ClO﹣,再把二价镍氧化为三价镍.ClO﹣氧化Ni(OH)2生成Ni2O3的离子方程式为 .a mol二价镍全部转化为三价镍时,外电路中通过电子的物质的量为 .
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时,NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是 .
36.【化学-选修3物质结构与性质】
氮族元素(Nitrogen group)是元素周期表VA 族的所有元素,包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)和Uup共计六种.
(1)氮族元素的外围电子排布式的通式为 ;基态磷原子中,电子占据的最高能层符号为 ,该能层具有的原子轨道数为 .
(2)PH3分子的VSEPR模型为 ,键角NH3 H2O(填“>”、“<”或“=”).
(3)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子中氮的杂化方式为 .
(4)从化合物NF3和NH3的结构与性质关系比较,回答它们两者如下性质差异原因:
①NF3的沸点为﹣129℃,而NH3的沸点为﹣33℃,其原因是 .
②NH3易与Cu2+反应,而NF3却不能,其原因是 . - 磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层,磷化硼晶体的晶胞结构与金刚石类似,磷原子作面心立方最密堆积,则硼原子的配位数为 ;已知磷化硼的晶胞边长a=478pm,计算晶体中硼原子和磷原子的核间距(dB﹣P)= pm(保留三位有效数字).
$来&源:
一模化学答案:
一、7--13 ABCCD DB
二、26.(14分)
(1)漂白性
(2)还原性,抑制
(3)SO2+2CO S +2CO2
S +2CO2
(4)物理,激发
(5)2SO2+2e-= S2O42-
27.(14分)
(1)MgCO3 MgO+CO2↑
MgO+CO2↑
(2)MgO+H2O+2NH4Cl=MgCl2+2NH3·H2O(其它合理答案也给分)。
(3)NH3前后两次称量质量不变(恒重法或检验氨气)
(4)MgCl2能与水发生水解,煅烧MgCl2·6H2O最终得到的是MgO
(5)MgCl2+ H2O2 +2 NH3·H2O = MgO2+2NH4Cl +2H2O
28.(15分)
①124
②1.5×10-3, 0.019(有无单位均给分)
③增大
④C
⑤2.4×105
35、解:(1)分析框图:“酸溶”生成含镍、铁、钙、镁离子的溶液,加酸溶解,溶解金属,除去不溶物过滤;
故答案为:加酸溶解,过滤;
(2)加双氧水的目的是氧化生成Fe3+,反应的离子方程式为:2Fe2++H2O2+2H+═2Fe3++2H2O,加入碳酸钠溶液的作用是调节pH,促进铁离子水解沉淀完全,;
故答案为:2Fe2++H2O2+2H+═2Fe3++2H2O,促进铁离子水解沉淀完全;
(3)草酸镍(NiC2O4•2H2O)在热空气中干燥脱水后生成NiC2O4,NiC2O4再发生氧化还原反应(Ni由+2价升高到+3价,则C由+3价降低到+2价,题中要求生成混合气体,则另一气体为CO2)生成Ni2O3、CO、CO2,再利用化合价升降相等,Ni:升高2×(3﹣2),C:升高1×(4﹣3),C:降低:3×(3﹣2),配平方程式为:2NiC2O4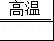 Ni2O3+3CO↑+CO2↑;
Ni2O3+3CO↑+CO2↑;
故答案为:2NiC2O4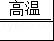 Ni2O3+3CO↑+CO2↑;
Ni2O3+3CO↑+CO2↑;
(4)Cl由+1价降低到﹣1价,Ni由+2价升高到+3价,利用化合价升降相等可配平ClO﹣、Ni(OH)2、Cl﹣、Ni2O3的系数,再利用H原子守恒配平水的系数,最后可利用O原子检查配平是否正确,得到离子方程式为:ClO﹣+2Ni(OH)2═Cl﹣+Ni2O3+2H2O;
ClO﹣+2Ni(OH)2═Cl﹣+Ni2O3+2H2O
1 2
n(ClO﹣) a mol
则n(ClO﹣)=0.5 a mol
Cl2+2OH﹣═ClO﹣+Cl﹣+H2O
0.8n(Cl2) 0.5 a mol
则n(Cl2)=0.625 a mol
进行电解时:
2Cl﹣﹣2e﹣═Cl2↑
2 1
n(e﹣) 0.625 a mol
则n(e﹣)=1.25a mol;
故答案:ClO﹣+2Ni(OH)2═Cl﹣+Ni2O3+2H2O;1.25a mol;
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,发生还原反应,则Al发生氧化反应,碱性条件下得到NaAlO2,该电池反应的化学方程式是:Al+3NiO(OH)+NaOH+H2O=3Ni(OH)2+NaAlO2,
故答案为:Al+3NiO(OH)+NaOH+H2O=3Ni(OH)2+NaAlO2.
36、解:(1)氮族元素的外围电子为其最外层上s、p能级电子,则氮族元素外围电子排布式为ns2np3;基态磷原子中,电子占据的最高能层符号为M,该能层有1个s轨道、3个p轨道、5个d轨道,所以有9个轨道,
故答案为:ns2np3;M;9;
(2)PH3分子中P原子价层电子对个数是4且含有一个孤电子对,根据价层电子对互斥理论判断该分子的VSEPR模型为四面体形,成键电子对和孤电子对之间的排斥力小于孤电子对之间的排斥力,氨气分子中只含一个孤电子对、水分子中含有两个孤电子对,所以键角,
故答案为:四面体形;>;
(3)氮的最高价氧化物为N2O5,由两种离子构成,其中阴离子构型为平面正三角形,化学式应为NO3﹣,则其阳离子的化学式为:NO2+,其中心原子价电子对数为2+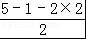 =2,根据价层电子对互斥理论判断原子杂化方式为sp,
=2,根据价层电子对互斥理论判断原子杂化方式为sp,
故答案为:sp杂化;
(4)①NH3存在氢键,而NF3只存在分子间作用力,两种作用力前者较强,物质的沸点较高,
故答案为:NH3分子间存在较强的氢键,而NF3分子间仅有较弱的范德华力;
②F的电负性大于N元素,NF3中N﹣F成键电子对偏向于F原子,N原子上的孤对电子难与铜离子形成配离子,所以NF3不易与Cu2+形成配离子,
故答案为:F的电负性大于N元素,NF3中N﹣F成键电子对偏向于F原子,N原子上的孤对电子难与铜离子形成配离子;
(5)磷化硼结构如图所示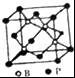 ,该晶胞中B原子为4个、P原子个数=8×
,该晶胞中B原子为4个、P原子个数=8× +6×
+6×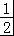 =4,每个B原子连接4个P原子,则硼原子的配位数为4;已知磷化硼的晶胞边长a=478pm,则晶胞的体对角线长为
=4,每个B原子连接4个P原子,则硼原子的配位数为4;已知磷化硼的晶胞边长a=478pm,则晶胞的体对角线长为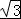 a,晶体中硼原子和磷原子的核间距应为体对角线的
a,晶体中硼原子和磷原子的核间距应为体对角线的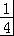 ,所以dB﹣P=
,所以dB﹣P=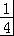
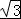 ×478pm=207pm,
×478pm=207pm,
故答案为:4;207.

 资*源%库
资*源%库




![]() ,则该反应的活化能Ea为______kJ/mol。
,则该反应的活化能Ea为______kJ/mol。




![]() S +2CO2
S +2CO2![]() MgO+CO2↑
MgO+CO2↑![]() Ni2O3+3CO↑+CO2↑;
Ni2O3+3CO↑+CO2↑;![]() Ni2O3+3CO↑+CO2↑;
Ni2O3+3CO↑+CO2↑;![]() =2,根据价层电子对互斥理论判断原子杂化方式为sp,
=2,根据价层电子对互斥理论判断原子杂化方式为sp, ,该晶胞中B原子为4个、P原子个数=8×
,该晶胞中B原子为4个、P原子个数=8×![]() +6×
+6×![]() =4,每个B原子连接4个P原子,则硼原子的配位数为4;已知磷化硼的晶胞边长a=478pm,则晶胞的体对角线长为
=4,每个B原子连接4个P原子,则硼原子的配位数为4;已知磷化硼的晶胞边长a=478pm,则晶胞的体对角线长为![]() a,晶体中硼原子和磷原子的核间距应为体对角线的
a,晶体中硼原子和磷原子的核间距应为体对角线的![]() ,所以dB﹣P=
,所以dB﹣P=![]()
![]() ×478pm=207pm,
×478pm=207pm,