
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2017届高三年级第西次模拟考试
化学
注意事项
可能用到的相対原子质量:H1 C 12N14016S32K39Fe56
第I卷选择题(共40分)
单项选择题:本题包括10小题,每小题2分,共计20分。每小题了个选项符合题意。
1.化学与生产、生活、科技、环境等密切相关。下列说法正确的是
A.地沟油禁止用于食品用油,但可以用亍制肥皂
B.用漂粉精和洁厕灵(主要成分是盐酸)混合后的浓溶液清洗马捅效果更佳
C.光化学烟雾、硝酸型酸雨的形成都与煤的大量燃烧有关
D.碳纤维是一种新型的高强度的有机高分子材料
2.下列化学用语正确的是
 3.下列有关物质的性质或应用的说法不ik确的是
3.下列有关物质的性质或应用的说法不ik确的是
A.水玻璃可用于生产黏合剤和防火剤
B.油脂水解可得到氨基酸和甘油
C.盐析可提纯蛋白质并保持其生理活性
D.FeCl3溶液能与Cu反应,可用于蚀刻印刷电路
4.短周期元素X、Y、Z、W、R的原子序数依次增大,其中只有Z和W是金属元素,X与Z同一主族;Y的气态氢化物与其最高价氧化物对应水化物可以化合生成盐;W的氢氧化物可与Z 和R的最高价氧化物对应水化物反应;R的单质常温下是黄绿色气体,常用于自来水的杀菌、消毒。下列说法正确的是$来&源:
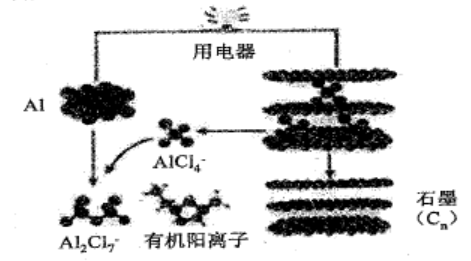
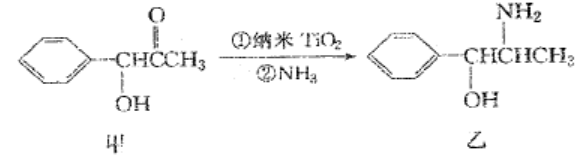
A.原子半径:Y B. X元素的最高正价和最低负价的绝对值相等 C. Y的单质化学性质很稳定,不与任何金属发生反应 D.工业上通常用W和R形成的化合物来冶炼金属W 5.下列离子方程式书写正确的是 6.实验室拟制备纯净的氯气并回收剩余药品,下列图示装置和原理能达到实验目的的是 7.下列有关说法正确的是 A.用金属活动性顺序可解释反应:Na(I)+KC1(I)=NaCi(I)+K(g) B. 0.1molNa202和足量C02气体充分反应,理论上转移的电子数目为0.2x6.02xl023 C.高温下,工业上用纯碱和石英砂制玻璃,说明硅酸的酸性强于碳酸 D.常温下,NH4C1溶液加水稀释后,溶液中的值不变 8.常温下,下列各组离子在指定的条件下一定能大量共存的是 B.在某无色溶液中:K+、H+、IO3-、r C.在c (H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、N03- D.水电离出 c(H+)=10-12的溶液中:Mg2+、Cu2+、SO42-、K+ 9.甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化),下列各组物质中,满足图示转化关系的是 A.①③ B.②③ C.②④ D.①④ A.图甲表示H2与02发生反应过程中的能量变化,则H2的燃烧热△H=-241.8kJ•mo1-1 B.图乙可以表示对某化学平衡体系改变温度后反应速率随时间的变化 C.图丙表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数 D.图丁表示常温卞,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH 不定项选择题;本题包括5小题,每小题4分,共计20分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。 11.某有机物X的结构如图所示,下列有关说法正确的是 A.X分子中含1个手性碳原子 B.X能与NaHC03反应放出二氧化碳 C.X能发生缩聚、消去、银镜反应 D. 1 mol X最多能与含4 mol Br2的浓溴水反应 12.2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用A1Cl4-和有机阳离子构成电解质溶液,其放电工作原理如右图所示。下列说法不正确的是 A.放电时,铝为负极、石墨为正极 B.放电时,有机阳离子向铝电极方向移动 C.放电时的负极反应为:Al-3e- + 7A1Cl4-= 4 A12Cl7- D.充电时的阳极反应为:Cn + AlCl4-e-=CnAlCl4 13.下列依据相关实验得出的结论正确的是. A.向新制的氯水中加入NaHC03粉末,有气泡产生,说明氯元素的非金属性强于碳 B.向Fe(N03)3溶液中通入适量S02气体后,再滴加BaCl2溶液,产生白色沉淀,说明Fe3+能够将H2SO3氧化为H2SO4 C.向NaOH溶液中滴加少量的MgCl2溶液,产生白色沉淀,然后再滴加足量的CuCl2溶液,沉淀变蓝色,说明 Ksp[Cu(OH)2] D.用铂丝蘸取少量某溶液进行焰色反应,火焰呈紫色,说明该溶液一定含有钾元素 b、c、d三点的溶液中水的电离程度:b a 点溶液中:c(Na+)=2c(OH-)-2c(H+) d 点溶液中:c[(CH3)2NH2+]+c(H+)—(OH-)=O.lOO mol•L-1 e 点溶液中:c(H+)>c[(CH3)2NH2+]+2c[(CH3)2NH•H20] 15.一定温度下,在三个体积均为2.0 L的恒容密闭容器中发生反应: 3CO(g) + 3H2(g)=CH3OCH3(g) + C02(g) 下列说法正确的是 A.达到平衡时,容器I中的逆反应速率大于容器Ⅲ中的正反应速率 B.达到平衡时,容器I中CO的转化率与容器Ⅱ中C02的转化率之和小于I C.达到平衡时,容器Ⅱ中c(C02)大于容器Ⅲ中c(C02)的3倍 D.若起始时向容器Ⅲ中充入四种反应物质且物质的量均为0.04mol,则反应将向正反应方向进行 第Ⅱ卷非选择题(共80分) 16. (12分)高纯氧化镁可用于冶金、橡胶、电子等行业。利用轻烧白云灰粉料(主要成分是氧化镁、氧化钙及微量二氧化硅)制备高纯氧化镁的流程如下: 写出E的两种满足下列条件的同分异构体的结构简式:▲。 ①该物质能使FeCl3溶液显色;②分子中有3种不同化学环境的氢。 (5)参照上述合成路线,以E和乙醇为原料(无机试剂任选),设计制备 路线。 其中“沉淀”的滤渣是FeC204•2H20 ,“氧化”得到绿色溶液并有红褐色沉淀生成。 (3)收获产物后,为测定产品中C204>的含量,准确称取0.8490g产品,配制成250mL溶液3移取 25.00mL溶液,酸化后用标定浓度力O.OlOOOmol•L-1的高猛酸钾溶液滴定至终点,消耗22.25mL 溶液,用同浓度的高锰酸钾溶液滴定25.0mL配制溶液用的蒸馏水,滴定至终点消耗1.05mL, 计算产品中C2042-的含量。 (K3[Fe(C204)3]•3H20的相对分子质量为491.3)$来&源: 已知K3[Fe(C204)3]•3H20纯品中C2042-的含量为53.73%,实际产品中C2042-的含量与纯品相比产生偏差的原因是▲。 19. (15分)二氧化氯(C1O2)是第四代杀菌消毒剂,因其高效、无污染而被广泛使用。以下是氯化钠电解法生产C1O2的工艺流程。已知:①二氧化氯是一种强氧化性气体,呈黄绿色,易溶于水的,不与水反应。②纯C1O2易分解爆炸,一般用稀有气体或氮气稀释到10%以下安全。③C1O2和C12的熔沸点如右下表所示。 PH3+202=H3P04,写出负极的电极反应式▲。 21.(12分)纳米Ti02是一种应用广泛的催化剂,纳米Ti02催化的一个实例如下所示。 (4)与NH3分子互为等电子体的阳离子为▲,氨的沸点▲(“高于”或“低于”)膦(PH3)的原因是▲。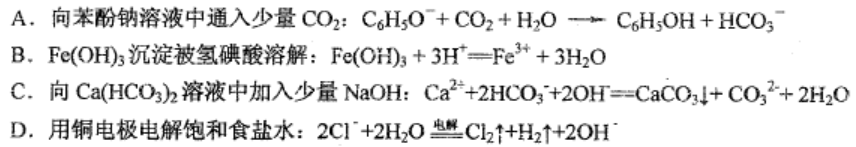
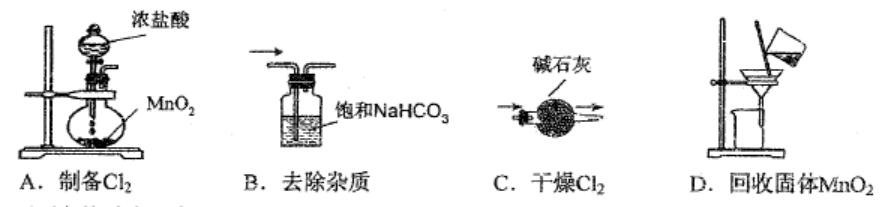
甲 乙 丙 戊 ① NH3 O2 NO H2O ② Fe H2O H2 Fe2O3 ③ A1203 NaOH溶液 NaA102溶液 过量CO2 ④ CO2 O2 Na 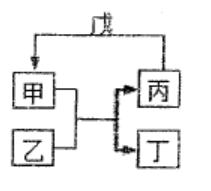
 10.下列关于各图的叙述正确的是
10.下列关于各图的叙述正确的是![]() >
>![]()
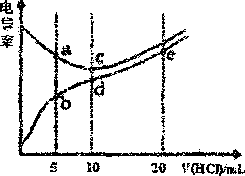 14.电解质溶液的电导率越大,导电能力越强。常温下用0.100 mol•L-1盐酸分别滴定1O.OOmL浓度 均为0.100 mol•L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氨相似,常温 Kb[(CH3)2NH•H2O3=1.6xl04),利用传感器测得滴定过程中溶液的电导率如图所示》下列说法正确的是
14.电解质溶液的电导率越大,导电能力越强。常温下用0.100 mol•L-1盐酸分别滴定1O.OOmL浓度 均为0.100 mol•L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氨相似,常温 Kb[(CH3)2NH•H2O3=1.6xl04),利用传感器测得滴定过程中溶液的电导率如图所示》下列说法正确的是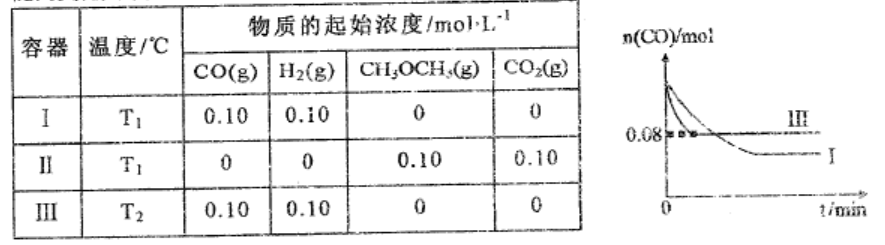 各容器中起始物质的量浓度与反应温度如下表所示,反应过程中I、Ⅲ容器中CO的物质的量随间变化关系如图所示
各容器中起始物质的量浓度与反应温度如下表所示,反应过程中I、Ⅲ容器中CO的物质的量随间变化关系如图所示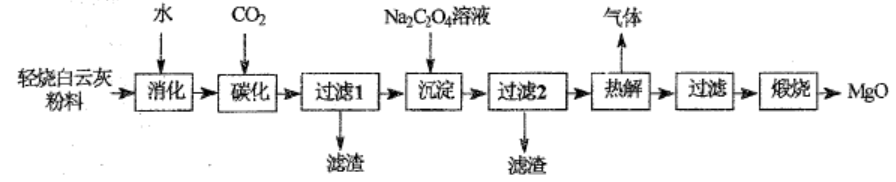
(2)“过滤1”的滤渣主要成分为▲(填化学式),滤液中仍会有少量Ca2+,加入Na2C204溶液可将其转化为CaC204沉淀。若向CaCl2溶液中加入Na2C03和Na2C204,当两种沉淀共存时,c(C032-): c(C204)=▲(已知:KspCaCO3=2.5xlO-9, KspCaC2O4=4.0xl0-8); Na2C204的用量对Ca2+去除率和Mg2+损失率的影响如下图所示。你认为Na2C204与Ca2+最佳的物质的量之比为__▲。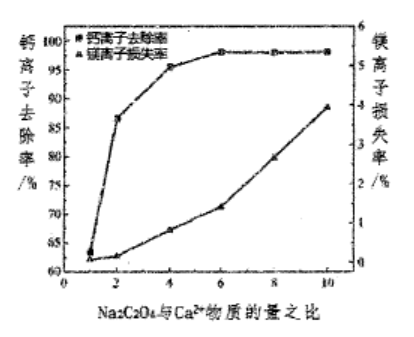
(3)“过滤3”得到的滤液为高纯度Mg(HC03)2,请写出其热解生成不Mg2(0H)2C03的化学方程式__▲。
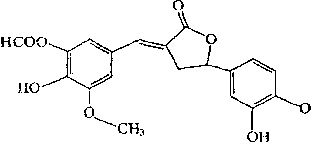
(4)上述流程中可以直接循环使用的物质是▲。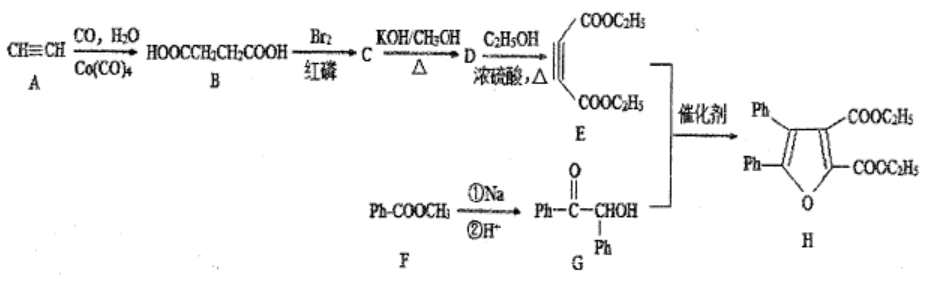 17.(15分)呋喃类化合物是重要的有机合成中间体。下面是某研究小组合成呋喃类化合物的路线:
17.(15分)呋喃类化合物是重要的有机合成中间体。下面是某研究小组合成呋喃类化合物的路线:
注:Ph—为苯环。回答下列问题:![]()
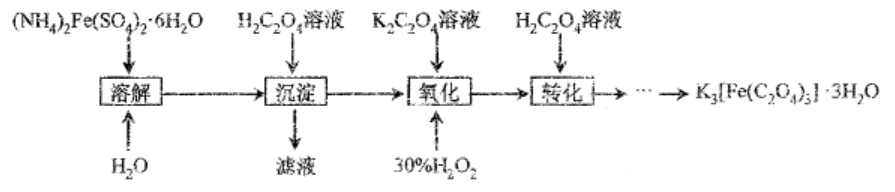 18. (12分)制备负载型活性铁催化剂的主要原料K3(Fe(C204)3]•3H20 (三草酸合铁(Ⅲ)酸钾)为绿色晶体,易溶于水,难溶于乙醇、丙酮等有机溶剂。110℃下失去结晶水, 230℃下即可分解, 实验室具备K3[Fe(C204)3]•3H20的部分实验过程如下:
18. (12分)制备负载型活性铁催化剂的主要原料K3(Fe(C204)3]•3H20 (三草酸合铁(Ⅲ)酸钾)为绿色晶体,易溶于水,难溶于乙醇、丙酮等有机溶剂。110℃下失去结晶水, 230℃下即可分解, 实验室具备K3[Fe(C204)3]•3H20的部分实验过程如下: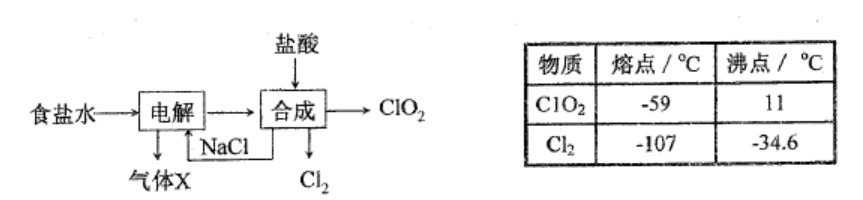
(5) C102可用于处理含硫的废水。课外实验小组为了探究C102与Na2S溶液反应的产物中含有Cl-和SO42-,不含SO32-。设计了以下实验装置: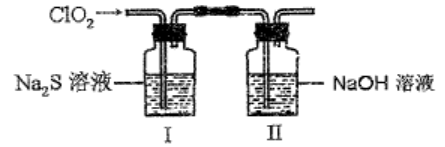
①在装置Ⅱ中C102和NaOH溶液反应生成等物质的量的两种盐,其中一种盐为NaC102,写出该反应的离子方程式▲。
②请补充完整实验步骤:将用氮气稀释后的足量C102通入I中的Na2S溶液中充分反应,得到无色澄清溶液。i.取少量I中溶液于试管甲中,▲,证明溶液中无SO32-,ii.另取少量I中溶液于试管乙中,▲。
20. (14分)磷化氢(PH3)环流熏蒸广泛应用于粮食、烟草、中草药、綿麻等行业杀虫作业。
(1)磷化钙可由磷灰石和焦炭在一定条件下反应获得。相关热化学方程式如下: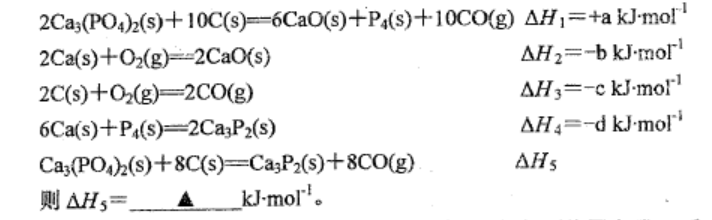
(2)PH3可利用磷化钙水解等若干方便的方法制取。但却不能用白磷(P4)和氢气直接化合的方法来制备,试运用焓变和熵变的相关知识进行解释▲。
(3)磷化氢毒性极强,磷化氢中毒后可用CuS04溶液解毒,解毒时反应生成H3P04、H2S04和难溶 性Cu3P,其离子方程式为▲。
(4)磷化氢在高温下分解生成两种气态物质。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如题20图-1所示,磷化氢在高温下分解反应的化学方程式为▲。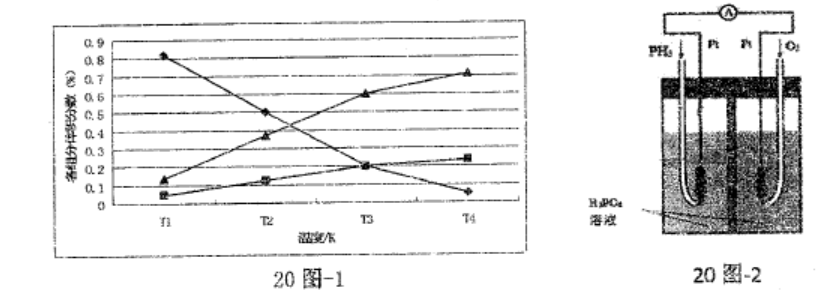
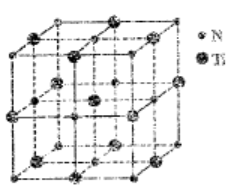 (5)有一种氮化钛晶体的晶胞如图所示,该晶体的化学式可表示为▲。
(5)有一种氮化钛晶体的晶胞如图所示,该晶体的化学式可表示为▲。
