
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2017~2018学年第一学期高三第一次模拟考试
理科综合试题
可用的化学相对原子量:C:12 H:1 N:14 O:16
一、选择题(每题6分,共78分)
7.化学在生活中有着广泛的应用,下列对应关系错误的是( )
| 化学性质 | 实际应用 | |
| A | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
| B. | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
| C. | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
| D | HF与SiO2反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
8. 某溶液由相同物质的量的CuCl2、FeCl3、AlCl3混合而成,向该溶液中加入铁粉,充分搅拌后振荡,铁粉仍有剩余,则溶液中主要存在的阳离子是( )
| A.Fe3+、Cu2+ | B.Fe2+、Al3+ | C.Fe3+、Al3+ | D.Fe2+、Fe3+ |
9.将物质的量相等的硫酸铝和硫酸铵溶于水形成V mL混合溶液,向混合溶液中逐滴加入某氢氧化钠溶液(其物质的量浓度为混合溶液中两溶质的物质的量浓度之和),直至过量.下列表示氢氧化钠溶液加入的体积(x)与溶液中沉淀物的量(y)的关系示意图中正确的是( )
A.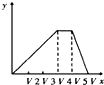 B.
B.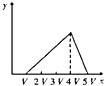 C.
C.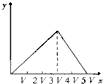 D.
D.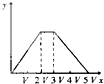
10.下列说法不正确的是 ( )
A.向乙酸乙酯中加入饱和Na2CO3溶液,振荡,分液分离除去乙酸乙酯中的少量乙酸
B.用溴水鉴别苯、乙醇、四氯化碳
C.汽油、柴油和植物油都是碳氢化合物,完全燃烧只生成CO2和H2O
D.部分油脂不能使溴的四氯化碳溶液褪色
11.图示为一种天然产物,具有一定的除草功效。下列有关该化合物的说法错误的是( )
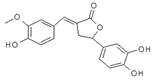
A.分子中含有三种含氧官能团
B.1 mol该化合物最多能与6molNaOH反应
C.既可以发生取代反应,又能够发生加成反应
D.能与FeCl3发生显色反应,分子中所有碳原子可能共面
12. 某有机物的结构简式为 ![]() ,它的同分异构体中属于芳香醇的共有( )
,它的同分异构体中属于芳香醇的共有( )
A.3种 B.4种 C.5种 D.6种
13. 铝土矿的主要成分中含有氧化铝、氧化铁和二氧化硅等,工业上经过下列工艺可以冶炼金属铝。下列说法错误的是( )
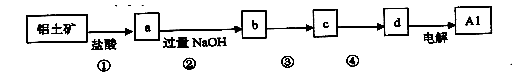
A.①、②中除加试剂外,还需要进行过滤操作B.a、b中铝元素的化合价相同
C.③中需要通入过量的氨气D.④进行的操作是加热,而且d一定是氧化铝
26.(11分)某混合物 A,含有 KAl(SO4)2、Al2O3 和 Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
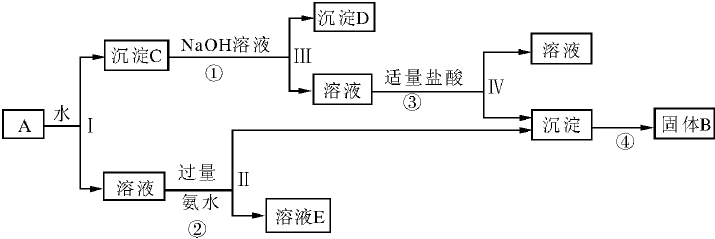
据此回答下列问题:
27.(18分)某小组在验证反应“Fe+2Ag+=Fe2++2Ag”的实验中检测到Fe3+,发现和探究过程如下。向硝酸酸化的0.05 mol·L-1硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。
(1)检验产物
①取出少量黑色固体,洗涤后,____(填操作和现象)证明黑色固体中含有Ag。
②取上层清液,滴加K3[Fe(CN)6]溶液,产生蓝色沉淀,说明溶液中含有_______。
(2)针对“溶液呈黄色”,甲认为溶液中有Fe3+,乙认为铁粉过量时不可能有Fe3+,乙依据的原理是___________________(用离子方程式表示)。
针对两种观点继续实验:
①取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测。同时发现有白色沉淀产生,且溶液颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
| 序号 | 取样时间/min | 现象 |
| ⅰ | 3 | 产生大量白色沉淀;溶液呈红色 |
| ⅱ | 30 | 产生白色沉淀;较3 min时量少;溶液红色较3 min时加深 |
| ⅲ | 120 | 产生白色沉淀;较30 min时量少;溶液红色较30 min时变浅 |
(资料:Ag+与SCN-生成白色沉淀AgSCN)
② 对Fe3+产生的原因作出如下假设:
假设a:可能是铁粉表面有氧化层,能产生Fe3+;
假设b:空气中存在O2,由于________(用离子方程式表示),可产生Fe3+;
假设c:酸性溶液中NO3-具有氧化性,可产生Fe3+;
假设d:根据_______现象,判断溶液中存在Ag+,可产生Fe3+。
③ 下列实验Ⅰ可证实假设a、b、c不是产生Fe3+的主要原因。实验Ⅱ可证实假设d成立。
实验Ⅰ:向硝酸酸化的________溶液(pH≈2)中加入过量铁粉,搅拌后静置,不同时间取上层清液滴加KSCN溶液,3 min时溶液呈浅红色,30 min后溶液几乎无色。
实验Ⅱ:装置如图。其中甲溶液是________,操作及现象是________________。
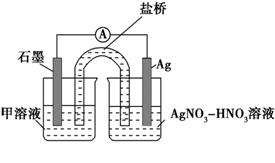
(3)根据实验现象,结合方程式推测实验ⅰ~ⅲ中Fe3+浓度变化的原因:______。
28.(14分)利用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等)制取草酸钴的工艺流程如下:
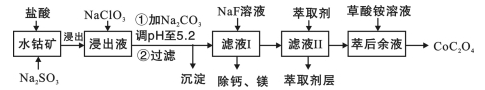
已知①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
![]()
(1)浸出过程中加入Na2SO3的目的是_____________。
 (2)制取NaClO3可以将氯气通入到热的浓氢氧化钠溶液,该反应的离子方程式为 ;实验需要制取10.65克NaClO3,需要的氯气由电解食盐水生成,若不考虑反应过程中的损失,则同时生成的氢气的体积为 (标准状况)。
(2)制取NaClO3可以将氯气通入到热的浓氢氧化钠溶液,该反应的离子方程式为 ;实验需要制取10.65克NaClO3,需要的氯气由电解食盐水生成,若不考虑反应过程中的损失,则同时生成的氢气的体积为 (标准状况)。
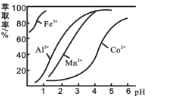
(3)萃取剂对金属离子的萃取率与pH的关系如图所示。
滤液Ⅱ中加入萃取剂的作用是_________;使用萃取剂适宜的pH是______(填选项序号)。
A.接近2.0 B.接近3.0 C.接近5.0
(4)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。
已知K sp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液c(Mg2+)/ c(Ca2+)=________________。
(5)工业上用氨水吸收废气中的SO2。已知NH3·H2O的电离平衡常数K1 =1.8×10-5mol·L-1H2SO4的电离平衡常数K2=1.2×10-2mol·L-1,K3 =1.3×10-8mol·L-1。在通入废气的过程中:
当恰好形成正盐时,溶液中离子浓度的大小关系为 。
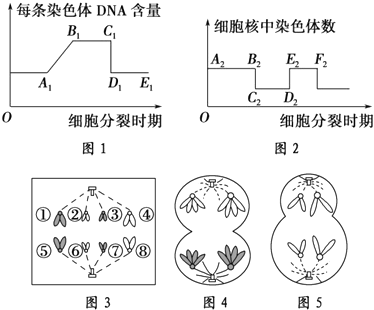
29、(8分)下列是有关二倍体生物的细胞分裂图示.请据图分析回答下列问题.
30、(10分)某植物净光合速率的变化趋势如图所示。据图回答下列问题:
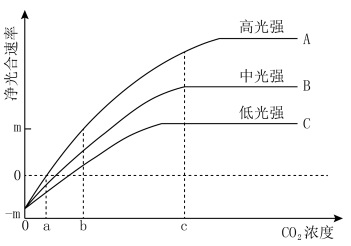
(1)当![]() 浓度为a时,高光强下该植物的净光合速率为 。
浓度为a时,高光强下该植物的净光合速率为 。![]() 浓度在a~b之间时,曲线 表示了净光合速率随
浓度在a~b之间时,曲线 表示了净光合速率随![]() 浓度的增高而增高。
浓度的增高而增高。
(2)![]() 浓度大于c时,曲线B和C所表示的净光合速率不再增加,限制其增加的环境因素主要是 。
浓度大于c时,曲线B和C所表示的净光合速率不再增加,限制其增加的环境因素主要是 。
(3)当环境中![]() 浓度小于a时,在图示的3种光强下,该植物呼吸作用产生的
浓度小于a时,在图示的3种光强下,该植物呼吸作用产生的![]() 量 (填“大于”、“等于”或“小于”)光合作用吸收的
量 (填“大于”、“等于”或“小于”)光合作用吸收的![]() 量。
量。
(4)据图可推测,在温室中,若要采取提高![]() 浓度的措施来提高该种植物的产量,还应该同时考虑 这一因素的影响,并采取相应措施。
浓度的措施来提高该种植物的产量,还应该同时考虑 这一因素的影响,并采取相应措施。
31、(7分)现有一批基因型都相同的黄色豌豆种子(黄色、绿色分别由Y和y基因控制,子粒的颜色是子叶表现的性状)。某实验中学生物兴趣小组的同学准备以这些豌豆种子和另一些黄色、绿色的豌豆种子作为实验材料,来探究这些黄色豌豆种子具体的基因型。请你设计一个简便易行的实验方案。
①取所需种子播种并进行苗期管理。
②植株开花时,________________________。
③收集每株植株所结种子进行统计分析。
④实验结果及结论:
a._____________________________________;
b._____________________________________。
32、(15分)下图是某家系甲、乙、丙三种单基因遗传病的系谱图,其基因分别用![]() 、
、![]() 、
、![]() 、
、![]() 和
和![]() 、
、![]() 表示。甲病是伴性遗传病,Ⅱ-7不携带乙病的致病基因。在不考虑家系内发生新的基因突变的情况下,请回答下列问题:
表示。甲病是伴性遗传病,Ⅱ-7不携带乙病的致病基因。在不考虑家系内发生新的基因突变的情况下,请回答下列问题:
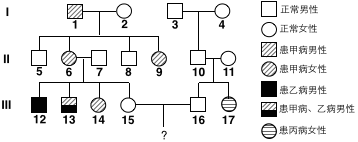
(1)甲病的遗传方式是_____,乙病的遗传方式是_____,丙病的遗传方式是_____,Ⅱ-6的基因型是_____。
(2)Ⅲ-13患两种遗传病的病因是_____。
(3)假如Ⅲ-15为乙病致病基因的杂合子、为丙病致病基因携带者的概率是![]() ,Ⅲ-15和Ⅲ-16结婚,所生的子女只患一种病的概率是_____,患丙病的女孩的概率是_____。
,Ⅲ-15和Ⅲ-16结婚,所生的子女只患一种病的概率是_____,患丙病的女孩的概率是_____。
33、[物理—选修3-3](15分)
(1)(5分)如图为两分子系统的势能![]() 与两分子间距离r的关系曲线。下列说法正确的是(填正确答案标号,选对1个给2分,选对2个得4分,选对3个得5分,每选错1个扣3分,最低得分0分)
与两分子间距离r的关系曲线。下列说法正确的是(填正确答案标号,选对1个给2分,选对2个得4分,选对3个得5分,每选错1个扣3分,最低得分0分)
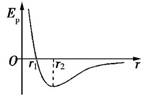 A: 当r大于
A: 当r大于![]() 时,分子间的作用力表现为引力
时,分子间的作用力表现为引力
B: 当r小于![]() 时,分子间的作用力表现为斥力
时,分子间的作用力表现为斥力
C: 当r等于![]() 时,分子间的作用力为零
时,分子间的作用力为零
 D: 在r由
D: 在r由![]() 变到
变到![]() 的过程中,分子间的作用力做负功
的过程中,分子间的作用力做负功
E、在r由![]() 变到
变到![]() 的过程中,分子间的作用力做正功
的过程中,分子间的作用力做正功
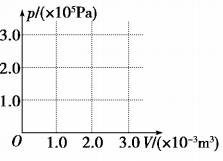
(2)(10分)内壁光滑的导热汽缸竖直浸放在盛有冰水混合物的水槽中,用不计质量的活塞封闭压强为1.0×105Pa、体积为2.0×10-3m3 的理想气体.现在活塞上方缓缓倒上沙子,使封闭气体的体积变为原来的一半,然后将汽缸移出水槽,缓慢加热,使气体温度变为127℃。
(1)求汽缸内气体的最终体积;
(2)在如图所示的p-V图上画出整个过程中汽缸内气体的状态变化。(大气压强为1.0×105Pa)
34、[物理—选修3-4](15分)
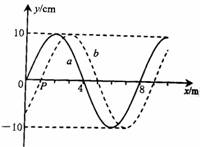 (5分)如图所示,一简谐横波在某区域沿x轴传播,实线a为t=0时刻的波形图线,虚线b为t=△t时刻的波形图线。已知该简谐横波波源振动的频率为f=2.5Hz,虚线b与x轴交点P的坐标为xP=1m。则下列说法正确的是( ) (填正确答案标号,选对1个给2分,选对2个得4分,选对3个得5分,每选错1个扣3分,最低得分0分)
(5分)如图所示,一简谐横波在某区域沿x轴传播,实线a为t=0时刻的波形图线,虚线b为t=△t时刻的波形图线。已知该简谐横波波源振动的频率为f=2.5Hz,虚线b与x轴交点P的坐标为xP=1m。则下列说法正确的是( ) (填正确答案标号,选对1个给2分,选对2个得4分,选对3个得5分,每选错1个扣3分,最低得分0分)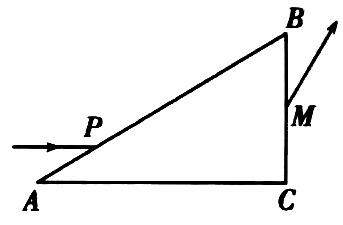 (10分)如图,三棱镜的横截面为直角三角形ABC,∠A=30°,∠B=60°.一束平行于AC边的光线自AB边的P点射入三棱镜,在AC边发生反射后从BC边的M点射出.若光线在P点的入射角和在M点的折射角相等,
(10分)如图,三棱镜的横截面为直角三角形ABC,∠A=30°,∠B=60°.一束平行于AC边的光线自AB边的P点射入三棱镜,在AC边发生反射后从BC边的M点射出.若光线在P点的入射角和在M点的折射角相等,(ⅰ)求三棱镜的折射率;
(ⅱ)在三棱镜的AC边是否有光线透出?写出分析过程.(不考虑多次反射)
35.[选修3------物质结构与性质](15分)
 已知A、B、C、D、E都是元素周期表中前36号的元素,它们的原子序数依次增大。A原子基态时最外层电子数是其内层电子总数的2倍,B原子基态时s电子数与P电子数相等,C在元素周期表的各元素中电负性最大,D的基态原子核外有6个能级且全部充满电子,E原子基态时未成对电子数是同周期元素中最多的。
已知A、B、C、D、E都是元素周期表中前36号的元素,它们的原子序数依次增大。A原子基态时最外层电子数是其内层电子总数的2倍,B原子基态时s电子数与P电子数相等,C在元素周期表的各元素中电负性最大,D的基态原子核外有6个能级且全部充满电子,E原子基态时未成对电子数是同周期元素中最多的。
(1)基态E原子的价电子排布式为 ;
(2)AB32-的立体构型是 ,其中A原子的杂化轨道类型是 。
(3)A22-与B22+互为等电子体,B22+的电子式可表示为 ,1mol B22+中含有的π键数目为 。
(4)用氢键表示式写出C的氢化物水溶液中存在的所有氢键 。
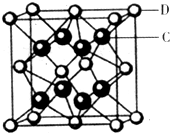
(5)化合物DC2的晶胞结构如图所示,该离子化合协晶体的密度为a g/cm3,则晶胞的体积是 (只要求列算式,阿伏加德罗常数的值为NA)
36.[选修5-------有机化学](15分)
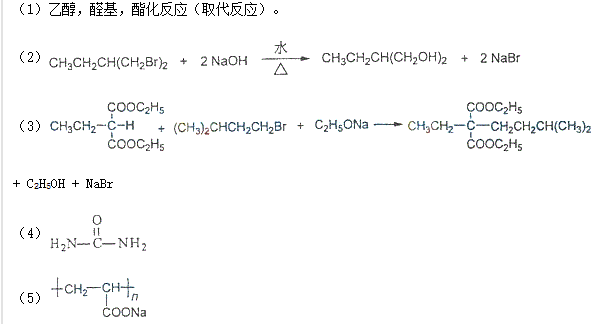
化合物F(异戊巴比妥)是临床常用的镇静催眠药物,其合成路线如下(部分反应条件和试剂略):
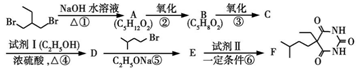
已知:
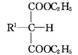 +R2Br+C2H5ONa
+R2Br+C2H5ONa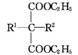 +C2H5OH+NaBr(R1,R2代表烷基)
+C2H5OH+NaBr(R1,R2代表烷基)请回答下列问题:
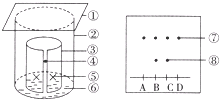
37、生物(选修一)(15分)
图为胡萝卜素粗品的鉴定实验装置示意图,请据图回答下列问题:
化学一模答案
7.B 8.B 9.A 10.C 11.B 12.C 13.C
26(总11分,除了备注,均为2分)
(1)过滤 (2)Al2O3;Al2O3和Fe2O3;Fe2O3;(每空1分)
(3)①Al2O3 + 2OH -=2AlO2-+H2O ②Al3++3NH3·H2O=Al(OH)3↓+3NH4+
(4)答案合理即可
27(总18分,每空2分)
(1)①加硝酸加热溶解固体,再滴加稀盐酸,产生白色沉淀 ②Fe2+
(2)Fe+2Fe3+=3Fe2+②4Fe2++O2+4H+=4Fe3++2H2O 加入KSCN溶液后产生白色沉淀
③0.05 mol·L-1 NaNO3溶液 FeSO4溶液(或FeCl2溶液)
分别取电池工作前与工作一段时间后左侧烧杯中溶液,同时滴加KSCN溶液,后者红色更深
(3)溶液中存在反应:①Fe+2Ag+=Fe2++2Ag ,②Ag++Fe2+=Ag+Fe3+,③Fe+2Fe3+=3Fe2+。反应开始时,c(Ag+)大,以反应①、②为主,c(Fe3+)增大。约30分钟后,c(Ag+)小,以反应③为主,c(Fe3+)减小。
28.(总14分,每空2分)
![]()
![]()
![]()
![]()
35.(总15分,除了备注,均为2分)
(1)3d54s1(2)平面三角形(1分) sp2(3)![]() 2NA
2NA
(4)F-H…F、F-H…O、O-H…F、O-H…O(5)312/aNA cm3
36. (总15分,第3问为3分,其余每空2分,)
高三生物一摸答案
一、选择题(36分)
1—6:B A C D C A
二、非选择题(54分)
1、(8分,一空一分)
(1)![]()
![]()
(2) 图4 卵细胞和极体(第二极体)
(3)4 0 一条染色体的两条染色单体
(4)图5
2、(10分,每空2分)
(1)0、A、B、C
(2)光照强度
(3)大于
(4)光照强度
3、(7分)(1)自交法(1分)
(2)②让其在自然状态下自花受粉(2分)
④ a.若收获的种子全为黄色,则黄色豌豆基因型为YY。(2分)
b.若收获的种子有黄色和绿色,比例近3:1,则黄色豌豆基因型为Yy。(2分)
4、(14分,每空2分)(1)伴![]() 显性 伴
显性 伴![]() 隐性 常染色体隐性
隐性 常染色体隐性 ![]()
(2)Ⅱ-6的初级卵母细胞在减数第一次分裂前期,![]() 和
和![]() 基因发生了交叉互换,使得
基因发生了交叉互换,使得![]() 基因与
基因与![]() 基因在同一条
基因在同一条![]() 染色体上,产生
染色体上,产生![]() 的配子
的配子
(3)![]() (或
(或![]() )
) ![]()
5、(1)纸层析法
(2)防止层析液挥发 石油醚 胡萝卜素溶解在层析液中,使鉴定失败
(3)B和C
(4)把![]() 胡萝卜素分离开,便于鉴定
胡萝卜素分离开,便于鉴定
(5)有机溶剂都是易燃物,直接使用明火加热容易引起燃烧、爆炸
高三一模考试物理参考答案
14. C 15. D 16. C 17. B 18. BD 19. BC 20. AC 21. AD
22.(1)①③⑤⑥⑧⑨(2分);(2) ①0.138(2分); ②1.26(2分);
③计时初时的速度(2分) (2分)
(2分)
23.参考答案:①如图
②1/m ;k/m。
24.解:(1)![]() ,--------1分
,--------1分
![]() ,--------1分
,--------1分
![]() -------2分
-------2分
(2)![]() -------1分
-------1分
![]() --------1分
--------1分
![]() --------2分
--------2分
(3)![]() ---------1分
---------1分
![]() ---------1分
---------1分
![]() -------2分。
-------2分。
25.解:(1)设超声波追上A车的时间为![]() ,此段时间A车的位移
,此段时间A车的位移![]() ,超声波从A车反射回的时间为
,超声波从A车反射回的时间为![]() ,此段时间A车的位移
,此段时间A车的位移![]() 。则:
。则:
![]() --------1分
--------1分
![]() ------2分
------2分
![]() -----1分
-----1分
解得:![]() -----2分
-----2分
![]() ---------1分
---------1分
![]() --------2分
--------2分
位移![]() -----------1分
-----------1分
匀速运动到边境线的时间![]() -----1分
-----1分
B车运动到边境线的时间![]() ------1分
------1分
设B车加速到最大速度的时间![]() , B匀速运动到边境线的时间
, B匀速运动到边境线的时间![]() .
.
![]() ---------------------1分
---------------------1分
![]() --------3分
--------3分
解得![]() ----------1分
----------1分
B车的加速度至少为![]()
![]() -------1分。
-------1分。
33.(1)BCE(共5分)
(2)解:(1)在活塞上方倒沙的过程中温度保持不变,对气体,由玻意耳定律得:p0V0=p1V1,(2分)
p1=2.0×105Pa;(1分)
设最终体积为V2,在缓慢加热到127℃的过程中,气体压强保持不变,由盖•吕萨克定律得:

![]() =
=![]() ,(2分)
,(2分)
所以V2=1.47×10-3m3;(1分)
(2)整个过程中汽缸内气体的状态变化,如下图所示:
(4分)
34.
参考答案
(1)ACE
解:
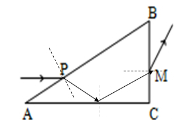 作出光路图如图所示.画图(2分)
作出光路图如图所示.画图(2分)
光线在AB面上的入射角为i=60°.因为光线在P点的入射角和在M点的折射角相等.知光线在AB面上的折射角等于光线在BC面上的入射角.根据几何关系知,光线在AB面上的折射角为r=30°.
根据n=![]() (3分)
(3分)
光线在AC面上的入射角为60°.sinC=![]() =
=![]() (3分)
(3分)
因为sin60°>sinC,光线在AC面上发生全反射,无光线透出.(2分)
