
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mg-24 S-32 K-39 Ca-40 Cu-64 Y-89 Ba-137
7.下列叙述中正确的是( )
A.由乙酸和乙醇生成乙酸乙酯的反应类型和由溴乙烷生成乙烯的反应类型相同
B.糖类、油脂和蛋白质均能发生水解反应
C.丙烯在一定条件下可与氯气发生取代反应生成3-氯丙烯
D.甲苯与氯气在光照下发生取代反应主要生成2,4二氯甲苯
8. 设NA为阿伏加德罗常数的值,下列说法正确的是( )
B.含有0. 1 mol NH4+的氨水中,含有OH-的数目为0.1NA
C. 标准状态下,33.6 L氟化氢中含有1.5 NA个氟化氢分子
D. 30 g乙酸和乙酸乙酯的混合物完全燃烧,消耗O2的分子数目为NA
9. 短周期原子序数依次增大的主族元素R、T、Q、W、Y、Z具有如下信息:①R、Y原子的最外层电子数与电子层数相同;②Q是地壳中含量最高的元素,R与T的核电荷数之和等于Q的核电荷数;③W与R同主族,Z与Q同主族。下列说法正确的是( )
A.Q与Y组成的常见物质是一种两性物质,能与氨水反应
B.已知WRZQ3溶液呈酸性,若将WRZQ3固体溶于水,能促进水的电离
C.元素Q与W形成的两种常见化合物中含有相同比例的阴、阳离子
D.元素T、Q、W、Y的原子半径大小为T
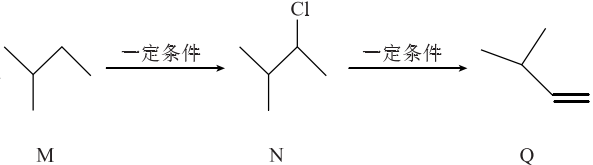
10. 有机物M、N、Q的转化关系如下图所示,下列说法正确的是( )
11.现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(![]() ),其原理如下图所示,下列说法正确的是( )
),其原理如下图所示,下列说法正确的是( )
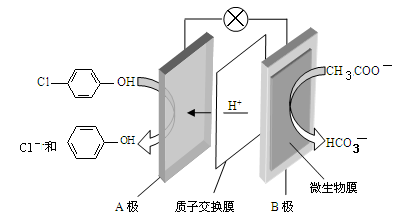
A.A极的电极反应式为![]() + e-=Cl-+
+ e-=Cl-+![]()
B.当外电路中有0.2mole-转移时,A极区增加的H+的个数为0.1NA
C.电流方向从B极沿导线经小灯泡流向A极
D.B为电池的正极,发生还原反应
12. 下列操作、现象和所得结论不正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 分别向2.0mL 0.1mol/LCH3COOH溶液和2.0mL 0.1mol/LH3BO3溶液中滴加等浓度的NaHCO3溶液,前者有气泡产生,后者无明显现象 | 酸性:CH3COOH>H2CO3>H3BO3 |
| B | 在酒精灯上分别加热打磨和未打磨的铝箔,现象都是铝箔熔化不滴落 | 铝能被氧气氧化成氧化铝 且熔点:氧化铝>铝 |
| C | 加热盛有浓硫酸和可抽动铜丝的试管,并将产生的气体通入到品红溶液中,观察到品红溶液褪色,试管中产生蓝色溶液 | 浓硫酸具有强氧化性 |
| D | 向漂白粉中加入较浓的盐酸,并将湿润的淀粉碘化钾试纸置于试管口,观察到产生气泡,试纸未变蓝 | 漂白粉已经失效 |
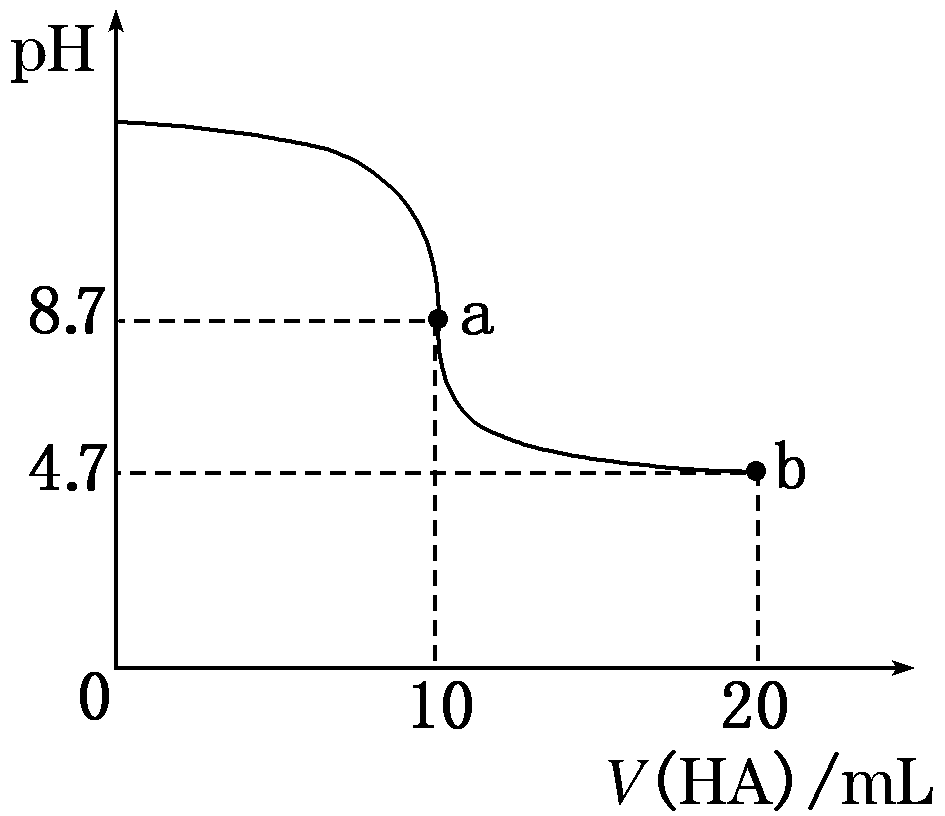 13. 室温下向10 mL 0.1 mol·L-1 NaOH溶液中加入 0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )
13. 室温下向10 mL 0.1 mol·L-1 NaOH溶液中加入 0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )
A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度:a >b,且a点所示溶液中
由水电离出的c(OH-)=10-8.7mol/L
C.pH=7时溶液中c(HA)>c(Na+)=c(A-)>c(H+)=c(OH-)
D.b点所示溶液中c(A-)>c(HA)
26.(14分)氮化钙(Ca3N2)是一种重要的化学试剂,通常条件下为棕色易水解的固体。某小组在实验室制备氮化钙并测定其纯度,设计如下实验(夹持装置略去):
Ⅰ. 氮化钙的制备。
(1)加热条件下,钙和氮气制备氮化钙的反应方程式为 。
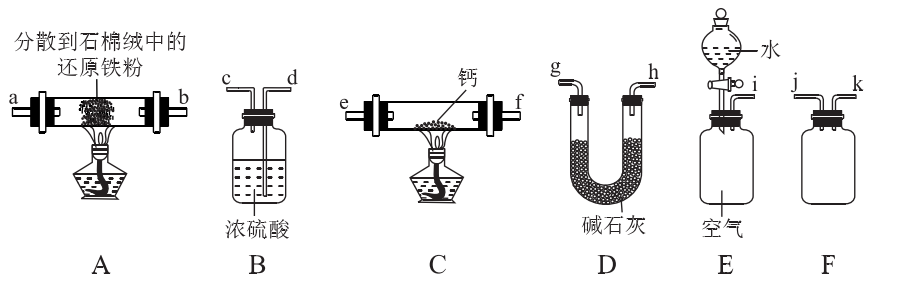
(2)按气流由左到右的方向,上述装置合理的连接顺序为i- -e-f-
(填仪器接口字母)。
(3)按连接好的装置进行实验。
①实验步骤如下:检查装置气密性、加入药品、点燃装置A处酒精灯、
、熄灭装置A处酒精灯(请按正确顺序填入下列步骤的字母标号)
a.点燃装置C处酒精灯,反应一段时间 b.打开分液漏斗活塞
c.熄灭装置C处酒精灯 d. 关闭分液漏斗活塞
②装置B的作用为
③装置C的硬质玻璃管中的现象为
(4)设计实验证明Ca3N2中混有钙单质:
Ⅱ.测定氮化钙纯度。
i.称取4.0g反应后的固体,加入足量水,将生成的气体全部蒸出并通入100. 00 mL 1.00 mol /L的盐酸中,充分反应后,将所得溶液稀释到200.00 mL;
ii.取20.00 mL稀释后的溶液,用0.2 mol /LNaOH标准溶液滴定过量的盐酸,到终点时消耗标准溶液25. 00 mL。
(5)所取固体中氮化钙的质量分数为 。
27.(14分)石棉尾矿主要含有Mg3(Si2O5)(OH)4和少量的Fe2O3、Al2O3。以石棉尾矿为镁源制备碳酸镁晶体(MgCO3·nH2O)的工艺如下:
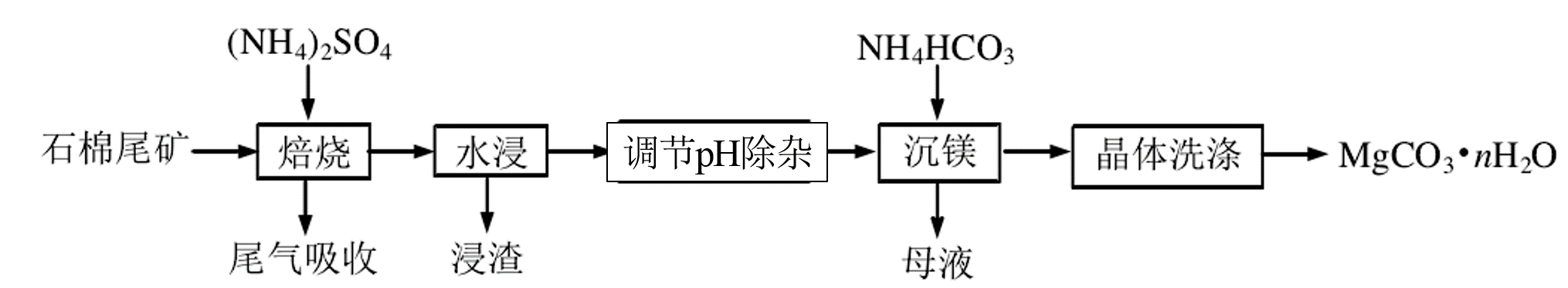
已知“焙烧”过程中的主反应为:
![]()
(1)写出焙烧产物NH3的电子式 。
(2)为提高水浸速率,可采取的措施为 (任写一条),“浸渣”的主要成分为 。
(3)“调节pH除杂”时,需将pH调至5.0,则除去的杂质离子是,此时溶液中的c(Fe3+)=(已知Ksp[Fe(OH)3]=4.0×10-38)。
(4)“沉镁”过程中反应的离子方程式为 。
“沉镁”时若温度超过60℃,将产生较多的碱式碳酸镁杂质,原因是
(5)流程中可以循环利用的物质是 (填化学式)。
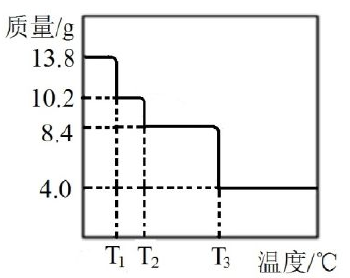
(6)某小组同学称取13.8g MgCO3·nH2O进行热重分析,并绘制剩余固体质量随温度变化的曲线如图所示,则n= 。
28.(15分)乙二醛(OHC—CHO)是一种重要的精细化工产品。
Ⅰ. 工业生产乙二醛
(1)乙醛(CH3CHO)液相硝酸氧化法
在Cu(NO3)2催化下,用稀硝酸氧化乙醛制取乙二醛,反应的化学方程式为 。该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点是。
(2)乙二醇(HOCH2CH2OH)气相氧化法
①已知:OHC—CHO(g) +2H2(g)![]() HOCH2CH2OH(g) △H=−78kJ·mol−1K1
HOCH2CH2OH(g) △H=−78kJ·mol−1K1
2H2(g) + O2(g)![]() 2H2O(g) △H=−484kJ·mol−1K2
2H2O(g) △H=−484kJ·mol−1K2
乙二醇气相氧化反应HOCH2CH2OH(g) +O2(g)![]() OHC—CHO(g) + 2H2O(g)的△H=
OHC—CHO(g) + 2H2O(g)的△H=
kJ·mol−1。相同温度下,该反应的化学平衡常数K=(用含K1、K2的代数式表示)。
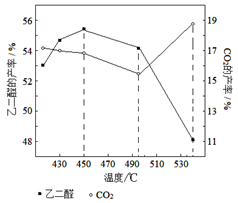
②当原料气中氧醇比为1.35时,乙二醛和副产物CO2的产率与反应温度的关系如下图所示。反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是 、 。
Ⅱ. 乙二醛电解氧化制备乙醛酸(OHC—COOH)的生产装置如下图所示,通电后,阳极产生的Cl2与乙二醛溶液反应生成乙醛酸。
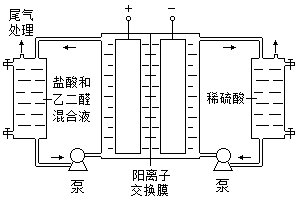
(3)阴极反应式为。$来&源:
(4)阳极液中盐酸的作用,除了产生氯气外,还有。
(5)保持电流强度为aA,电解tmin,制得乙醛酸m g,列式表示该装置在本次电解中的电流效率η= 。
(已知:法拉第常数为fC•mol−1;η=![]() )
)
35.[化学——选修3:物质结构与性质](15分)
砷、镓和铜均为重要的合金材料,在工业生产和科研领域均有重要应用。
请回答下列问题:
(1)基态Ga原子中有 种能量不同的电子,其价电子排布图为
(2)GaAs的晶胞与金刚石相似,其中As原子位于晶胞的顶点和面心,则GaAs晶体中存在的化学键类型为 ,Ga、Ge、As、Se四种基态原子的第一电离能由大到小的顺序为
(3)Cu3(AsO4)2是一种木材防腐剂。其阴离子中As原子的杂化轨道类型为$来&源:
H3AsO4的酸性强于H3AsO3的原因为 。
(4)[Cu(NH3)4]SO4是一种重要的配合物。与SO42-互为等电子体的分子的化学式为
(任写一种)。一定压强下,将NH3和PH3的混合气体降温,首先液化的为
(5)晶胞有两个基本要素:
①原子坐标参数:表示晶胞内部各原子的相对位置。一种钇钡铜氧晶体的晶胞结构如图所示,其中原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为 。
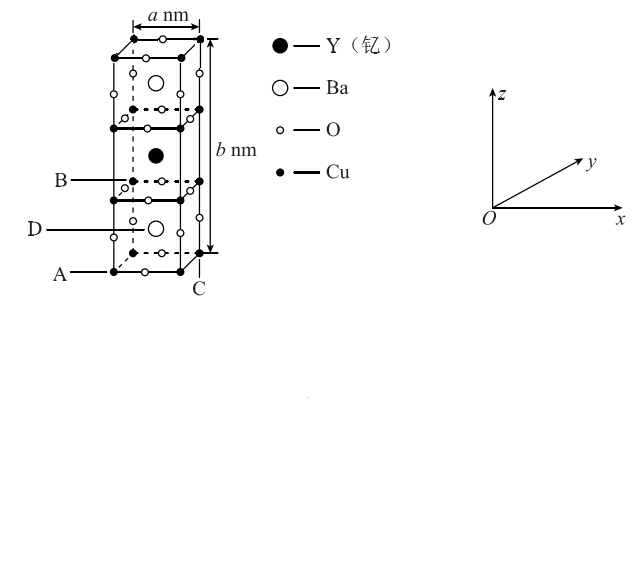
②晶胞参数:描述晶胞的大小和形状。
已知:该钇钡铜氧晶体的晶胞参数分别为anm、bnm(如图所示),阿伏加德罗常数的值为NA,其密度为 g/cm3(列出计算式即可)。
36. [化学——选修5:有机化学基础](15分)$来&源:
有机高分子化合物M的一种合成路线如下:
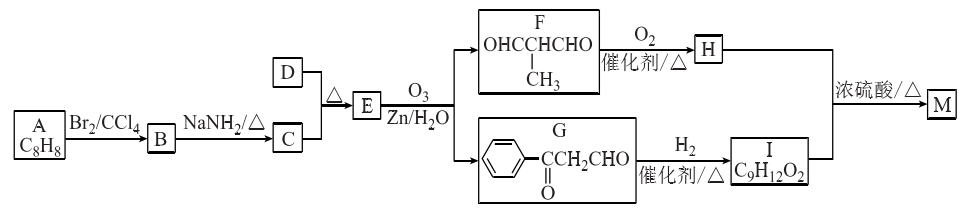
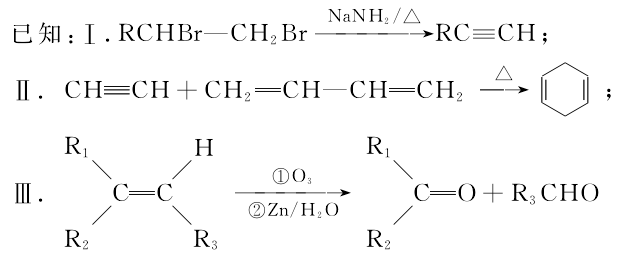
请回答下列问题:
(1)A的化学名称为 ,F中所含官能团的名称为 。
(2)C+D→E的反应类型为
(3)B的结构简式为 ,C的分子中最多有 个原子在同一直线上。
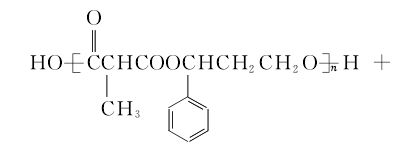
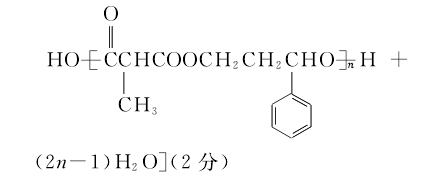
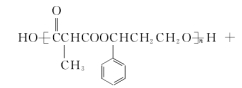
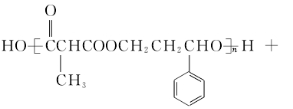
(4)H+I→M的化学方程式为
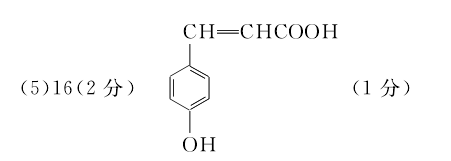
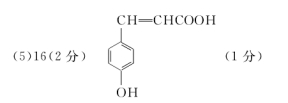
(5)在催化剂、加热条件下,G与氧气反应生成Q(C9H8O3),同时满足下列条件的Q的同分异构体有 种(不考虑立体异构),其中核磁共振氢谱有6组吸收峰的结构简式为
①除苯环外不含其他环状结构 ②能与FeCl3溶液发生显色反应
③能与NaHCO3溶液反应生成CO2
(6)参照上述合成路线和相关信息,以甲醇和一氯环己烷为有机原料(无机试剂任选),设计制备己二酸二甲酯的合成路线:
。
7~13:CACBBCD
26.(14分)
![]()
(2)gh(或hg) ab(或ba)、 jk(或kj)dc(2分)
(3)① bacd (2分)
②防止外界空气进入装置C,使Ca3N2变质(2分,其他合理答案也给分)
③银自色金属逐渐变为棕色(2分)
(4)取混合物少量于洁净试管中,加入适量稀盐酸,将生成的气体净化后,通入灼热的CuO,黑色固体变红,则Ca3N2中混有钙单质(或取混合物少量于洁净试管中,加入适量水,将生成的气体通过足量浓硫酸,再通入灼热的CuO,黑色固体变红,则Ca3N2中混有钙单质)(2分,其他合理答案也给分)
(5)92. 5%(2分)
27.(14分)
(1)(1分)
(2)将焙烧渣粉碎或加热或搅拌(1分),SiO2(1分)
(3)Fe3+、Al3+(2分);4.0×10-11mol/L(2分)
(4)Mg2++2HCO+(n1)H2O=MgCO3•nH2O↓+CO2↑(2分),升温促进Mg2+部分水解或升温促进Mg2+水解(2分)
(5)(NH4)2SO4(1分,填名称不得分,多写H2O不扣分)
(6)3(2分)
28.(15分)(1)3CH3CHO + 4HNO3![]() 3OHC—CHO + 4NO↑+ 5H2O(2分)
3OHC—CHO + 4NO↑+ 5H2O(2分)
尾气有污染(或“腐蚀设备”等其他合理答案)(1分)
(2)① − 406(2分) K2/K1(2分)
② 温度升高,主反应平衡向逆反应方向移动(1分)
温度大于495℃,乙二醇大量转化为CO2等副产物(1分)
(3)2H+ + 2e- = H2↑(2分)
(4)增强导电性(或“平衡阴极区电解液电荷”等其他合理答案) (2分)
(5)mf/2220at×100%(2分)
35.[化学——选修3:物质结构与性质](15分)
(1)8(2分) (Ga的价电子排布图) (1分)
(2)共价键、配位键(2分) As> Se> Ge> Ga( 2分)
(3)sp3(1分) H3AsO4非羟基氧原子多,As的正电性更高,羟基中的O原子的电子向As偏移程度大,更容易电离出H+(2分)
(4)CCl4(或SiCl4或CBr4或SiF4等)(1分), NH3(1分),
(5)①(1/2,1/2,1/2)(1分)
![]()
36. [化学——选修5:有机化学基础](15分)
(1)苯乙烯(1分) 醛基(1分)
(2)加成反应(1分)
![]() (2分)
(2分)
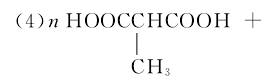
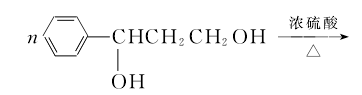
![]()
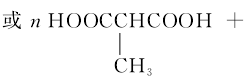
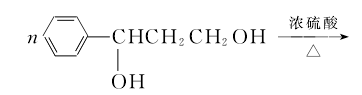
![]()
![]()
![]()
![]()
![]()
答题纸
26.(14分)
(1) 。
(2) 、
(3)①
②
③
(4)
(5)
27.(14分)
(1)
(2) 、 。
(3)、
(4)
(5)
(6)
28.(15分)
(1)
(2)① 、
② 、
(3)
(4)
(5)
陕西师大附中高2017届高三模考理综答案
化学
7~13:CACBBCD
26.(14分)
![]()
(2)gh(或hg) ab(或ba)、 jk(或kj)dc(2分)
(3)① bacd (2分)
②防止外界空气进入装置C,使Ca3N2变质(2分,其他合理答案也给分)
③银自色金属逐渐变为棕色(2分)
(4)取混合物少量于洁净试管中,加入适量稀盐酸,将生成的气体净化后,通入灼热的CuO,黑色固体变红,则Ca3N2中混有钙单质(或取混合物少量于洁净试管中,加入适量水,将生成的气体通过足量浓硫酸,再通入灼热的CuO,黑色固体变红,则Ca3N2中混有钙单质)(2分,其他合理答案也给分)
(5)92. 5%(2分)
27.(14分)
(1)H..N..N:H(1分)
(2)将焙烧渣粉碎或加热或搅拌(1分),SiO2(1分)
(3)Fe3+、Al3+ (2分) ;4.0×10-11mol/L(2分)
(4)Mg2++2HCO-+(n-1)H2O=MgCO3•nH2O↓+CO2↑(2分),升温促进Mg2+部分水解或升温促进Mg2+水解(2分)
(5)(NH4)2SO4(1分,填名称不得分,多写H2O不扣分)
(6)3(2分)
28.(15分)(1)3CH3CHO + 4HNO3![]() 3OHC—CHO + 4NO↑+ 5H2O(2分)
3OHC—CHO + 4NO↑+ 5H2O(2分)
尾气有污染(或“腐蚀设备”等其他合理答案)(1分)
(2)① − 406(2分) K2/K1(2分)
② 温度升高,主反应平衡向逆反应方向移动(1分)
温度大于495℃,乙二醇大量转化为CO2等副产物(1分)
(3)2H+ + 2e- = H2↑(2分)
(4)增强导电性(或“平衡阴极区电解液电荷”等其他合理答案) (2分)
(5)mf/2220at×100%(2分)
35.[化学——选修3:物质结构与性质](15分)
(1)8(2分) (Ga的价电子排布图) (1分)
(2)共价键、配位键(2分) As> Se> Ge> Ga( 2分)
(3)sp3(1分) H3AsO4非羟基氧原子多,As的正电性更高,羟基中的O原子的电子向As偏移程度大,更容易电离出H+(2分)
(4)CCl4(或SiCl4或CBr4或SiF4等)(1分), NH3(1分),
(5)①(1/2,1/2,1/2)(1分)
![]()
36. [化学——选修5:有机化学基础](15分)
(1)苯乙烯(1分) 醛基(1分)
(2)加成反应(1分)
![]() (2分)
(2分)
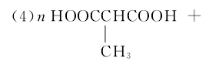
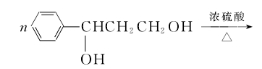
![]()
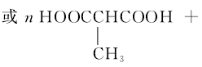
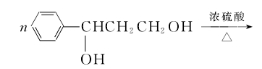
![]()
![]()
![]()
![]()
![]()