
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
武功县2016届高三摸底考试试题(化学)
注意事项:本试卷分第I卷(选择题)和第II卷(非选择题)两部分,总分100分,考试时间90分钟。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Cu-64
第I卷(选择题,共42分)
一、选择题(本题共14小题,每小题3分,共42分。只有一个选项符合题意。)
1.化学与人类生活、生产和社会可持续发展密切相关,下列说法正确的是( )
A.为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
B.采取“静电除尘”“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量
C.铝及其合金是电气、工业等广泛使用的材料,是因为铝的冶炼方法比较简单
D.化学药品着火,都要立即用水或泡沫灭火器灭火
2.下列说法正确的是 ( )
A.电解法精炼铜,当阴极质量增加32 g时,一定有6.02×1023个电子转移
B.含10.6 g Na2CO3的溶液中,所含阴离子总数等于6.02×1022
C.28 g由乙烯和氮气组成的混合气体中,含有6.02×1023个原子
D.含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为6.02×1022
3.能正确表示下列反应的离子方程式 ( )
A.向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32-
B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓
C.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2 + 2Fe3+ = 2Fe(OH)3 + 3Mg2+
D.NaHCO3溶液与稀H2SO4反应:CO32-+ 2H+ = H2O + CO2↑
4.在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量的锌粉,首先置换出的是
( )
5.已知某有机物X的结构简式为:下列有关叙述不正确的是 ( )
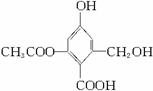
A.X的化学式为C10H10O6B.X在一定条件下能与FeCl3溶液发生显色反应
C.1molX分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3 mol、4 mol、1 mol
D.X在一定条件下能发生消去反应和酯化反应
6.原子序数依次增大的X、Y、Z、R、W、T六种前20号元素,X、Y原子的最
外层电子数与其电子层数相等,Y、T位于同族,R最外层电子数是次外层的3
倍,W无正价,甲的化学式为ZX3,是一种刺激性气味的气体,乙是由X、Z、
W组成的盐。下列说法正确的是 ( )
A.由X、Z、W组成盐的水溶液呈酸性,则溶液中该盐阳离子浓度小于酸根离
子浓度
B.气态氢化物的稳定性:W
C.原子半径:W
D.ZR2、TR2两化合物中R的化合价相同
7.下列说法正确的是: ( )
A.将pH均为a的氢氧化钠溶液和氨水分别加水稀释100倍,pH变为b和c,则a、b、c的大小关系是:b>c>a
B.常温下5.0×10-3mol·L-1KHA溶液的pH=3.75 ,该溶液中c(A2-)< c(H2A)
C.室温时,M(OH)2(s)![]() M2+(aq)+2OH-(aq) Ksp=a; c(M2+)=b mol·L-1时,溶液的pH等于14+
M2+(aq)+2OH-(aq) Ksp=a; c(M2+)=b mol·L-1时,溶液的pH等于14+![]()
![]()
![]()
D.Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4)
8.对下列实验装置的描述正确的是 ( )
① ② ③ ④
A.①可用于制备并收集少量NO2B.②不能用于制备并收集少量Cl2
C.③可用于配制150 mL 0.10 mol/L盐酸 D.④可用于实验室制NH3
9. 有机物![]() 的一氯代物可能的结构有(不考虑立体异构)( )
的一氯代物可能的结构有(不考虑立体异构)( )
A.6种 B.8种 C.11种 D.15种
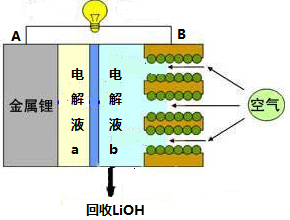 10锂空气电池放电时的工作原理如图所示。下列叙述正确的是: ( )
10锂空气电池放电时的工作原理如图所示。下列叙述正确的是: ( )
A.放电时Li+由B极向A极移动
B.电池放电反应为4Li + O2+ 2H2O = 4LiOH
C.正极反应式为O2 + 4H+ + 4e- = 2H2O
D.电解液a可以为LiCl溶液
11.工业上制氢气的一个重要反应是:CO(g) + H2O(g) ⇌ CO2(g) + H2(g) △H
已知:C(石墨) + 1/2O2(g) = CO(g) △H1 ;H2(g) + 1/2O2(g) = H2O(g) △H2
C(石墨) + O2(g) = CO2(g) △H3 ,则下列说法正确的是 ( )
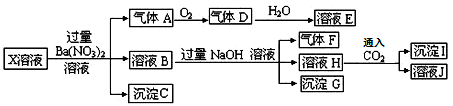 若干种,现取X溶液进行连续实验,实验过程及产物如下:下列说法正确的是( )
若干种,现取X溶液进行连续实验,实验过程及产物如下:下列说法正确的是( )C. 升高温度同时充入N2 D. 降低温度同时增大压
第Ⅱ卷 ( 非选择题 共58分)
二、非选择题(包括必考题和选考题两部分。第15题~第17题为必考题,每个试题考生都必须做答。第18题~第20题为选考题,考生选其中一题作答)
(一)必考题(共3题,共43分)
15、(14分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。回答下列问题:
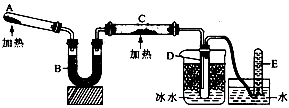
(1)A中加入的物质是___________,发生反应的化学方程式是_____________;
(2)B中加入的物质是___________,其作用是_____________________;
(3)实验时在C中观察到得现象是_________,发生反应的化学方程式是______;
(4)实验时在D中观察到得现象是_________, D中收集到的物质是_______,检验该物质的方法和现象是__________________________________。
16、(14分)我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法.
I. 已知:2CO(g)+ O2(g)=2CO2(g),ΔH=-566 kJ·mol-1
2Fe(s)+![]() O2(g)=Fe2O3(s),ΔH=-825.5 kJ·mol-1
O2(g)=Fe2O3(s),ΔH=-825.5 kJ·mol-1
反应:Fe2O3(s)+ 3CO(g) ![]() 2Fe(s)+ 3CO2(g),ΔH=______ kJ·mol-1.
2Fe(s)+ 3CO2(g),ΔH=______ kJ·mol-1.
Ⅱ.反应![]() Fe2O3(s)+ CO(g)
Fe2O3(s)+ CO(g) ![]()
![]() Fe(s)+ CO2(g)在1000℃的平衡常数等于4。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过l0min后达到平衡.
Fe(s)+ CO2(g)在1000℃的平衡常数等于4。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过l0min后达到平衡.
(1)CO的平衡转化率=____________.
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是________.
a.提高反应温度 b.增大反应体系的压强 c.选取合适的催化剂
d.及时吸收或移出部分CO2e.粉碎矿石,使其与平衡混合气体充分接触
Ⅲ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:
CO(g)+2H2(g)![]() CH3OH(g).请根据图示回答下列问题:
CH3OH(g).请根据图示回答下列问题:
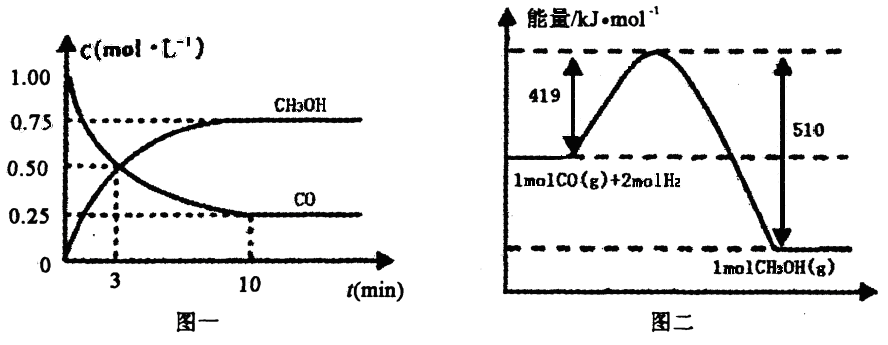
(1)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=________.
(2)若在温度和容器相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表:
| 容器 | 反应物投入的量 | 反应物的 转化率 | CH3OH的 浓度 | 能量变化 (Q1、Q2、Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1kJ热量 |
| 乙 | 1mol CH3OH | α2 | c2 | 吸收Q2kJ热量 |
| 丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3kJ热量 |
则下列关系正确的是________.
A. c1=c2B.2Q1=Q3 C. 2α1=α3 D. α1+α2=1
E. 该反应若生成1mol CH3OH,则放出(Q1+Q2)kJ热量
(3)若在一体积可变的密闭容器中充入l mol CO、2mol H2和1mol CH3OH ,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则该反应向______(填“正”、“逆”)反应方向移动.
(4)甲醇可与氧气构成燃料电池,该电池用多孔的惰性电极浸入浓氢氧化钾溶液,写出该电池的负极反应式__________________ 。
17、(15分)重金属元素铬的毒性较大,含铬废水需经处理达标后才能排放。
Ⅰ.某工业废水中主要含有Cr3+,同时还含有少量的Fe3+、Al3+、Ca2+和Mg2+等,且酸性较强。为回收利用,通常采用如下流程处理:
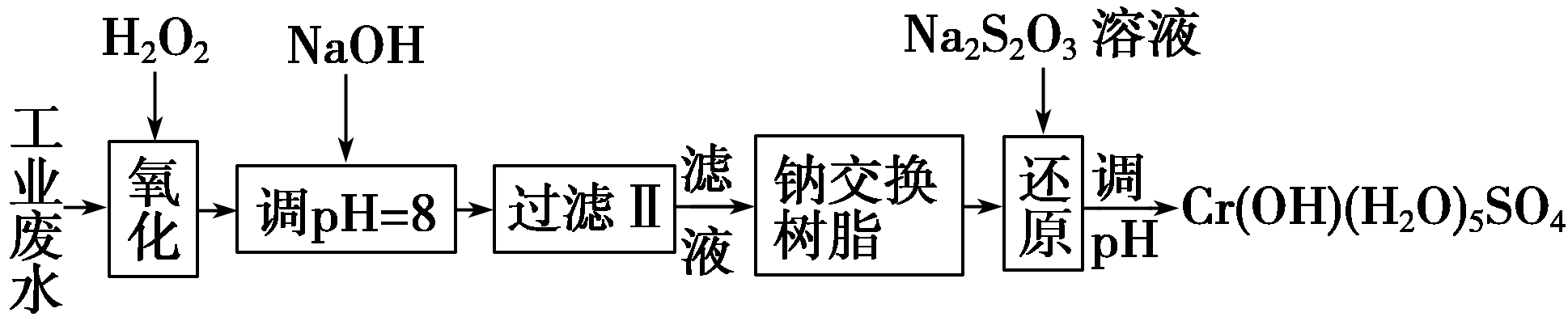
注:部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见下表。
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9溶解) |
(1)氧化过程中可代替H2O2加入的试剂是________(填序号)。
A.Na2O2B.HNO3C.FeCl3D.KMnO4
(2)加入NaOH溶液调整溶液pH=8时,除去的离子是________;已知钠离子交换树脂的原理:Mn++nNaR―→MRn+nNa+,此步操作被交换除去的杂质离子是__________。
A.Fe3+B.Al3+C.Ca2+D.Mg2+
(3)还原过程中,每消耗0.8molCr2O转移4.8 mol e-,该反应离子方程式为
_____________________________________________。
Ⅱ.酸性条件下,六价铬主要以Cr2O72-形式存在,工业上常用电解法处理含Cr2O72-的废水:该法用Fe作电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3溶液. (1)电解时能否用Cu电极来代替Fe电极?________(填“能”或“不能”),理由是__________________________________。
(2)电解时阳极附近溶液中Cr2O转化为Cr3+的离子方程式为__________________。
(3)常温下,Cr(OH)3的溶度积Ksp=1×10-32,溶液的pH应为___________时才能使c(Cr3+)降至10-5mol·L-1。
(二)选考题(考生选其中一题作答)
18. [化学——选修2:化学与技术](15分)
水是一种重要的自然资源,是人类赖以生存不可缺少的物质,水质优劣直接影响人体健康。请回答下列问题:
M2+(金属离子)+EBT-(铬黑T)===MEBT+
蓝色 酒红色
M2+(金属离子)+Y4-(EDTA)===MY2-
MEBT++Y4-(EDTA)===MY2-+EBT-(铬黑T)
实验过程:①取地下水样品25.00mL进行预处理。写出由Mg2+引起的暂时硬度的水用加热方法处理时所发生反应的化学方程式:____________________。
②预处理的方法是向水样中加入浓盐酸,煮沸几分钟,煮沸的目的是
___________________________________________________________。
③将处理后的水样转移到250mL的锥形瓶中,加入氨水—氯化铵缓冲溶液调节pH为10,滴加几滴铬黑T溶液,用0.010mol·L-1的EDTA标准溶液进行滴定。滴定终点时共消耗EDTA溶液15.00mL,则该地下水的硬度为________。
(3)某工业废水中含有CN-和Cr2O72-等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:
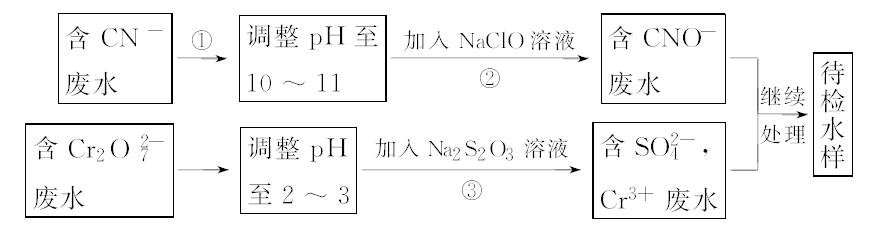
回答下列问题:
①流程②中,反应后无气体放出,该反应的离子方程式为_______。
②含Cr3+废水需进一步处理,请你设计一个处理方案:___________________________________________________________________________________________。
19.[化学——选修3:物质结构与性质](15分)
第ⅢA、ⅤA族元素组成的化合物AlN、AlP、AlAs等是人工合成的半导体材料,它们的晶体结构与单晶硅相似,与NaCl的晶体类型不同。
(1)核电荷数比As小4的原子基态的电子排布式为____________________。
(2)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有____种。
(3)NCl3中心原子杂化方式为__________,NCl3的空间构型为__________。
(4)在AlN晶体中,每个Al原子与_____个N原子相连,AlN属于________晶体。
(5)设NaCl的摩尔质量为Mrg·mol-1,食盐晶体的密度为ρg·cm-3,阿伏加德罗常数的值为NA。食盐晶体中两个距离最近的钠离子中心间的距离为______cm。
20.[化学——选修5:有机化学基础](15分)
某些有机化合物之间具有如下转化关系:
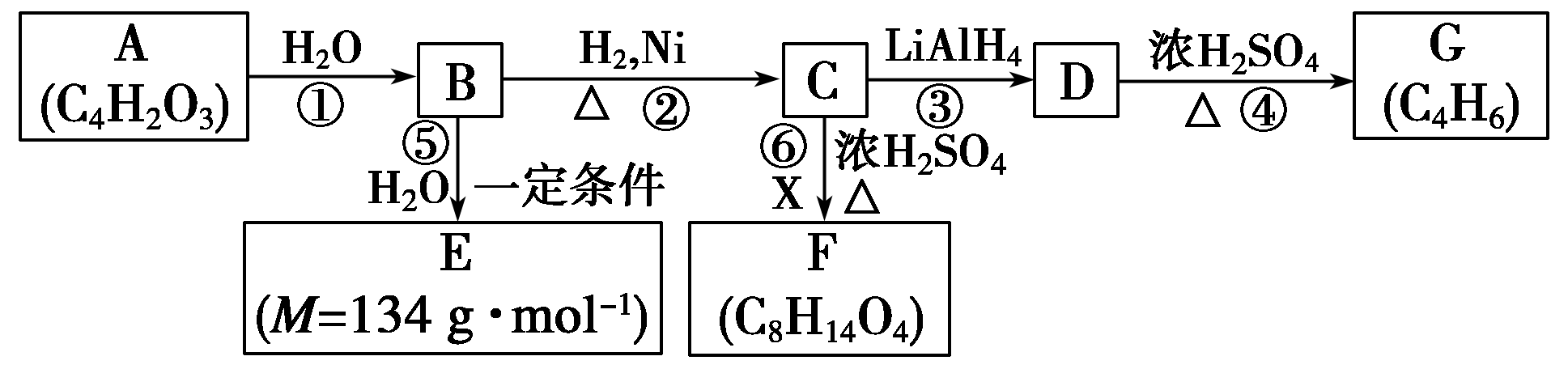
其中:A是一种五元环状化合物,其分子中只有一种化学环境的氢原子;F核磁共振氢谱显示有三种不同化学环境的氢原子,且峰面积之比为2∶2∶3;G是合成顺丁橡胶的主要原料。
已知:①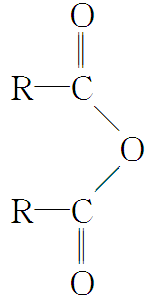 2RCOOH(其中R是烃基)
2RCOOH(其中R是烃基)
②R—COOH R—CH2OH(其中R是烃基)
武功县2016届高三摸底考试答题纸(化学)
班级 姓名 考号 学校 -_________________
选择题(每题只有一个选项正确,每题3分,共42分。)| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 答案 | |||||||
| 题号 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| 答案 |
②___________________________(2分)③_______________________(4分)
(3)①_______________________________________(2分)
②________________________________________________________(2分)
19.[化学——选修3:物质结构与性质](15分)
Ⅱ.(1)不能(2分) 因阳极产生的Cu2+不能使Cr2O还原到低价态(1分)
(2)Cr2O+6Fe2++14H+===2Cr3++6Fe3++7H2O(2分)
(3)5(2分)
选做题:
18. [化学——选修2:化学与技术](15分)
20.[化学——选修5:有机化学基础](15分)
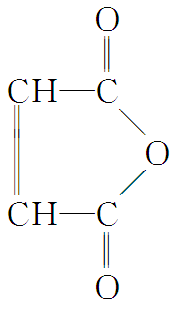
(1)
(2分)
(2)碳碳双键、羧基(2分)
(3)还原反应(2分) 消去反应(2分)
(4)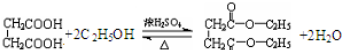
(2分)
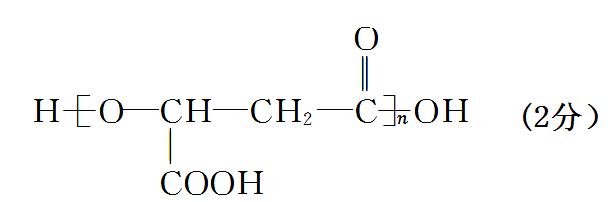 (5)
(5)
2(3分)