
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
宁夏六盘山高级中学
2017届高三年级第二次模拟测试卷
学科:理综 化学
相对原子质量:H—1C—12N—14O—16Al—27P—31S—32Cl—35.5
Fe—56Cu—64Zn—65Pb—207资*源%库
7.化学是一门实用性很强的科学,与社会、环境等密切相关。下列说法错误的是
A.用CO2合成可降解的聚碳酸酯塑料,能减少白色污染及其危害
B.用含橙色酸性重铬酸钾的仪器检验酒驾,利用了乙醇的挥发性和还原性
C.浸泡过高锰酸钾溶液的硅藻土放于新鲜的水果箱内是为了催熟水果
D.“煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气
8.NA代表阿伏加德罗常数的值。下列叙述正确的是
A.0.1 mol的白磷(P4)或甲烷中所含的共价键数均为0.4NA
B.将1 mol Cl2通入水中,HC1O、Cl-、ClO-粒子数之和为2NA
C.6.4 g由S2、S4、S8组成的混合物含硫原子数为0.2NA
D.密闭容器中2 mol NO与1 mol O2充分反应后,产物的分子数为NA
9.三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+ 5H2O == 2NO + HNO3+ 9HF.下列有关该反应的说法正确的是()资*源%库 资*源%库
A.NF3是氧化剂,H2O是还原剂
B.还原剂与氧化剂的物质的量之比为2:1
C.若生成0.2 mol HNO3,则转移0.2 mol电子
D.NF3在潮湿的空气中泄漏会产生红棕色气体
10.下列实验方案设计中,不能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 验证乙烯与溴发生加成反应 | 乙烯通入溴水中,测定反应前后溶液pH |
| B | 检验氯化铁溶液中是否含FeCl2 | 向氯化铁溶液中滴加铁氰化钾溶液 |
| C | 检验乙酸中是否混有乙醇 | 取样液于试管,加入一绿豆颗粒大的钠粒 |
| D | 验证Ksp(AgI)<Ksp(AgCl) | 向含等物质的量NaCl、KI的混合液中滴加AgNO3溶液 |
11.以铅蓄电池为电将CO2转化为乙烯的装置如图所示,电解所用电极材料均为惰性电
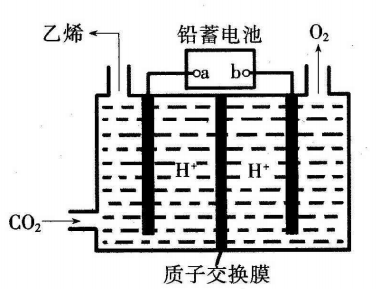 极。下列说法不正确的是
极。下列说法不正确的是
A.b为铅蓄电池的正极
B.电解过程中,阳极区溶液中c(H+)逐渐减小
C.阴极反应式:2CO2+ 12H++12e-== C2H4+ 4H2O
D.每生成1mol乙烯,理论上铅蓄电池中消耗12mol硫酸
12.下列图示与对应的叙述相符的是 ( )
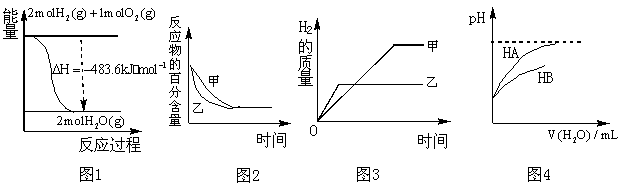
A.图1表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJ·mol-1
B.图2表示压强对反应2A(g)+2 B(g)![]() 3C(g)+D(S)的影响,乙的压强比甲的压强大
3C(g)+D(S)的影响,乙的压强比甲的压强大
C.图3表示等质量的钾、钠分别与足量水反应,则甲为钠
D.图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH
13.中学常见无机物A、B、C、D、E、X均由短周期元素组成,且存在如下图转化关系(部分反应物、生成物和反应条件略去)。下列推断不正确的是
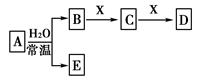
A.若X是Na2SO3,C是能使品红溶液褪色的气体,则A可能是氯气,且D和E不反应
B.若A是单质,B和D的反应是OH-+ HCO3—=H2O+CO32-则E-定能还原CuO
C.若B、X均为单质,D为CO,C能和E反应,则E为NaOH
D.若D为白色沉淀,且与A的摩尔质量相等,则X-定是铝盐
资*源%库
26. (14分)直接排放含SO2的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关SO2性质的探究活动。
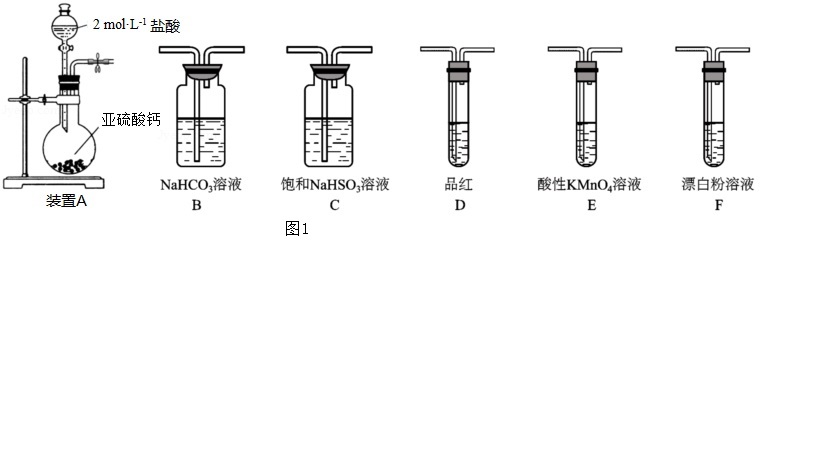
 ②丙同学设计的合理实验方案为:按照A→C →尾气处理(填字母)顺序连接装置。其中装置C的作用是 。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是 。
②丙同学设计的合理实验方案为:按照A→C →尾气处理(填字母)顺序连接装置。其中装置C的作用是 。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是 。(已知:5SO2 + 2MnO4- + 2H2O == 2Mn2+ + 5SO42- + 4H+,
10I- + 2MnO4- + 16H+ == 2Mn2++ 5I2 + 8H2O)
①该装置中仪器C的名称为 ,水通入C的进口为_____。
②残液中SO2的含量为 mol·L-1。
27.(15分)砷为VA族元素,金属冶炼过程产生的含砷有毒废弃物需处理与检测。
(l)冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:
已知:I .As2S3与过量的S2一存在以下反应:As2S3(s)+3S2—(aq)![]() 2AsS33—(aq);
2AsS33—(aq);
II.亚砷酸盐的溶解性大于相应砷酸盐。
①亚砷酸中砷元素的化合价为 ;
②砷酸的第一步电离方程式为 ;
③“一级沉砷”中FeSO4的作用是 ;
④“二级沉砷”中H2O2与含砷物质反应的化学方程式为 ;
(2)冶炼废渣中的砷元素主要以As2O3的形式存在,可用古氏试砷法半定量检测(As的最低检出限为3.0×10-6g)。
步骤1:取10 g废渣样品,粉碎后与锌粉混合,加人H2SO4共热,生成H3AS气体。
步骤2:将H3AS气体通人AgNO3溶液中,生成银镜和As2O3。
步骤3:取1g废渣样品,重复上述实验,未见银镜生成。
②步骤2的离子方程式为 ;
③固体废弃物的排放标准中,砷元素不得高于4.0×10一5g·kg一1,请通过计算说明该排放的废渣中砷元素的含量 (填“符合”、“不符合”)排放标准,原因是
。
28.(14分)2016年9月。“乔歌里1号”中国首台静默移动发电站MFC30正式问世,MFC30是基于甲醇重整制氢燃料电池发电技术。
(1)甲醇制氢方式主要有以下三种:
反应Ⅰ甲醇水蒸气重整制氢:CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g) ΔH1=+49.4kJ/mol
CO2(g)+3H2(g) ΔH1=+49.4kJ/mol
反应Ⅱ甲醇分解制氢:CH3OH(g)![]() CO(g)+2H2(g) ΔH2=+90.6kJ/mol
CO(g)+2H2(g) ΔH2=+90.6kJ/mol
反应Ⅲ 气态甲醇氧化重整制氢同时生成二氧化碳和氢气:
①已知CO的燃烧热为283.0 kJ/mol,则反应Ⅲ的热化学方程式为
___________________________________________________。
②该三种制氢方式中,等量的甲醇产生氢气最多的是反应 (填“Ⅰ”、“Ⅱ”、“Ⅲ”)。
(2)实验室模拟反应Ⅰ甲醇水蒸气重整制氢过程,合成器组成n(CH3OH):n(H2O) =1:1时,体系中甲醇的平衡转化率与温度和压强的关系如图所示。
③图中的压强由小到大的顺序是 。
(3)MFC30燃料电池是以氢为燃料,Li2CO3与K2CO3混合的碳酸盐为电解质的高温型燃料电池,其负极的电极反应式为 ,正极上通入的气体为 。
35.【化学一选修3:物质结构与性质】(15分)
化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用。
_ __ _____。
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合作录音磁带磁粉原料的为_ (填选项字母)。
A. V2O5B.CrO2 C.PbO D.ZnO
(3)屠呦呦因在抗疟药——青蒿素研究中的杰出贡献,成为首获科学类诺贝尔奖的中国人。青蒿素的结构简式如图l所示,其组成元素的电负性由大到小的顺序为 ;氧原子的杂化方式为____。碳原子的杂化方式为____。
(4)“可燃冰”因储量大、污染小被视为未来石油的替代能源,由甲烷和水形成的“可燃冰”结构如图2所示。
①“可燃冰”中分子间存在的2种作用力为_ ___。
②H2O的VSEPR模型为__ ,比较键角的大小:H2O _ _CH4(填“>”“<”或“=”),原因为

(5) 锂离子电池在便携式电子设备以及电动汽车、卫星等领域显示出广阔的应用前景。$来&源:
该电池负极材料为石墨,石墨为层状结构(如图3),其晶胞结构如图4所示,该晶胞中有 个碳原子。
36.【化学一选修5:有机化学基础】(15分)
颠茄酸酯(J)是一种用于胃肠道平滑肌痉挛及溃疡病的辅助治疗药物,其合成路线如下:
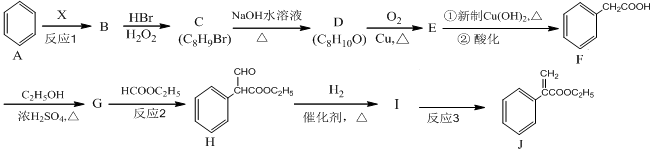
回答下列问题:
(1)烃B中含氢的质量分数为7.69%,其相对分子质量小于118,且反应1为加成反应,则B的分子式为___________,X的化学名称为 。
(2)C→D的反应类型为_____________,G→H 的反应类型为_____________。
(3)D的结构简式为___________________,G的结构简式为_______________________。
(4)反应3的化学方程式为__________________________________________。
(5)J的核磁共振氢谱有__________个峰。
(6)化合物I有多种同分异构体,同时满足下列条件的结构有 种。
①能发生水解反应和银镜反应
②能与FeCl3溶液发生显色反应
③苯环上有四个取代基,且苯环上一卤代物只有一种
二模理综 化学试卷答案
选择题 7、C 8、C 9、D 10、 C 11、B 12、 C 13、A
26、(14分)(1)CaSO3+ 2H+ = Ca2++ SO2↑ + H2O(2分)
(2) ①二氧化硫通入次氯酸钙溶液发生了氧化还原反应不能证明强酸制备弱酸的原理(2分)
②B→E→D→F(2分)除去HCl气体以免影响后面的实验测得(2分)
装置D中品红溶液不褪色,F中出现白色沉淀(2分)
(3)①球形冷凝管(1分)b(1分)②0.2500(2分)
27、(15分)
(1) ① +3(2分) ②H3AsO4![]() H++H2AsO4—(2分)
H++H2AsO4—(2分)
③沉淀过量的S2—,使As2S3(s)+3S2—(aq)![]() 2AsS33—(aq)平衡左移,提高沉砷效果 (2分)
2AsS33—(aq)平衡左移,提高沉砷效果 (2分)
④H3AsO3+H2O2=H3AsO4+H2O(2分)
(2)①![]() (2分) ②12Ag++2H3As+3H2O==12Ag↓+As2O3+12H+(2分)
(2分) ②12Ag++2H3As+3H2O==12Ag↓+As2O3+12H+(2分)
③不符合(1分) 因为该废渣砷含量为(3.0×10-6g÷10g)×1000g/kg=3.0×10—4g/kg
大于排入标准4.0×10一5g·kg一1(2分)
28、(14分)
(1)①CH3OH(g)+1/2O2(g)![]() CO2(g)+2H2(g)△H=-192.4 kJ/mol(2分)
CO2(g)+2H2(g)△H=-192.4 kJ/mol(2分)
(无单位0分) ②Ⅰ(2分)
(2)①平衡常数表达式略;(2分) ②67.6%或0.676或0.68;(2分)
③P1<P2<P3(2分)
(3)H2+2e-+CO32-![]() H2O+CO2;(2分)O2(或空气)、CO2(2分)【少答一个扣1分】
H2O+CO2;(2分)O2(或空气)、CO2(2分)【少答一个扣1分】
35、(15分)(1)第四周期第ⅠB族(1分) [Ar] 3d8(1分)(2)B(2分)
(3)O>C>H(1分)sp2(1分)sp3(1分)
(4)①氢键、范德华力(2分,答对一个1分)②V形(1分)<(1分)
甲烷分子的杂化轨道中无孤电子对,而H2O分子有两对孤对电子,孤对电子与成键电子的排斥
力大、键角小。(2分,答案合理即可得分)。
(5)4(2分)
36、(15分)((1)C8H8(2分)乙炔(1分)
(2)水解(或取代)反应取代反应 (每空1分)
(3)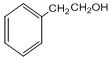 (2分)
(2分)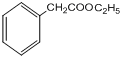 (2分)
(2分)
(4)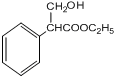
![]()
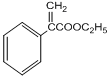 +H2O(2分)
+H2O(2分)
(5)6(2分)(6)6(2分)