
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
宁夏长庆高级中学2017高三第一次模拟考试
理科综合 化学试卷2017.3
第Ⅰ卷 选择题(共126分)
可能用到的相对原子质量(原子量):H:1 Li:7 C:12 N:14 O:16Na:23 S:32Cl:35.5Fe:56 Cu:64
7.化学在人类生活中扮演着重要角色,下列应用不正确的是
A.明矾可用于水的杀菌,消毒B.盐卤可用于制豆腐
C.目前加碘食盐主要添加的是KIO3D.在空气质量日报中SO2含量属于空气污染指数
![]() 8、下列关于有机化合物的说法正确的是
8、下列关于有机化合物的说法正确的是
A. 的名称为2-甲基-1-丙醇 B.氯乙烯和聚乙烯均能发生加成反应
C.C3H2Cl6有4种同分异构体 D.C2H4和C4H8一定是同系物
9、设NA为阿伏加德罗常数的值,下列说法正确的是
A.4.6g乙醇含有的C-H键数为0.6NAB.2gD216O含有的质子数和中子数均为NA
C.每生成1molO2,转移的电子数一定为4NA
D.标准状况下, 22.4L NO与11.2L O2充分反应,产物分子数为NA
10.下列有关实验装置的说法中正确的是
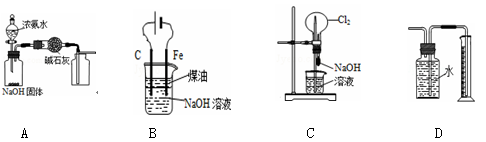
A.用图装置制取干燥纯净的NH3B.用图装置实验室制备Fe(OH)2
C.用图装置可以完成“喷泉”实验 D.用图装置测量Cu与浓硝酸反应产生气体体积
11.常温下,下列各组离子一定能在指定溶液中大量共存的是
![]() A.使甲基橙变红色的溶液中:Na+、Al3+、SO42-、SiO32-
A.使甲基橙变红色的溶液中:Na+、Al3+、SO42-、SiO32-
B. 的溶液中:NH4+、Ca2+、Cl-、NO3-
C.0.1mol·L-1NH4HCO3溶液中:K+、Na+、NO3-、Cl-
D.与Al反应能放出H2的溶液中:Na+、Fe2+、ClO-、SO42-
12、四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性.下列说法正确的是
A.简单离子半径:W<X<ZB.W与X形成的化合物溶于水后溶液呈碱性
C.气态氢化物的热稳定性:W<YD.最高价氧化物的水化物的酸性:Y>Z
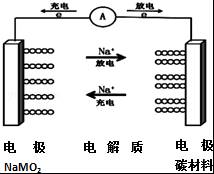 13、.C﹣NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍.该电池的电池反应式为:NaMO2+nC⇌Na(1﹣x)MO2+NaxCn,下列有关该电池的说法正确的是
13、.C﹣NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍.该电池的电池反应式为:NaMO2+nC⇌Na(1﹣x)MO2+NaxCn,下列有关该电池的说法正确的是
$来&源:A.电池放电时,溶液中钠离子向负极移动
B.电池充电时的阳极反应式为:nC+x Na+﹣xe﹣═NaxCn
C.消耗相同质量金属时,用锂作负极产生电子的物质的量比用钠时少
D.该电池负极的电极反应为:NaMO2﹣xe﹣═Na(1﹣x)MO2+xNa+
26、(14分)氯化亚铜(CuCl)常用作有机合成工业中的催化剂,在空气中迅速被氧化成绿色;见光则分解,变成褐色。如图是工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:$来&源:资*源%库
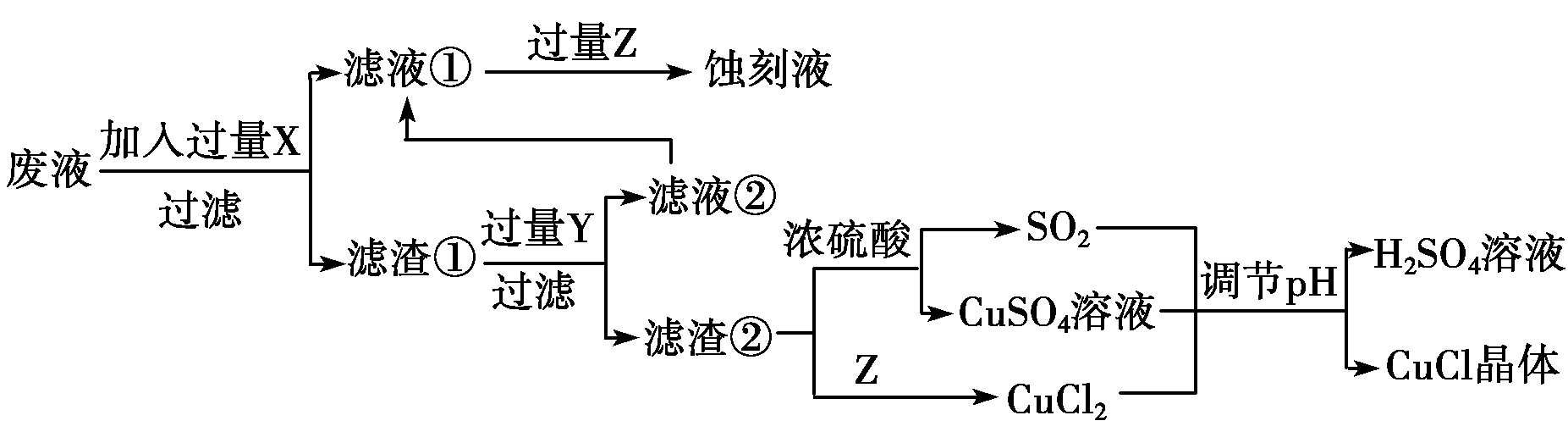
根据以上信息回答下列问题: (1)生产过程中X的化学式为________。
(2)写出产生CuCl的化学方程式:____________________________________。
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由__________________________,实际生产中SO2要适当过量,原因可能是__________________(答一点即可)。
(4)实验探究pH对CuCl产率的影响如下表所示:
| pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| CuCl产率/% | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
析出CuCl晶体最佳pH为________,当pH较大时CuCl产率变低原因是____________________。调节pH时,________(填“能”或“不能”)用相同pH的硝酸代替硫酸,理由是________________________________________________。
(5)氯化亚铜的定量分析:
①称取样品0.25 g和过量的FeCl3溶液于锥形瓶中,充分溶解。
②用0.10 mol·L-1硫酸铈标准溶液滴定。已知:CuCl+FeCl3===CuCl2+FeCl2、
Fe2++Ce4+===Fe3++Ce3+。三次平行实验结果如下(平行实验结果相差不能超过1%):
| 平行实验次数 | 1 | 2 | 3 |
| 0.25 g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为________(结果保留三位有效数字)。
27、(14分)淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去):实验过程如下:
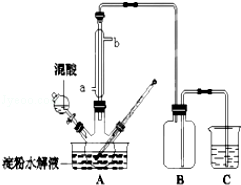 ①将1:1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30min,然后逐渐将温度降至60℃左右;
①将1:1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30min,然后逐渐将温度降至60℃左右;
②将一定量的淀粉水解液加入三颈烧瓶中;
③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液;
④反应3h左右,冷却,减压过滤后得草酸晶体粗品,再重结晶得草酸晶体.硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
请回答下列问题:
(1)实验①加入98%硫酸少许的目的是:__________.
(2)冷凝水的进口是__________(填a或b);实验中若混酸滴加过快,将导致草酸产量下降,其原因是__________.
(3)装置B的作用是__________.为使尾气充分吸收,C中试剂是__________.
(4)重结晶时,将草酸晶体粗品经①加热溶解、②趁热过滤、③冷却结晶、④过滤洗涤⑤干燥等实验步骤,得到较纯净的草酸晶体.该过程中可将粗品中溶解度较大的杂质在__________(填上述步骤序号)时除去;而粗品中溶解度较小的杂质最后留存在__________(填“滤纸上”或“滤液中”).
(5)将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸.
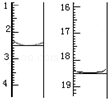 用KMnO4标准溶液滴定,该反应的离子方程式为:__________,称取该样品加适量水完全溶解,然后用0.02000mol•L﹣1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图,则消耗KMnO4溶液的体积为__________.
用KMnO4标准溶液滴定,该反应的离子方程式为:__________,称取该样品加适量水完全溶解,然后用0.02000mol•L﹣1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图,则消耗KMnO4溶液的体积为__________.
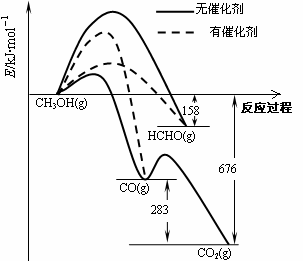
28、(15分)(1)、人们常用催化剂来选择反应进行的方向。右图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图。
①在有催化剂作用下,CH3OH与O2反应主要生成(填“CO、CO2” 或“HCHO”)。2HCHO(g)+O2(g)=2CO(g)+2H2O(g)△H=。
②甲醇制取甲醛可用Ag作催化剂,含有AgCl会影响Ag催化剂的活性。用氨水可以溶解除去其中的AgCl,写出该反应的离子方程式:。
(2)、已知:CO(g)+2H2(g)![]() CH3OH(g)△H = -a kJ•mol-1。
CH3OH(g)△H = -a kJ•mol-1。
①经测定不同温度下该反应的平衡常数如下:
| 温度(℃) | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4 mol·L-1、c(H2)=0.4 mol·L-1、c(CH3OH)=0.8 mol·L-1, 则此时v正v逆(填“>”、“<”或“=”)。
②某温度下,在体积固定的2L的密闭容器中将1 mol CO和2 mol H2混合,测得不同时刻的反应前后压强关系如下:资*源%库
| 时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
则0~15 min,用H2表示的平均反应速率为,达到平衡时CO的转化率为。
(3)、利用钠碱循环法可除去SO2,消除SO2对环境的污染。吸收液吸收SO2的过程中,pH随n(SO32-)∶n(HSO3-)变化关系如下表:
| n(SO32-)∶n(HSO3-) | 91∶9 | 1∶1 | 1∶91 |
| pH | 8.2 | 7.2 | 6.2 |
①根据上表判断NaHSO3溶液显性。
②在NaHSO3溶液中离子浓度关系正确的是(填字母)。
34.[化学—选修3:物质结构与性质](15分)
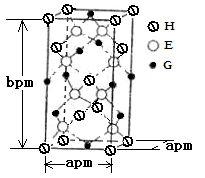 A、B、D、E、G、H均是前四周期的元素。在所有前四周期的基态原子中A的未成对电子最多;B基态原子的L电子层的p能级上有一个空轨道;D 的基态原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;E的基态原子M层有6种运动状态不同的电子;G在周期表中位于第8列,H的原子序数比G大3。根据信息回答下列问题:
A、B、D、E、G、H均是前四周期的元素。在所有前四周期的基态原子中A的未成对电子最多;B基态原子的L电子层的p能级上有一个空轨道;D 的基态原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;E的基态原子M层有6种运动状态不同的电子;G在周期表中位于第8列,H的原子序数比G大3。根据信息回答下列问题:
(1)E元素基态原子的M层有种能量不同的电子;EO2分子的立体构型为,其VSEPR模型名称为。
(2)A元素的名称为,其基态原子价电子排布图为。
(3)区分晶体与非晶体最可靠的科学方法是对固体进行;G与BD能形成挥发性液体G(BD)5,则其属于_________晶体。G常见晶体结构为体心立方堆积,其中G原子在二维平面里放置时的配位数为。某种含G化合物的晶胞如图所示,该晶体的密度为ρg/cm3,则NA可以表示为(用含ρ、a、b的式子表示,不必化简)
35.[化学—选修5:有机化学基础](15分)
Ⅰ.已知:R-CH=CH-O-R′![]() R-CH2CHO + R′OH
R-CH2CHO + R′OH
(烃基烯基醚)
烃基烯基醚A的相对分子质量为176,分子中碳氢原子数目比为3∶4 。与A相关的反应如下:

请回答下列问题:
⑴A的分子式为,B的名称是。
⑵写出C → D反应的化学方程式:。
⑶链烃M的相对分子质量比B多24,分子中所有碳原子均在同一平面上,其结构简式是。
Ⅱ.由E转化为对甲基苯乙炔(![]() )的一条路线如下:
)的一条路线如下:

⑷①反应中所加试剂是; ③ 的反应类型是。
⑸写出G的结构简式:。
⑹写出两种同时符合下列条件的E的同分异构体的结构简式:
_________________________、________________________。
① 属于芳香醛; ② 苯环上有两种不同环境的氢原子。
一模考试化学答案
26、(共14分)
(1)Fe(1分)
(2)CuCl2+CuSO4+SO2+2H2O===2CuCl↓+2H2SO4(2分)
(3)Cu+2H2SO4(浓)△CuSO4+SO2↑+2H2O反应中生成的CuSO4和SO2为1∶1,所以理论上不需要补
充SO2气体(2分)
提高Cu2+的还原速率,同时可以防止生成的Cu+被空气氧化(2分)
(4) 2(1分)Cu2+水解程度增大,反应生成CuCl减少,产率减小(2分)
不能 硝酸会与产品CuCl发生反应(2分)
(5) 95.5%(2分)
(6)![]() (各2分)
(各2分)