
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
![]()
![]() 2018年安庆市高三模拟考试(二模)
2018年安庆市高三模拟考试(二模)
理综化学
7.下列生活用品含有天然高分子化合物的是
A.普通玻璃 B.动物脂肪 C.医用药棉 D.硅橡胶
8.《本草纲目》对白酒(俗称烧酒) 的制造过程有如下叙述:“烧酒非古法也,自元时创始,其法用浓酒和糟入甑,蒸令气上,用器承滴露”,“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次……价值数倍也”。文中涉及的操作方法是
A.蒸馏 B.蒸发 C.干馏 D.升华
9. 化合物![]() (b)、
(b)、![]() (d)、
(d)、![]() (p) 的分子式均为C8H8,下列说法正确的是
(p) 的分子式均为C8H8,下列说法正确的是
A.b的同分异构体只有d和p两种
B.b、d、p中仅b不与酸性高锰酸钾溶液反应
C.b、d、p 的二氯代物均只有三种
D.b、d、F 中仅b不可能所有原子在同一平面上
10.实验室测定已部分变质的过氧化钠样品纯度的装置如图所示(Q为弹性良好的气球不与药品反应,取定量的样品放入其中)。按图示安装好仪器,打开分液漏斗的活塞,将稀硫酸滴入气球中。下列说法中不正确的是
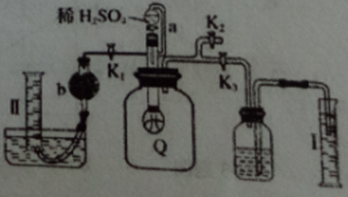
A.稀硫酸滴入气球中,Q 中能生成两种气体
B.准确读取量筒I读数后,先关闭K3然后打开K2,再缓缓打开K1,准确谈取量筒II读数
C.I、II中测量的气体体积的差值即为CO2的体积(相同状况下)
D.b中的固体试剂可以是碱石灰,也可以是无水氯化钙。
11.某化学兴趣小组能探究发现水果汁中存在电解质,可以设计成如图所示的水果原电池。随后又进一步思考原电池工作效率和其构成要素之间的一些关系如下表所示。
| 实验次数 | 电极材料 | 水果品种 | 电极间距/cm | 电压/mV | |
| 1 | 锌 | 铜 | 菠萝 | 3 | 900 |
| 2 | 锌 | 铜 | 苹果 | 3 | 650 |
| 3 | 锌 | 铜 | 西红柿 | 3 | 750 |
| 4 | 锌 | 铝 | 菠萝 | 3 | 650 |
| 5 | 锌 | 铝 | 苹果 | 3 | 450 |
| 6 | 锌 | 铝 | 苹果 | 2 | 550 |
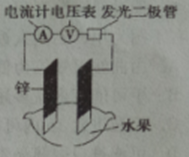
由表中数据可知,下列说法不正确的是
A.实验1、4电流方向应该相反
B.电极及其间距相同时,电压大小只与水果种类有关,与其他因素无关
C.如果用锌、碳棒作电极,实验1中电压可能大于900mV
D.实验中发光二极管不太亮,可用铜锌作电极,用菠萝作介质,并将多个此电池串联起来
12.短周期主族元素W、X、Y、Z的原子序数依次增大,它们占据三个周期。Y原子最外层电子数是电子层数的3倍。同由W、X、Z和SO42-组成一种离子化合物的水溶液中滴加稀氢氧化钠溶液,产生沉淀与加入的氢氧化钠溶液的体积关系如图所示。下列说法正确的是
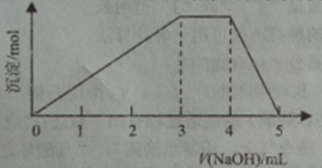
B.Z与X、Y形成的常见盐的水溶液会使蓝色石蕊试纸变红
C.Z的最高价氧化物对应的水化物可溶于X的最简单氢化物的水溶液中
D.由W、X、Y 三种元素只能组成一种盐
13.常温下向浓度均为0.10mol/L、体积均为1mL的NaOH溶液和Na2CO3溶液中分别加水,均稀释至VmL,两种溶液的pH与lgV的变化关系如图所示。下列叙述中错误的是

A.Ka1(CO32-)(Ka1为第一级水解平衡常数)的数量级为10-4
B.曲线N表示Na2CO3溶液的pH随lgV 的变化关系
C.Na2CO3溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
D.若将Na2CO3溶液加热蒸干,由于CO32-水解,最终析出的是NaOH固体
26.(14分)氨基甲酸按(NH2COONH4)是一种白色固体,可由两种常见气体制取,其易分解、易水解,可用于医药、氨化剂等。某科研小组利用以下装置制备氨基甲酸铵。回答下列问题:
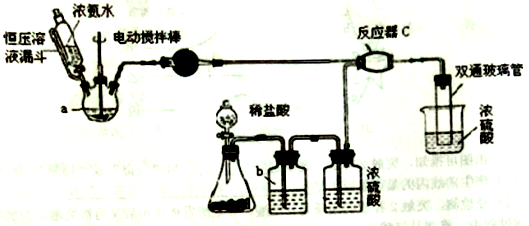
 代替,你认为他的改进有何优点(试述一种): ________ 。
代替,你认为他的改进有何优点(试述一种): ________ 。①设计方案,进行成分探究,请填写表中空格。
限选试剂: 蒸馏水、稀HNO3、BaCl2溶液、Ba(OH)2溶液、AgNO3溶液、稀盐酸。
实验步骤
预期现象和结论
步骤1: 取少量固体样品于试管中,加入蒸馏水至固体溶解。
得到无色溶液
步骤2: 向试管中加入过量的BaCl2溶液,静置。
溶液不变浑浊,则证明固体中不含有________。
步骤3: 取步骤2的上层清液于试管中加入少量 的______。
溶液变浑浊,则证明固体中含有_______。
②根据①的结论: 取氨基甲酸铵样品15.80g,用上题步骤经充分处理后,过滤、洗涤、干燥,测得沉淀质量为5.91g 。则样品中氨基甲酸铵的质量分数为________。
27.(14分)
工业上以砷烟灰(主要含PbO、As2S3、In2O2、In2S3等) 为原料回收稀散金属铟(In)。铟是稀缺资源,主要应用于在透明导电涂层、荧光材料、有机合成等,铟的逆流氧化酸浸工艺流程及工艺条件如下:
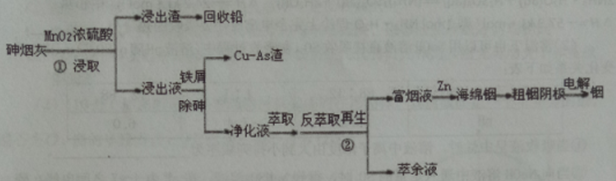
砷烟灰的逆流氧化酸浸工艺条件
| 项目 | 液固比 | 始酸酸度(g·L-l) | 终酸酸度(g·L-l) | 温度(℃) | 时间(h) | 锰粉加入量(%) |
| 一次浸出 | 3~7:1 | 90-120 | 30-80 | >95 | >4 | 3~7 |
| 二次浸出 | 3~7:1 | 150-180 | 120-150 | >95 | >4 | 10-15 |
28.(15分)
造成酸雨的主要物质是NO2和SO2,某科研小组进行如下研究。
| n(SO32-):n(HSO3-) | 88:12 | 1:1 | 12:88 |
| pH | 8.2 | 7.4 | 6.0 |
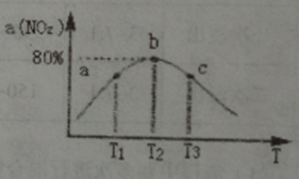
①a、c两点反应速率大小关系: v(a) ___v(c)。(填“>”、“<” 或“=”)
②温度为T2时从反应开始经过2min 达到b点,用SO3表示这段时间的反应速率为______,此温度下该反应的平衡常数为_______。若在此温度下,保持容器的容积不变,再向容器中充入0.10molNO2和0.2molSO2,NO2的转化率_______(填“增大”、“减小”或“不变”).
③NO2的转化率随温度升高先增大后减小的原因是____________。
35.【化学-选修3: 物质结构与性质】 (15分)
组成生命的最基本元素之一是碳,其单质及化合物在研究和生产中有许多重要用途。请回答下列问题:
| 碳酸盐 | MgCO3 | CaCO3 | BaCO3 | SrCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 阳离了半径/pm | 66 | 99 | 112 | 135 |
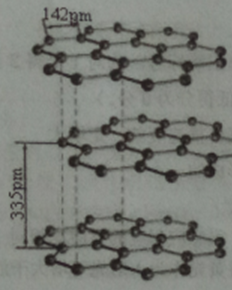
①同一层面内的平面六元并环结构(见上图)。在含lmolC原子的石墨中,有_____个平面正六边形。
②已知石墨层间距为335pm,C-C键长为142pm,其密度______g/cm (已知:lpm=10-10cm。列出计算式即可)
36.【化学选修5: 有机化学基础】 (15 分)
聚合物![]() (W是链接中的部分结构) 是一类重要的功能高分子材料,聚合物X 是其中的一种,转化路线如下:
(W是链接中的部分结构) 是一类重要的功能高分子材料,聚合物X 是其中的一种,转化路线如下:
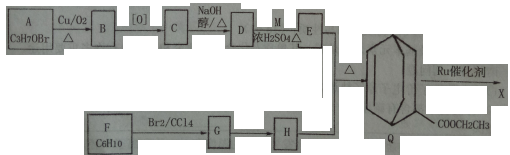
已知:
①A中官能团不在同一个碳原子上。
②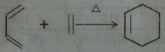
③R1CH=CHR2+R3CH=CHR4![]() R1CH=CHR4+R2CH=CHR3(R 表示烃基或氧原子)。
R1CH=CHR4+R2CH=CHR3(R 表示烃基或氧原子)。
7-13:CABDB BD
26.(14分)
(1)新制生石灰(NaOH固体、碱石灰均可)(1分)CaO+NH3.H2O=Ca(OH)2+NH3↑ CaO吸水且放热促进氨气生成。(填“NaOH固体”则要“放热且降低氨气溶解度促进氨气放出”,合理即可)(2分)
(2)平衡压强,使漏斗内液体顺利滴下(1分)
(3)①装置简单,无需干燥;②低温环境,提高产率(答其中一点即可)(1分)
(4)2NH3+CO2=H2NCOONH4(2分)
(5)防止倒吸 吸收氯化氢气体(2分)
(6)①(NH4)2CO3(1分);Ba(OH)2(1分);NH4HCO3(1分)②85.0%(0.85)(2分)
27.(14分)
(4)As2S3+2MnO2+4H2O+2H2SO4=2H3AsO4+2MnSO4+3H2S↑(2分)
(5)纯铟 减小(每空2分)
(6)[ksp(SnS2)/10-5]1/2(2分)
28.(15分)
(1)45.2 kJ(2分)
(2)① c(Na+)>c(HSO3-) >c(SO32-) >c(H+)= c(OH-)(2分),
②2HSO3-+2H++2e-=S2O42-+2H2O(2分)。
(3))①< (1分),
② 0.04mol·L-1·min-1(2分,掉单位扣1分) 8/3(2分) 不变(2分),
③T2对应的b点为平衡点。T2前是平衡的建立过程,温度升高,反应速率加快,NO2转化率增大;T2后是平衡的移动过程,升高温度,平衡向吸热的逆反应方向移动,转化率减小。(2分)
35. [化学——选修3:物质结构与性质](15分)
(1)![]() ;6;(每空1分)
;6;(每空1分)
(2)碳原子间的价电子可以通过sp3sp2sp等形成共用电子对,构成长的碳链、碳环,以及碳碳单键、双键、三键,而且还存在同分异构现象(3分)。
(3)因为碳酸盐的分解过程实际上是晶体中阳离子结合CO32-中的氧离子,使CO32-分解为CO2的过程,所以当阳离子所带电荷相同时,阳离子半径越小,其结合氧离子能力就越强,对应的碳酸盐就越容易分解(3分);
(4)N>O>C ;(1分)
(5)sp2 分子间作用力;(每空1分)2×12×107
(6)①0.5NA, (1分) ② 6.02×3×1422×sin600×335 (3分)
36.[化学——选修5:有机化学基础](15分)
(1)醛基、溴原子(2分)
(2)丙烯酸乙酯(1分) 消去反应(1分)
(3)CH2=CHCOOH+CH3CH2OH![]() CH2=CHCOOCH2CH3+H2O (2分)
CH2=CHCOOCH2CH3+H2O (2分)
(4) X的结构简式是 ![]() (2分)
(2分)
(5)7种(2分) CH2=C(CH3)COOCH3、CH3COO(CH3)C=CH2(2分,写1个得1分)
(6)(3分)
![]()
欢迎访问“”——