
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
山东省济南市2018届高三第一次模拟考试
理综化学
一、选择题:在每小题给出的四个选项中,只有一项是符合题目要求的。
7.2017年国家科技奖刚刚宣布。下列有关内容都涉及这些奖项。下列说法中不正确的是
A太阳能光解水制氢气涉及到物理过程和化学过程
B.碳纤维、石墨烯和富勒烯互为同素异形体
C.纳米材料、磁性材料、金属材料、捡杂半导体材料能体现新的功能及用途
D.高能量密度炸药、芳香化合物、卤代经、植物油都是有机物,其中植物油属于天然高分子
8.设NA为阿伏伽德罗常数的值。下列有关叙述错误的是
A.80gCuO和Cu2S的混合物中,所含铜原子数为NA
B.1molNaBH4与足量水反应(NaBH4+H2O=NaBO2+H2↑)时转移的电子数为:4NA
C.pH=13的Ba(OH)2溶液中,含有OH-0.2NA个
D.密闭容器中PCl3与Cl2反应生成molPCl5(g),增加2A个P-C1键
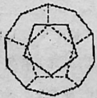
9.在探索苯结构的过程中,人们写出了符合分子式“C6H6”的多种可能结构(如图),下列说法正确的是
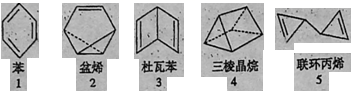
A.1--5对应的结构中的一氯取代物只有1种的有3个
B.1--5对应的结构均能使溴的四氯化碳溶液褪色
C.1--5对应的结构中所有原子均可能处于同一平面的有1个
D.1--5对应的结构均不能使酸性高锰酸钾溶液褪色
10.短周期主族元素W、X、Y、Z的原子序数依次增加。K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体。K是无色气体,是主要的大气污染物之一。0.05 mol/L丙溶液的pH为1,上述物质的转化关系如图所示。下列说法正确的是
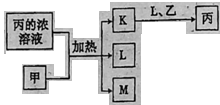
A.元素的非金属性:Z>Y>X
B.丙也可由W、Y组成的某种化合物与K直接反应制得
C.原子半径: W
D.K、L、M中沸点最高的是M
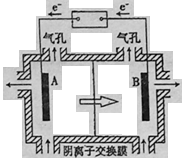
11.现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚![]() ,同时利用此装置的电能在铁上镀铜,下列说法正确的是
,同时利用此装置的电能在铁上镀铜,下列说法正确的是
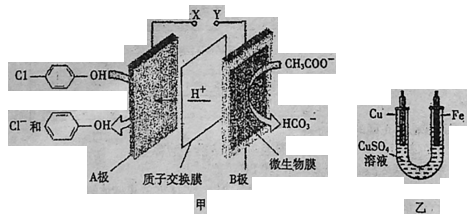
A 当外电路中有0.2mole-转移时,A极区增加的H+的个数为0.2NA
B.A极的电极反应式为![]()
C.铁电极应与Y相连接
D.反应过程中甲中右边区域溶液pH逐渐升高
12.用如图所示装置进行实验,实验现象与对应的结论均正确的是
| 装置 | ① | ② | 实验现象 | 结论 | |
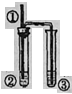 | A | 铜丝 | 稀硝酸 | ②出现红棕色气体 | 硝酸与铜生成了NO2③中需要碱溶液吸收尾气 |
| B | 底端灼热的碳棒 | 浓硝酸 | ②中出现红棕色气体 | 产生气体一定是混合气体 | |
| C | 铜丝 | Fe2(SO4)3溶液 | ②中溶液黄色变浅 | Cu与Fe2(SO4)3溶液发生置换反应 | |
| D | 铁丝 | 浓硫酸 | 无明显现象 | 铁与浓硫酸不反应 |
13.常温下,将11.65gBaSO4粉末置于盛有250mL蒸馏水的烧杯中,然后向烧杯中加入Na2CO3固体(忽视溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是
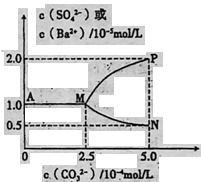
A.相同温度时,Ksp(BaSO4)>Ksp(BaCO3)
B.BaSO4在水中的溶解度、Ksp均比在BaCl2溶液中的大
C.若使0.05molBaSO4全部转化为BaCO3,至少要加入1.25molNa2CO3
D.0.05molBaSO4恰好全部转化为BaCO3时,溶液中离子浓度大小为:c(CO32-)>c(SO42-)>c(Ba2+)
26.(15分)绿矾化学式可以用FeSO4•xH2O表示,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
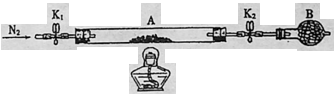
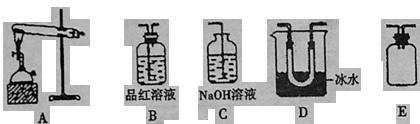
已知:三氧化硫的熔点为16.8℃,沸点为44.8℃
①A中提供热源的仪器名称:______,上述装置正确的连接顺序A→___________ (用大写字母表示)。
②写出煅烧绿矾的化学方程式_____________。
③实验过程中不宜加入过多绿矾,主要原因是_____________________。
27.(14分)红帘石矿的主要成分为Fe3O4、Al2O3、MnCO3、Mg0少量MnO2 等。工业上将红帘石处理后运用阴离子膜电解法的新技术提取金属钰并制得绿色高效的水处理剂(K2FeO4)。工业流程如下:
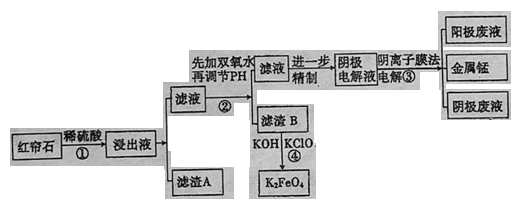
| 离子 | Fe3+ | A13+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀的pH | 2.7 | 3.7 | 7.0 | 7.8 | 9.6 |
| 完全沉淀的pH | 3.7 | 4.7 | 9.6 | 9.8 | 11.1 |
28.(14 分在一定条件下,将燃煤废气中的CO2转化为二甲醚的反应为:
2CO2(g)+6H2(g) CH3OCH3(g+3H2(g) △H
已知:①CO(g)+2H2(g) CH3OH(g) △H1=-90.7kJ.mol-l
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-23.5kJ.mol-l
③CO(g)+H2O(g) CO2(g)+H2(g) △H2=-41.2kJ.mol-l
| 时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强比(P前/P后) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
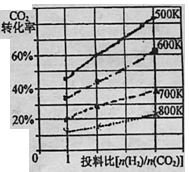
③_______________。
(4)反应③的v-t图像如图1所示,若其他条件不变,只是在反应前增大容器体积使压强减小,则其v-t图像如图2所示。
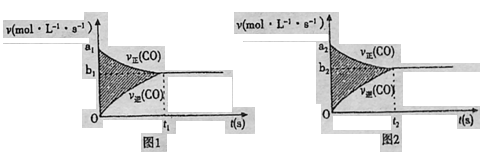
下列说法正确的是
①a1>a2②a1
⑨右图阴影部分面积更大 ⑩左图阴影部分面积更大
(5)由甲醇液相脱水法也可制二甲醚,首先将甲醇与浓硫酸反应生成硫酸氢甲酯(CH3OSO3H):CH3OH +H2SO4→CH3OSO3H+H2O;生成的硫酸氢甲酯再和甲醇反应生成二甲醚,第二步的反应方程式为:____________。与CO2和H2反应制备二甲醚比较,该工艺的优点是反应温度低,转化率高,其缺点是______________。
35.【化学—选修3:物质结构与性质】(15分)
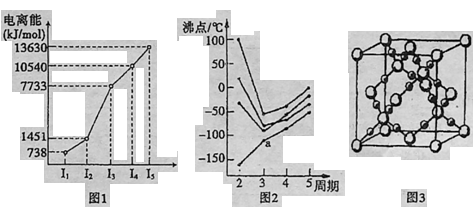
| 离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
| 颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
36.【化学-有机化学基础】(15分)
有机物A含碳72.0%、含氢为6.67%,其余为氧用质谱法分析得知A的相对分子质量为150,A在光照条件下生成一溴代物B,B分子的核磁共振氢谱中有4组峰,峰面积比为2:2:2:3,B可发生如下转化关系(无机产物略):
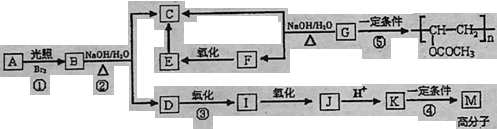
已知:①K与氧化铁溶液发生显色反应,且环上的一元取代物只有两种结构
②当羟基与双键碳原子相连时,会发生如下转化:RCH=CHOH→RCH2CHO
请回答下列问题:
I.苯环上有两个取代基;II.能发生水解反应;III.与氯化铁溶液发生显色反应
其中核磁共振氢谱为5组峰的为_________(写结构简式)。
参考答案
一、选择题:
7.【解析】本题考查STSEC内容,即关注科学技术、社会、环保、文化方面的问题,是高考的方向之一。本题涉及到的新东西比较多,可以用排除法解题,因为植物油是小分子,所以D选项错误,不正确。答案就是D。
8.【解析】本题考查化学计量,是高考考试方向之一。 CuO相对分子质量是80,Cu2S相对分子质量是160, A项正确。NaBH4中氢是-1价,NaBH4+2H2O→NaBO2+4H2↑是与水中的+1价氢的归中反应,B项正确。C选项中没有告诉溶液体积2L,C项错误。值得一提的是D项,要注意是生成了1molPCl5,不是1molPCl3与1molCl2反应生成1 mol PCl5。所以答案是C。
9.【解析】本题是考察必修内容中的有机化学,是高考必考内容。1~5对应的结构中的一氯取代物只有1种的有1和4,是2个,A项错误。1~5对应的结构能使溴的四氯化碳溶液褪色的是2、3、5,B项错误。1~5对应的结构中所有原子均可能处于同一平面的有苯1个,C项正确。1~5对应的结构中2、3、5能使酸性高锰酸钾溶液褪色,D项错误。答案是C。本题模式有些类似2017新课标1的有机化学题型。
10.【解析】本题考查是必修2第一章《原子结构、元素周期律》内容,是高考必考内容,捎带一点儿元素化合物知识。题型类似2016新课标1的该内容题。本题干扰信息比较多:WXYZ、KLM、甲乙丙等等,不易理清。但由丙的浓溶液与甲单质加热反应,产生无色污染性气体K,以及0. 05 mol/L丙溶液的pH为1,可推测丙是浓硫酸,甲是碳单质。但要打破定势思维:SO2+Cl2+2H2O==H2SO4+2HCl,而要有创新思维:2SO2+O2+2H2O==2H2SO4。还要分析到有这样的反应:SO2+ H2O2==H2SO4。推理出:WXYZ依次是HCOS,答案是B。
11.【解析】本题是电化学内容,是高考必考内容。考察了原电池的应用(污水处理)、电镀等。有一定的综合性。A极的电极反应式为![]() +H++2e-=Cl-+
+H++2e-=Cl-+![]() ,B项错误。由该电极反应可知:当外电路中有0.2mole-转移时,A极区增加的H+的个数为0.1NA,A项错误。反应过程中甲中右边区域的电极反应式:CH3COO—8e-+4H2O==2HCO3-+9H+,pH逐渐降低,D项错误。答案C。
,B项错误。由该电极反应可知:当外电路中有0.2mole-转移时,A极区增加的H+的个数为0.1NA,A项错误。反应过程中甲中右边区域的电极反应式:CH3COO—8e-+4H2O==2HCO3-+9H+,pH逐渐降低,D项错误。答案C。
12.【解析】本题考查实验题,是高考必考题型。本题型有些类似2017北京的考试题。稀硝酸与铜反应生成无色一氧化氮气体,A项错误。碳与热的浓硝酸反应生成二氧化碳、二氧化氮气,B项正确。铜与三价铁反应:Cu+2Fe3+==Cu2++2Fe2+,C项错误。铁丝与浓硫酸发生钝化反应,D项错误。答案B。
13.【解析】13题传统上考溶液中的“三个平衡”,本题是溶解平衡,是高考方向之一。由图A点可知:BaSO4的Ksp=1.0x10-10,M点可知BaCO3的Ksp=2.5x10-9,A项错误。由于同离子效应和Ksp只随温度变而变,B项错误。若使0.05molBaSO4全部转化为BaCO3,至少要加入1.30molNa2CO3,C项错误。答案D。
(1)MnO2+2Fe2++4H+=2Fe3++Mn2++2H2O (2分)
(2)Mn2+、Mg2+、Al3+(2分)
(3)d(2分) b(2分)
(4)2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O(2分)
(5)负(2分) 2.24L(2分)
28.(14分)
(1)-122.5 (2分) (2)45%(2分)(3)②升高温度,CO2的转化率降低(2分)
③温度越低,增大投料比使CO2的转化率增大的越显著 (2分)(4)D(2分)
(5)CH3OSO3H +CH3OH→CH3OCH3+H2SO4(2分)
浓H2SO4腐蚀设备或有硫酸废液产生(2分)
35.[化学——选修3:物质结构与性质](15分)
(1)3s23p6(1分) (2)SiH4;(1分)
(3)b (1分) 化合物(CH3)3N为极性分子且可与水分子间形成氢键 (2分)
(4)高;(1分) sp3杂化(1分) (5)12 (1分) 30 (2分)
(6)有(1分) Ni2+的3d轨道上有未成对电子(2分) (7)0.92 (2分)
36.[化学-选修5:有机化学基础](15分)
(1) 溴原子、 酯基(2分) 缩聚反应 (1分)
(2)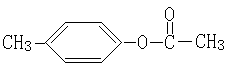 (2分)
(2分)
(3)CH3CHO+2Ag(NH3)2++2OH-![]() CH3COO-+NH4++2Ag↓+3NH3+H2O (2分)
CH3COO-+NH4++2Ag↓+3NH3+H2O (2分)
(4)![]() (2分)
(2分)
![]() (2分)
(2分)
(5)9 (2分)![]() (2分)
(2分)
欢迎访问“”——