
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
青岛二中2017-2018学年第一学期第二学段模块考试
理综化学
注意事项:
1.本卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
2.答题前考生务将自己的姓名、准考证号填写在本试题相应的位置。
3.全部答案在答题卡上完成,答在本试题上无效。
可能用到的原子量 H-1 C-12 O-16 Ni-59 Ce- 140
第Ⅰ卷
一、选择题:本题共13小题,每小题6分,在每小题给出的四个选项中,只有一项是符合题目要求的。
7.化学与科技、生产、生活等密切相关,下列说法正确的是( )
A.利用高纯度 SiO2的光学特性,可制成光电池将光能直接转化为电能
B.“神舟十一号”宇宙飞船返回舱外表面主要是耐高温的新型无机非金属材料
C. 用Ba(OH)2处理含Cu2+的废水,可消除水中重金属离子的污染
D. 聚乙炔用I2或Na等做掺杂后可形成导电塑料,该导电塑料具有固定的熔点、沸点
8.NaCl和KNO3的溶解度随温度变化示意图如右图所示。实验室提纯只含少量氯化钠杂质的硝酸钾的过程如下图所示。下列分析正确的是( )

A.操作Ⅰ是过滤,将固体分离除去
B.操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠
C.操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来
D.操作Ⅰ~Ⅲ总共需两次过滤
9.下列关于有机化合物的说法不正确的是( )
A.高分子化合物![]() 的单体是CH2=CH2和C2H5COOH
的单体是CH2=CH2和C2H5COOH
B.苹果酸的结构简式为HOOCCH(OH)CH2COOH,则该物质可发生氧化、酯化、缩聚反应
C.—C3H7和—C2H5O各取代苯分子中的一个氢原子形成的二元取代物共有24种
D.可以用新制的氢氧化铜悬浊液(可加热)鉴别乙醇、乙酸和葡萄糖
10.分别依据下列实验事实,得出的结论正确的是( )
| 实验事实 | 结论 | |
| A | 向某钾盐溶液中加入浓盐酸产生的气体能使品红褪色 | 该钾盐只能是K2SO3 或 KHSO3 |
| B | 铝热剂加入盐酸后再加入KSCN溶液,溶液变红色 | 铝热剂中一定含有氧化铁 |
| C | 铜放入稀硫酸中,无明显现象,再加入硝酸钠固体,溶液变蓝,有明显的气泡放出,铜溶解 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 向2 mL 0.1 mol/L的硝酸银溶液中加入2 mL0.1 mol/LNaCl溶液,出现白色沉淀,再加入几滴0.1 mol/L Na2S溶液,有黑色沉淀生成 | 氯化银的溶解度大于硫化银 |
11、五种短周期的元素X、Y、Z、W、M的原子序数依次增大,元素X与W位于同一主族,Z元素的单质既能与盐酸反应也能与NaOH溶液反应,W原子的最外层电子数是次外层电子数的一半,M的最高正价与最低负价的绝对值之差为4,五种元素原子的最外层电子数之和为19,下列说法正确的是![]()
|
| B. 室温下, |
| C. 简单离子半径由大到小的顺序: |
| D. Y、Z元素的单质作电极,在NaOH溶液环境下构成原电池,Z电极上产生大量气泡 |
12. 在通电条件下,用下图装置由乙二醛 (OHC—CHO) 制备乙二酸 (HOOC-COOH) 。其制备反应为: OHC—CHO + 2Cl2 + 2H2O→HOOC—COOH + 4HCl ,下列说法不正确的是( )
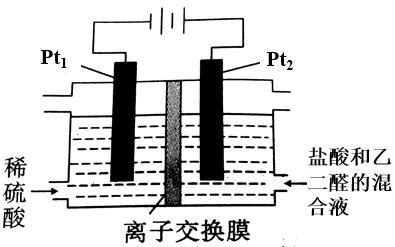
A . 盐酸是起提供 Cl—和增强导电性的作用
B . Pt1的电极反应为:2H+ + 2e—===H2↑
C . 每得到 1mol 乙二酸将有 2molH+从右室迁移到左室
D . 每消耗 0.1mol 乙二醛在 Pt1 极放出 4.48L 气体(标准状况)
13.常温下,几种物质的电离平衡常数如下:
| HCOOH | CH3COOH | NH3•H2O | |
| Ka | 1.77×10—4 | 1.75×10—5 | 1.76×10—5 |
下列说法正确的是( )
A.浓度相同的HCOOH溶液与NH3•H2O溶液等体积混合,所得溶液显碱性。
B.用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液,HCOOH消耗NaOH溶液的体积大
C.0.2 mol•L—1 HCOOH 与 0.1 mol•L—1 NaOH 等体积混合后的溶液中:
C(HCOO—) + C (OH—) = C (HCOOH) + C (H+)
D.0.2 mol•L﹣1CH3COONa 与 0.1 mol•L﹣1盐酸等体积混合后的溶液中(pH<7):
C (CH3COO—)>C Cl—)>C (CH3COOH)>C (H+)
26. (14分)二氧化铈(CeO2)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。
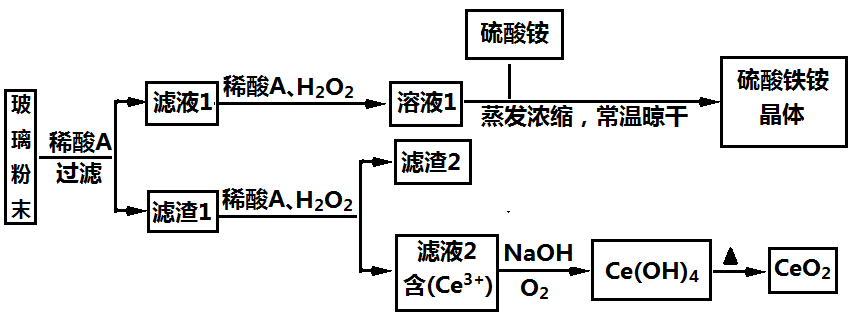
已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
回答下列问题:
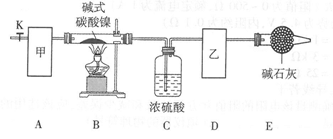

| 装置B中样品质量/g | 装置C 质量/g | 装置D质量/g | |
| 实验前 | 3.77 | 132.00 | 41.00 |
| 实验后 | 2.25 | 133.08 | 41.44 |

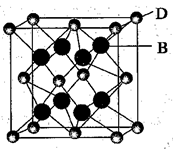
| 元素 | 相关信息 |
| A | A原子的1s轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道中有三个未成对电子 |
| D | D是主族元素且与E同周期,其最外能层上有两个运动状态不同的电子 |
| E | E能与氧形成砖红色E2O和黑色的EO两种氧化物 |
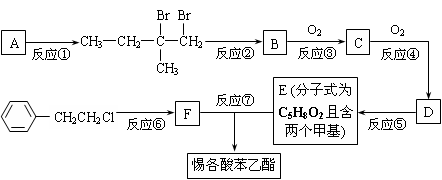
(3) 若发生消去反应(消去HBr分子)生成的产物有 种,
若发生消去反应(消去HBr分子)生成的产物有 种,
写出其中一种的结构简式 。
反应⑥的化学方程式为 。
(5) F的同分异构体有多种,其中能与Na反应产生H2,且苯环上有两个侧链的同分异构体共有____种。
化学答案:
7、B 8、C 9、A 10、D 11、B 12、C 13、D
26、【答案】(1)b(2分)(2)使Fe2+氧化为Fe3+(2分)
(3) 2Ce O2 + H2O2+ 6H+==2Ce3++O2↑+ 4H2O(2分)
(4)取少许滤液1,滴加铁氰化钾溶液,有蓝色沉淀生成,则证明滤液1中有Fe2+。或在溶液中滴加高锰酸钾溶液,紫色退去,或其他合理答案(2分)
(5) Fe2+ +2FeO(OH) == Fe3O4+2H+(2分)
(6)Fe3+ + 3H2O Fe(OH)3 + 3H+,酸性废水抑制Fe3+的水解(或水解平衡逆向移动),使其不能生成有吸附作用的Fe(OH)3胶体(2分)
(7) 98%(2分)
27.(14分)
(l)c(1分)c(1分)
(2)不再有气泡产生 将装置中残留的气体产物吹入吸收装置中
(3)吸收空气中的CO2和水蒸气偏小
(4)Ni3(OH)4CO3·4H2O=3NiO+6H2O+CO2
(5)在装置B、C之间连接一个安全瓶(或其它合理答案均可给分)
28、答案.![]()
![]() H
H![]()
(2)①<,根据图1二氧化碳的转化率随着温度的升高二降低,可知该反应的正反应是放热反应,所以b点的K比c点的K小。② < ③ 正极 ④ CH3OH-6e-+H2O==CO2+6H+
(3) 1×10-12增大
(4) 向右 60
35、![]()
![]() 大 由于N的p电子满足洪特规则,能量降低,第一电离能升高,故N元素的第一电离能比氧元素的第一电离能大
大 由于N的p电子满足洪特规则,能量降低,第一电离能升高,故N元素的第一电离能比氧元素的第一电离能大
![]()
![]() a
a![]()
![]()
36.(15分)⑴碳碳双键、羧基(2分); (2分)
(2分)
⑵②⑥⑦(2分);
⑶3(1分);![]() 、
、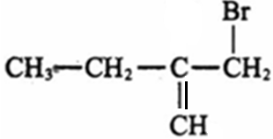 、
、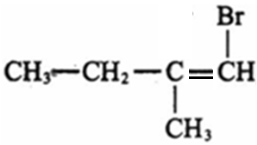
(任写其中一种,2分)
⑷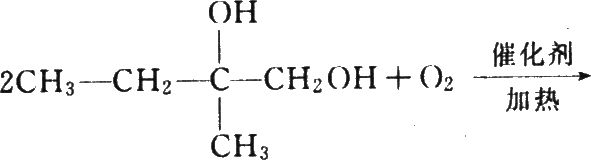
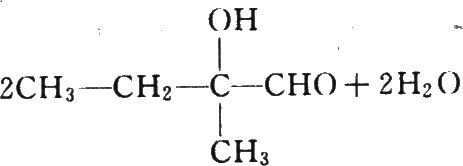 (2分)
(2分)
C6H5CH2CH2Cl + NaOH ![]() C6H5CH2CH2OH + NaCl(2分)
C6H5CH2CH2OH + NaCl(2分)
⑸6(2分)
欢迎访问“”——