
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
![]() 秘密★启用前 2017 年 3 月 7 日
秘密★启用前 2017 年 3 月 7 日
绵阳南山中学 2018 年春季高 2018 届
入学考试理科综合能力测试题(化学)
可能用到的相对原子质量:H 1C 12N 14O 16Co 59Fe 56
7.化学与人类生活、生产和社会可持续发展密切相关,下列说法不正确的是
A.纤维素是多糖,但不能作人类的营养物质
B.生理盐水就是物质的量浓度为 0.9 mol/L 的氯化钠水溶液
C.葡萄酒中可添加适量的二氧化硫起抗氧化、防腐和杀菌等作用
D.有机磷农药多为磷酸酯或硫代磷酸脂类物质,使用肥皂水等碱性物质有利其水解而解毒8.设NA 为阿伏加德罗常数的值,下列说法正确的是
A.在标准状况下,11.2 L NO 与 11.2 L O2 混合所含分子数为 0.75 NA
B.反应 3H2(g)+N2(g) 2NH3(g) H=-92 kJ·mol-1,若转移电子数目为 1.2NA ,则放出热量 4.6 kJ
C.C3H8 分子中的 2 个 H 原子分别被 1 个-NH2 和一个-OH 取代,1 mol 此有机物所含共用电子
对数目为 13 NA
D.40 g CuO 和 Cu2S 混合物中所含铜原子的数目不等于 0.5 NA 9.利用下图装置可以进行实验并能达到实验目的的是

| 选项 | 实验目的 | X 中试剂 | Y 中试剂 | |
| A | 用 MnO2 和浓盐酸制取并收集纯净干燥的 Cl2 | 饱和食盐水 | 浓硫酸 | |
| B | 用 Cu 与稀硝酸制取并收集纯净干燥的 NO | 水 | 浓硫酸 | |
| C | 验证电石与饱和食盐水反应生成的气体的性质 | CuSO4 溶液 | KMnO4 | |
| 并收集 | 溶液 | |||
| D | CaCO3 和稀盐酸制取并收集纯净干燥的 CO2 | 饱和 NaHCO3 溶液 | 浓硫酸 | |
10.下表为元素周期表的部分,其中 A、C、D、E 为短周期元素,最外层电子数之和为 23,下列说
| 法正确的是 | |||||
| A .元素 A 对应的氢化物,常温下一定是气态 | |||||
| B.元素 B、E 的原子序数相差 19 | A | C | D | ||
| C.与金属钠的反应中,1molC 原子和 1molE 原子 | E | ||||
| 得电子数目一定相等 | B | ||||
| D. A、C、D 均可形成 18e-分子 |
11.化学式为 C5H12O2 的二元醇有多种同分异构体。其中主链上有 3 个碳原子和主链上有 4 个碳原子的二元醇,其同分异构体数目分别是 (1 个碳原子上连接 2 个羟基的二元醇不稳定,不计入)
A.1 和 6B.2 和 6C.1 和 7D.2 和 7
12.实验室模拟电解法处理含六价铬的工业废水,用如图装置将主要有害物 Cr2O72-转化为 Cr3+(无害)
除去。得到如下实验结果:

下列说法中,正确的是
A.对比实验①②可知,升高 pH 可以提高 Cr2O72-的去除率
B.实验②中,Cr2O72-在阳极放电,电极反应式为 Cr2O72- + 6e- + 14H+ = 2Cr3+ + 7H2O
C.对比实验②③可知,Cr2O72-去除率增大的原因是 A 电极产生的 Fe2+也能还原 Cr2O72-
 D.实验③中,理论上电路中每通过 6mol 电子,则有 1mol Cr2O72-被还原
D.实验③中,理论上电路中每通过 6mol 电子,则有 1mol Cr2O72-被还原
c(H)
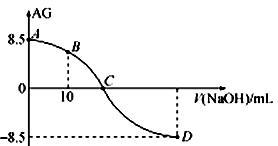
13.化学上常用 AG 表示溶液中的 lg c(OH)。25℃时,用
20.00 mL 0.100 mol•L-1 的 HNO2 溶液,AG 与所加 NaOH 下列说法正确的是
A.D 点溶液的 pH = 11.25
B.B 点溶液中存在 c(H+) - c(OH-) = c(NO2-) - c(HNO2)
C.C 点时,加入 NaOH 溶液的体积为 20 mL
D.25℃时,HNO2 的电离常数 Ka = 1.0×10-5.5
0.100mol•L-1 的 NaOH 溶液滴定
溶液的体积(V)的关系如图所示,
26.(15 分)为探讨化学平衡移动原理与氧化还原反应规律的联系,某同学通过改变浓度研究
“2Fe3++2I-2Fe2++I2”反应中 Fe3+ 和 Fe2+ 的相互转化。实验如下图 1:
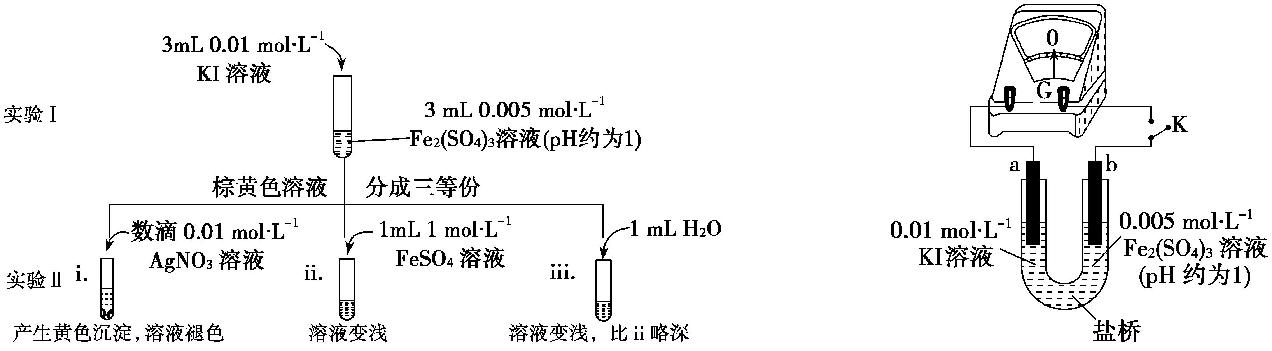
(2) ⅲ是ⅱ的对比实验,目的是排除ⅱ中造成的影响。
(3)ⅰ和ⅱ的颜色变化表明平衡逆向移动,Fe2+ 向 Fe3+转化。用化学平衡移动原理解释原因:
① K 闭合时,指针向右偏转,b 作极。
② 当指针归零 (反应达到平衡) 后,向 U 形管左管中滴加 0.01 mol·L-1AgNO3 溶液,产生的现象证
实了其推测,该现象是。
| ① 转化原因是 | 。 | |||
| ② 与(4)实验对比,不同的操作是 | 。 | |||
结论是。
27.(14 分)
(1)下列环境问题主要由硫氧化物和氮氧化物的排放引发的是。
A.全球变暖 B.酸雨 C.水体富营养化(水华) D.白色污染(2)SO2 的排放主要来自于煤的燃烧。常用石灰石脱硫,其产物可以做建筑材料。
| 已知:CaCO3(s) = CO2(g) + CaO(s) | H= +178.2 kJ·mol1 | |
| SO2(g) + CaO(s) = CaSO3(s) | H= - 402 kJ·mol1 | |
| 2CaSO3(s) + O2(g) = 2CaSO4(s) | H= - 234.2 kJ·mol1 | |
写出石灰石脱硫的热化学反应方程式_________________________________。
| 反应 a: C(s) + 2NO(g) | N2(g) + CO2 (g) | H= - 34.0 kJ·mol1 |
| 反应 b:2C(s) + 2NO2(g) | N2(g) + 2CO2 (g) | H= - 64.2 kJ·mol1 |
![]()
![]()
(3)对于反应 a,在 T1℃时,借助传感器测得反应在不同时间点上各物质的浓度如下:
| 时间(min) | 0 | 10 | 20 | 30 | 40 | 50 | |
| 浓度(mol·L-1) | |||||||
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 | |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 | |
![]()
① 0~10min 内,N2 的平均反应速率 v(N2)=_____,当升高反应温度,该反应的平衡常数
K____________(选填“增大”、“减小”或“不变”)。
_________(填字母)。
a.加入一定量的活性炭b.通入一定量的 NO
c.适当缩小容器的体积d.加入合适的催化剂
(4)某实验室模拟反应 b,在密闭容器中加入足量的 C 和一定量的 NO2 气体,维持温度 T2℃,如图为不同压强下反应 b 经过相同时间 NO2 的转化率随着压强变化的示意图。
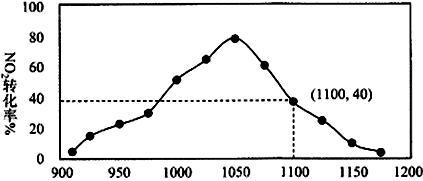
请从动力学角度分析,1050 kPa 前,反应 b 中 NO2 转化率随着压强增大而增大的原因____________;
(5)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作 Kp);在 T2℃、 1.1×105Pa 时,该反应的化学平衡常数 Kp=___________(计算表达式表示);
已知:气体分压(p 分)=气体总压(p 总)× 体积分数。
28.(14 分)
草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为 Co2O3,含少量 Fe2O3、A12O3、
MnO、MgO、CaO、SiO2 等)制取 CoC2O4·2H2O 工艺流程如下:

已知:①浸出液含有的阳离子主要有 H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;②酸性条件下,ClO3-不会氧化 Co2+,ClO3-转化为 Cl-;③部分阳离子以氢氧化物形式沉淀时溶液的 pH 见表:
| 沉淀物 | Fe(OH) | Al(OH) | Co(OH) | Fe(OH) | Mn(OH) | |||||||
| 完全沉淀的 pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 | |||||||
| (1)浸出过程中加入 Na2SO3 的主要目的是 | 。 | |||||||||||
| (2)向浸出液中加入 NaClO3 的离子反应方程式: | 。 | |||||||||||
| (3)已知:常温下 NH3·H2ONH4++OH- | Kb=1.8×10-5 | |||||||||||
| H2C2O4H++HC2O4-Ka1=5.4×10-2 | HC2O4-H+C2O42- | Ka2=5.4×10-5 | ||||||||||
![]()
![]()
![]()
则该流程中所用(NH4)2C2O4 溶液的 pH______7(填“>”或“<”或“=”)。
(4)加入(NH4)2C2O4溶液后析出晶体,再过滤、洗涤,洗涤时可选用的试剂有:________。
A.蒸馏水B.自来水C.饱和的(NH4)2C2O4 溶液D.稀盐酸
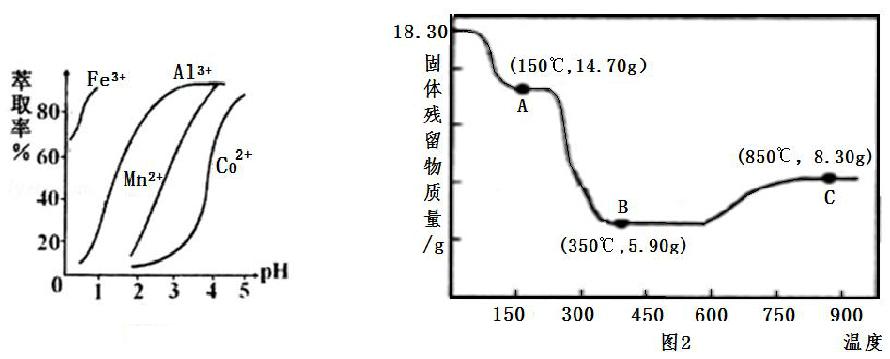
(5)萃取剂对金属离子的萃取率与 pH 的关系如右图 1,萃取剂的作用是________;其使用的适宜 pH
范围是________。
A.2.0~2.5B.3.0~3.5C.4.0~4.5
(6)CoC2O4·2H2O 热分解质量变化过程如图 2 所示。其中 600℃以前是隔绝空气加热,600 ℃以后是在空气中加热。A、B、C 均为纯净物;C 点所示产物的化学式是________。
35.【化学—选修3:物质结构与性质】(15分)
X、Y、Z、W 四种元素的部分信息如下表所示。回答下列问题:
| 元素 | X | Y | Z | W | ||||||
| 相关 | 短周期元素, | 基态原子中,电子占据的最高能 | 核外电子共 | 能与 X 形成两种常见化合物 | ||||||
| 最高化合价 | 层符号为 L,最高能级上只有两 | 有 15 种运动 | WX2、WX3,酚遇 WX3 溶液能 | |||||||
| 信息 | ||||||||||
| 为 +7 价 | 个自旋方向相同的电子 | 状态 | 发生显色反应 | |||||||
| ,X、Y、Z 三种元素电负性由大到小的顺 | |||||||||
| 序为 | (用具体的元素符号填写)。 | |||||||||
(2)化合物 YX4、ZX3、ZX5 (气态或液态时)中,中心原子的轨道类型不是 sp3杂化的是________(填
| 化学式,下同),分子构型是正四面体的是______, | 属于极性分子的是 | 。 | ||||||
| (3)已知 WX3 | 的熔点:306℃,沸点:319℃,则 WX3 的晶体类型为 | ,Y 与氢元素能形 | ||||||
| 成 YnH2n2 | (n 为正整数)的一系列物质,这一系列物质沸点的变化规律以及影响的因素 | |||||||
| 是 | 。 | |||||||
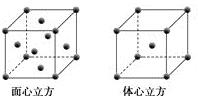
如右图所示。在面心立方晶胞中 W 原子的配位数为;若
晶体的密度可表示为g•cm-3。
36.【化学—选修5有机化学基础】(15分)
以苯为主要原料,制取高分子材料 N 和 R 的流程如下:
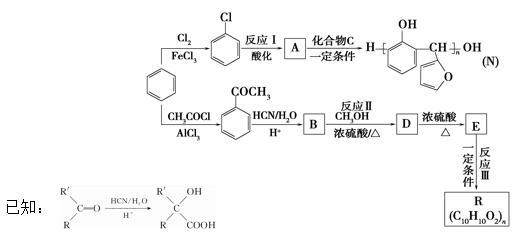
| 。 | ||||||||||||||||
| (2)由 | 生成 | 的反应类型是 | 。 | ||||||||||||||
| (3)一定条件下,发生反应Ⅰ所需的其他反应试剂是 | 。 | ||||||||||||||||
| (4)化合物 C 的结构简式是 | 。 | ||||||||||||||||
| (5)反应Ⅱ的化学反应方程式是 | 。 | ||||||||||||||||
| (6)下列说法正确的是 | (填字母)。 | ||||||||||||||||
| a.A 可与 NaOH 溶液反应 | b.常温下,A 能和水以任意比混溶 | ||||||||||||||||
| c.化合物 C 可使酸性高锰酸钾溶液褪色 | d.E 存在顺反异构体 | ||||||||||||||||
| (7)反应Ⅲ的化学反应方程式是 | 。 | ||||||||||||||||
| (8)符合下列条件的 B 的同分异构体有 | 种。 | ||||||||||||||||
| a.能与饱和溴水反应生成白色沉淀 | b.属于酯类 | ||||||||||||||||
| c.苯环上只有两个对位取代基 | |||||||||||||||||
![]()
![]()

