
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
齐齐哈尔市实验中学2015-2016学年度上学期期中考试
高一化学试题
可能用到的相对原子质量:H:1 O:16 S:32 Cl:35.5 Ba:137
一、选择题(本题包括20小题,每小题3分,共60分,每小题只有一个选项符合题意。)
1.进行化学实验必须注意安全,下列说法不正确的是( )
A. 为防止试管破裂,加热固体时试管口一般要略高于试管底
B. 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
C. 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
D. 酒精着火时用湿抹布盖灭
2.下列对化学概念判断的依据正确的是 ( )
A.溶液与胶体:不同的本质原因是否发生丁达尔效应
B.纯净物与混合物:是否仅含有一种元素
C.氧化还原反应:元素化合价是否变化
D.电解质与非电解质:物质本身的导电性
3.下列对阿伏加德罗定律及推论的理解不正确的是( )
A.同温同压下,气体的体积之比等于它们的物质的量之比
B.同温同压下,气体的体积之比等于它们的质量之比
C.同温同压下,相同体积的气体质量比等于它们的相对分子质量之比
D.同温等容下,气体的压强之比等于它们的物质的量之比
4.下列反应中,离子方程式书写正确的是( )
A. 过量CO2与澄清石灰水反应:Ca2++2OH﹣+CO2═ CaCO3↓+H2O
B. 向KHSO4溶液中加入Ba(OH)2溶液至所得溶液的pH=7
Ba2++OH-+H++SO42-=BaSO4↓+H2O
C 向Ca(HCO3)2溶液中滴入过量的NaOH溶液
Ca2++2 HCO3-+2OH-=CaCO3↓+CO32-+2H2O
D 硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓
5.实验室加热氯酸钾与MnO2的混合物制氧气,从剩余物中回收二氧化锰的操作顺序正确的是( )
A. 溶解、过滤、蒸发、洗涤 B. 溶解、过滤、洗涤、干燥
C. 溶解、蒸发、洗涤、过滤 D. 溶解、洗涤、过滤、干燥
6.在反应2KMnO4![]() K2MnO4+MnO2+O2↑中,还原产物是( )
K2MnO4+MnO2+O2↑中,还原产物是( )
①KMnO4②K2MnO4③MnO2④O2
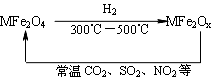 有关上述转化过程的下列叙述正确的是( )
有关上述转化过程的下列叙述正确的是( ) C. 2:11 D. 16:25
二、填空题(共40分)
21.(1)按要求填空:①液态SO3②BaCO3固体 ③酒精 ④盐酸 ⑤汞 ⑥NaCl晶体 ⑦纯醋酸 ⑧水,能导电的是 (填编号,下同),属于电解质的有 ,属于非电解质
(2) 除去NaCl中的Na2SO4,依次加入的溶液为(填溶质化学式):______、______、________;
22. 用98%的浓硫酸(其密度为1.84 g/cm3)配制100 mL 1.0 mol·L-1稀硫酸,若实验仪器有: A.100 mL量筒 B.托盘天平 C.玻璃棒 D.50 mL容量瓶 E.10 mL量筒 F.胶头滴管 G.50 mL烧杯 H.100 mL容量瓶
(1)需量取浓硫酸的体积为 mL。
(2)实验时选用的仪器有(填序号)
(3)配制过程中,下列情况会使配制结果偏低的是(填序号)
①定容时俯视刻度线观察液面 ②容量瓶使用时未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
(4)在容量瓶使用方法中,下列操作不正确的是(填序号)
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.将氢氧化钠固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
D.将准确量取的18.4 mol·L-1的硫酸,注入已盛有30 mL水的100 mL的容量瓶中,加水至刻度线
E.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转
23. 溴被称为“海洋元素”,海水中的溴主要以NaBr的形式存在。查阅资料得知:Br2的沸点为59℃,微溶于水,易溶于有机溶剂。实验室简单模拟从海水(此处以低浓度的NaBr溶液代替)中提取溴单质的流程如图:
(1)写出实验操作的名称,操作① 、操作② ;
(2)在富集过程中,有反应 5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是( )
A.2NaBr+Cl2= 2NaCl+Br2
B.2H2S+SO2= 2H2O+3S↓
C.AlCl3+3NaAlO2+6H2O = 4Al(OH)3↓+3NaCl
D.Cl2 + 2NaOH = NaCl +NaClO + H2O
(3)实验前检测分液漏斗没有问题,但在操作①的步骤中,旋开分液漏斗下端的旋塞,却发现分液漏斗中的液体很难滴下,其原因可能是 ;
(4)下列说法正确的是 。
A.操作①中,可以用酒精代替CCl4
B.操作②中,若发现忘了加碎瓷片,应该趁热补加
C.操作②中,温度计水银球应浸没在蒸馏烧瓶中液体的液面以下,但不能接触瓶底
D.操作②中,冷凝水流向应该是下进上出
24.(1)实验室制取Cl2的反应方程式之一为:2KMnO4+16HCl===2KCl+2MnCl2+5Cl2+8H2O
被氧化的盐酸占反应盐酸总量的 ,]当标准状况下有11.2L氯气生成时,该反应的电子转移数为 。
(2)用双线桥法标出电子转移情况:3BrF3+5H2O==HBrO3+Br2+O2+9HF,当180g水都做还原剂时,被自身还原的BrF3 是 mol.
(3)已知下列两个氧化还原反应:O2+4HI===2I2+2H2O 及Na2S+I2===2NaI+S,则三种单质的氧化性由强到弱的顺序为:
25.1774年,英国科学家Franklin在皇家学会上宣读论文时提到:“把4.9cm3
油脂滴到水面上,立即使水面平静下来,并迅速蔓延开去,使2000 m2水面看起来象玻璃那样光滑”。已知油脂在水面上为单分子层,假设油脂分子的摩尔质量为Mg/mol,每个油脂分子的横截面积为Acm2,取该油脂mg,配成体积为Vml的苯溶液,并将该溶液滴加到水中,当滴入第d滴油脂苯溶液时,油脂的苯溶液在水面上不再扩散,此时油膜表面积为Scm2的。若每滴溶液的体积为aml,则阿伏加德罗常数NA的表达式为
NA=
根据你对本实验的理解,为什么将油脂溶解
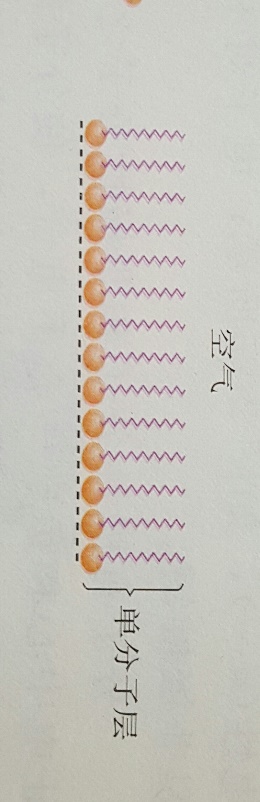
高一化学试卷参考答案
一选择题、(每个3分,共60分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 选项 | A | C | B | C | B | B | D | C | C | B |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 选项 | D | C | B | A | B | D | A | B | D | B |
二、(共40分)
21.(9分)
(1)④⑤⑧②⑥⑦⑧①③(各2分)
(2)BaCl2Na2CO3HCl(各1分)
22.(8分)
(1)5.4mL(2)CEFGH
(3)③(4)BCD(各2分)
23.(9分)
(1)①萃取分液②蒸馏(各1分)
(2)B
(3 ) 没有打开分液漏斗颈部的玻璃塞,或没有使玻璃塞上的凹槽(或小孔)对准漏斗上的小孔。
(4)D((2)、(3)、(4)各2分)
24.(10分)
(1)5/86.02x1023或NA
(2)3BrF3+5H2O=HBrO3+Br2+O2+9HF,10/3
(3)O2>I2>S(各2分)
25.(4分)
(1) SVM/a(d-1) mAmol-1
(2)分子小,油膜薄。不稀溶,膜面阔。(各2分)