
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
南涧县民族中学2016——2017学年下学期期中考
高二化学试题
命题人: 陈朝银
学校班级姓名学号
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共100分,考试用时90分钟。
原子量:H-1C-12 N-14 O-16 S-32 Al-27 Fe-56 Cu-64 Zn-64 Ag-108 Ca-40 Fe-56
第I卷(选择题 共21题,42分)
一、选择题 (本题共21小题,每小题2分,共42分。每小题只有一个正确选项)
1.中华民族有着光辉灿烂的发明史,下列发明创造不涉及化学反应的是
A.用胆矾炼铜 B.用铁矿石炼铁
C.烧结粘土制陶瓷 D.打磨磁石制指南针
2.烷烃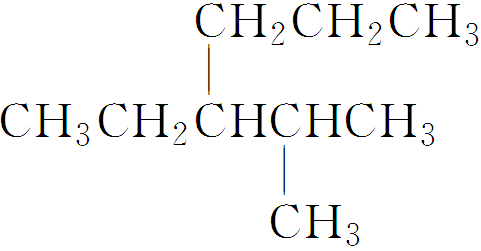 的命名正确的是
的命名正确的是
A.4甲基3丙基戊烷 B.3异丙基己烷
C.2甲基3丙基戊烷 D.2甲基3乙基己烷
3.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试剂是
A.NaOHB.KMnO4C.KSCND.淀粉KI
4.短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子。根据以上叙述,下列说中正确的是
A.上述四种元素的原子半径大小为W<X<Y<Z
B. W、X、Y、Z原子的核外最外层电子数的总和为20
C.W与Y可形成既含极性共价键又含非极性共价键的化合物
D.有W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点
5.下列实验能达到目的的是
A.只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液
B.将NH4Cl溶液蒸干制备NH4Cl固体
C.用萃取分液的方法除去酒精中的水
D.用可见光束照射以区别溶液和胶体
6.下列叙述错误的是
A.用AgNO3溶液可以鉴别KCl和KI
B.制备乙酸乙酯时可用饱和Na2CO3溶液收集产物以除去其中的乙酸
C.制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体
D.SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同
7.下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是
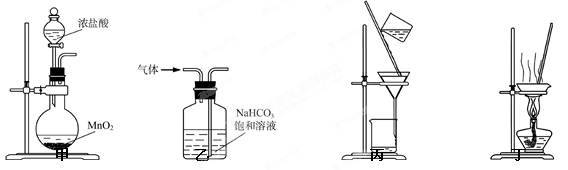
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl2·4H2O
8.下列指定反应的离子方程式正确的是
A.氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
B.Na2CO3溶液中CO32-的水解:CO32-+H2O=HCO3-+OH-
C.酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+=I2+3H2O
D.NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O
9.用NA表示阿伏加德罗常数的值.下列叙述正确的是
A.9g甲基(﹣CH3)所含有的电子数是10 NA个
B.22.4L乙烷中含有的共价键数为7NA个
C.常温下,14g乙烯和丙烯的混合物中总原子数为3NA
D.4.2g C3H6中含有的碳碳双键数一定为0.1NA
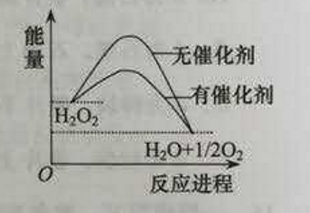 10.已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示。下列说法正确的是
10.已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示。下列说法正确的是
A.加入催化剂,减小了反应的热效应
B.加入催化剂,可提高H2O2的平衡转化率
C.H2O2分解的热化学方程式:
H2O2=H2O + O2ΔH<0
D.断键吸收的总能量小于成键放出的总能量
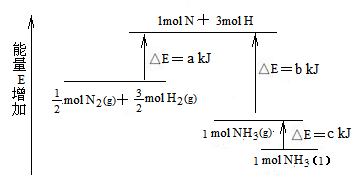 11.化学反应N2+3H2
11.化学反应N2+3H2![]() 2NH3的能量变化如图所示,
2NH3的能量变化如图所示,
该反应的热化学方程式是
A.N2(g)+3H2(g)![]() 2NH3(l)
2NH3(l)
⊿H = 2(a—b—c)kJ/mol
B.N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
⊿H = 2(b—a)kJ/mol
C.0.5N2(g)+1.5H2(g)![]() NH3(l)
NH3(l)
⊿H = (b+c—a)kJ/mol
D.0.5N2(g)+1.5H2(g)![]() NH3(g)
NH3(g)
⊿H = (a+b)kJ/mol
12.运用相关化学知识进行判断,下列结论错误的是
A.某吸热反应能自发进行,因此该反应是熵增反应
B.NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中
C.可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底
D.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率
13.对于可逆反应:A(g)+2B(g)![]() 2C(g) △H<0,下列图像正确的是
2C(g) △H<0,下列图像正确的是
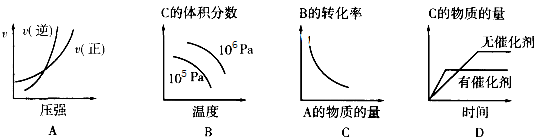
14.下列说法中一定正确的是
A.pH=5的溶液中c(H+)=1.0×10-5mol·L-1
B.pH=7的溶液呈中性
C.pH值为0的溶液中c(H+)=0 mol/L
D.pH=5的溶液中c(OH-)=1.0×10-9mol·L-1
15.下列事实不能证明HNO2是弱酸的是
C.0.1mol·L-1的HNO2溶液的pH=2
D.pH=3的HNO2溶液稀释至100倍后,3
16.等体积等物质的量浓度MOH强碱和HA弱酸溶液混合后,混合液中有关离子浓度应满足的关系是
A.c(M+)>c(H+)>c(A-)>c(OH-) B.c(M+)>c(A-)>c(OH-)>c(H+)
C.c(M+)>c(OH-)>c(A-)>c(H+) D.c(M+)>c(A-)>c(H+)>c(OH-)
17.下列有关沉淀平衡的说法中正确的是
A.在AgCl的沉淀溶解平衡体系中加入蒸馏水,Ksp(AgCl)增大
B.在CaCO3的沉淀溶解平衡体系中加入稀盐酸,平衡不移动
C.可直接根据Ksp的数值大小比较难溶物在水中的溶解度大小
D.25 ℃时,Ksp(AgCl)>Ksp(AgI),向AgCl的悬浊液中加入KI固体,有黄色沉淀生成
18.常温下,下列各组离子一定能在指定溶液中大量共存的是
A.使酚酞变红色的溶液中:Na+、Al3+、SO42﹣、Cl﹣
B.![]() =1×10﹣13molL﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
=1×10﹣13molL﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C.与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
D.水电离的c(H+)=1×10﹣13molL﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
19.O2F2可以发生反应:H2S+4O2F2→SF6+2HF+4O2,下列说法正确的是
A.氧气是氧化产物
B.O2F2既是氧化剂又是还原剂
C.若生成4.48 L HF,则转移0.8 mol电子
D.还原剂与氧化剂的物质的量之比为1:4
20.下列实验的反应原理用离子方程式表示正确的是
A.室温下,测得氯化铵溶液pH<7,证明一水合氨是弱碱:
NH4++2H2O=NH3·H2O+H3O+
B.用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O=2AlO2-+3H2↑
C.用碳酸氢钠溶液检验水杨酸中的羧基:
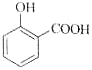 +2HCO3-→
+2HCO3-→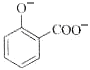 +2H2O+2CO2↑
+2H2O+2CO2↑
D.用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O
21.下列说法正确的 21.下列说法正确的是
中·华.资*源%库
A.图①中△H1=△H2+△H3
B.图②可用于证明实验中生成了乙烯
C.图③表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲线
D.图④可表示由CO(g)生成CO2(g)的过程中要放出566kJ 热量
第Ⅱ卷(非选择题 共58分)
二、 填空题(共4题,58分)
22、 (15分)
某化学研究小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,在实验室中按以下步骤进行实验:
①称取a g样品,置于烧杯中;
②取适量盐酸和适量蒸馏水使样品溶解,准确配制成250mL溶液;
③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;
④加入过量氨水,充分搅拌,使沉淀完全;
⑤过滤,洗涤沉淀;
⑥将沉淀转移到坩埚内,加热、搅拌,直到固体由红褐色全部变为红棕色,冷却至室温后,称量;
⑦……
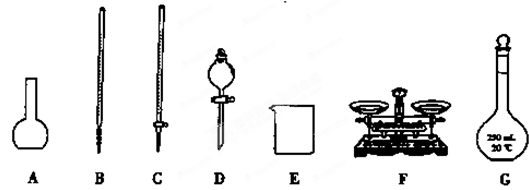
请根据上面的叙述回答下列问题:
(1)装置D的名称是 ,上图所给仪器中,实验步骤①②③中必须用到的仪器是E和_______ (填仪器序号)。
(2)配制步骤③中所得产物的溶液时常加 ,目的是
(3)步骤④中检验沉淀是否完全的操作是
(4)检验沉淀是否洗净的操作是取最后一次洗涤液,加入几滴______ (填写序号)。
①KSCN溶液 ②NaOH溶液 ③AgNO3溶液 ④酚酞试液
23、(13分)煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)将水蒸气通过红热的炭即可产生水煤气,反应为:
![]()
能使化学反应速率加快的措施有________(填序号)
①增加C的物质的量 ②升高反应温度
③随时吸收CO, H2转化为CH3OH ④密闭定容容器中充入CO(g)
(2)在不同温度下将不同起始量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应:![]() ,得到如下两组数据:
,得到如下两组数据:
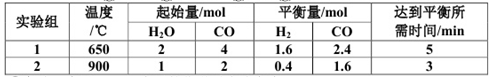
①实验1中以v(CO2)表示的化学反应速率为______________。
②650℃时的化学平衡常数为 ,温度从650℃升高到900℃时,化学平衡常数会______(填“增大”“减小”或“不变”),则该反应的正反应为_ ___(填“吸热”或“放热”)反应。
(3)在一容积为2L的密闭容器内加入2 mol的CO和6 mol的H2,在一定条件下发生如下反应![]() ,该反应的逆反应速率与时间的关系如图所示:
,该反应的逆反应速率与时间的关系如图所示:
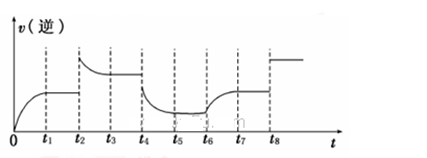
则t4时改变的条件是 ,t5时达到平衡,t6时改变的条件是______________,t8时改变的条件是______________。
请填写下列空白:
A.c(H+):c(OH-)=1:10-2的溶液中K+、Ba2+、ClO-、CO32-一定能大量存在
B.水电离出来的c(H+)=10-13mol/L的溶液中K+、Cl-、NO3-、I-一定能大量存在
C.往0.1mol/LCH3COOH溶液中通人少量HCl,醋酸的电离平衡向逆反应方向移动,且溶液中增大
D.等物质的量浓度的下列溶液:①H2CO3②Na2CO3③NaHCO3④(NH4)2CO3⑤NH4HCO3中
c(CO32-)的大小关系为:②>④>③>⑤>①
25、(14分)聚苯乙烯可用于制备高频绝缘材料,苯乙烯在一定条件下存在如下图转化关系。
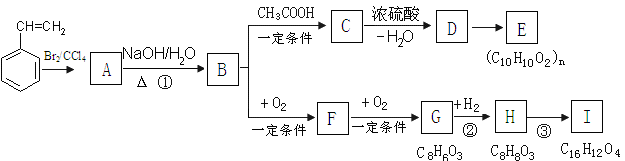
请回答下列问题:
(1)由苯乙烯合成高聚物的化学方程式为 。
(2)写出F中官能团的名称:
(3)C可能的结构简式有 。
(4)H有多种同分异构体,请写出有两个支链,且官能团不完全相同的两种同分异构体的结构简式: 。
(5)反应③的化学方程式是 。
南涧县民族中学2016——2017学年下学期期中考
高二化学答案
一、选择题(每小题2分,共46分)
1D 2D 3B 4C 5D 6C 7C 8D 9C 10D 11A 12D 13B 14A
15A 16B 17D 18B 19D 20B 21C
二.填空题(共54分)
22.(15分)
(1)分液漏斗(2分) , CFG(3分)
(2)盐酸(2分),防止Fe3的水解(2分)
(3)取少量上层清液于试管中,加入氨水,若无沉淀,则沉淀完全。(2分)
(4) ③(2分)
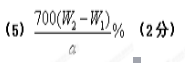
(3)减小压强,增大反应物的浓度,使用催化剂(每空1分)
24.(16分)
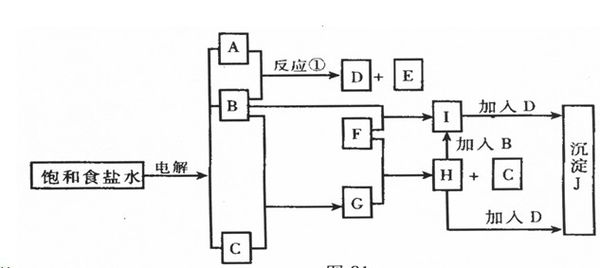
(1)NaClO Fe(OH)3
(2)![]()
![]() (以上每空1分,以下每空2分)
(以上每空1分,以下每空2分)
(3) Cl2+2OH-=Cl-+ClO-+H2O
Fe3+3H2O![]() Fe(OH)3+3H
Fe(OH)3+3H
Cl2+2Fe2=2Cl+2Fe3
5ClO-+2Fe2+5H2O=2Fe(OH)3+Cl+4HClO
(4)H2+2OH--2e-===2H2O或2H2+4OH--4e-===4H2O (5)D
(1)n![]()
![]()
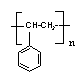
(2)羰基,醛基
(3)![]()
![]()
(4)略
(5)2![]()
![]()
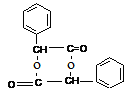 + 2 H2O
+ 2 H2O