
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
高2015级化学高考模拟试题
可能用到的相对原子质量:H-1 Na-23 S-32 O-16 Al-27 C-12
第Ⅰ卷 选择题(42分)
选择题(本大题共7小题,每小题6分,共42。在每小题给出的四个选项中,只有一个选项符合题目要求)
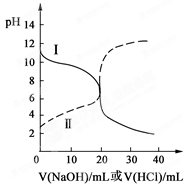 7. 25℃时,取浓度均为0.1 mol·L-1的醋酸溶液和氨水溶液各20 mL,分别用0.1 mol·L-1NaOH溶液、0.1 mol·L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如右图所示。下列说法中正确的是
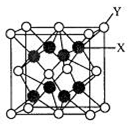
7. 25℃时,取浓度均为0.1 mol·L-1的醋酸溶液和氨水溶液各20 mL,分别用0.1 mol·L-1NaOH溶液、0.1 mol·L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如右图所示。下列说法中正确的是| 元 素 | 性 质 |
| A | 一种核素的原子核内不含中子 |
| B | 原子核外电子有6种不同运动状态 |
| C | 最高价氧化物的水化物与其氢化物反应生成离子化合物 |
| D | 单质之一可阻挡紫外线对人体的伤害 |
| E | 在地壳中的含量位居第三 |
| F | 周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍 |
| G | 该元素的一种氧化物W可用作红色油漆颜料 |
 (4)如果A单质的燃烧热△H1=akJ/mol,BA4的燃烧热△H2=bkJ/mol,一氧化碳的燃烧热△H3=ckJ/mol,那么BA4与水反应生成一氧化碳和氢气的热化学方程式为________________________________。
(4)如果A单质的燃烧热△H1=akJ/mol,BA4的燃烧热△H2=bkJ/mol,一氧化碳的燃烧热△H3=ckJ/mol,那么BA4与水反应生成一氧化碳和氢气的热化学方程式为________________________________。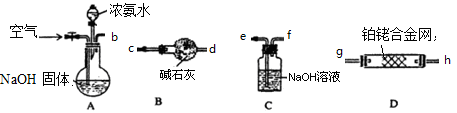
(2)C装置的作用是____________________
[验证性质]
(3)根据题意,该实验小组可能要验证氨气的性质是(用化学方程式表示)__________________,预期的实验现象是___________________
(4)上述装置接口的连接顺序为______________________(填小写字母)。
[延伸探究]
(5)实验小组对反应结束后C中阴离子(OH-除外)提出假设。
假设Ⅰ:只有NO3-
假设Ⅱ:只有NO2-
假设Ⅲ:__________________
(6)查阅资料:NO2-在碱性溶液中以还原性为主,氧气能氧化NO2-;NO2-在酸性溶液中以氧化性为主,I-能将其还原,但是遇到更强氧化剂时NO2-就变成了还原剂。AgNO2是浅黄色固体,不溶于水。
(7)设计实验方案进行探究。(所需试剂从酸性高锰酸钾溶液、碘化钾淀粉溶液、硝酸银溶液、氢氧化钠溶液、稀盐酸、稀硫酸、蒸馏水中选择)
取少量C中溶液于试管中,_________________,证明假设Ⅱ或假设Ⅲ成立,则原来C中发生反应的离子方程式可能为_______________________
10. (16分)A~I均为有机物,它们的转化关系如下图所示(部分反应条件及部分产物已略去)
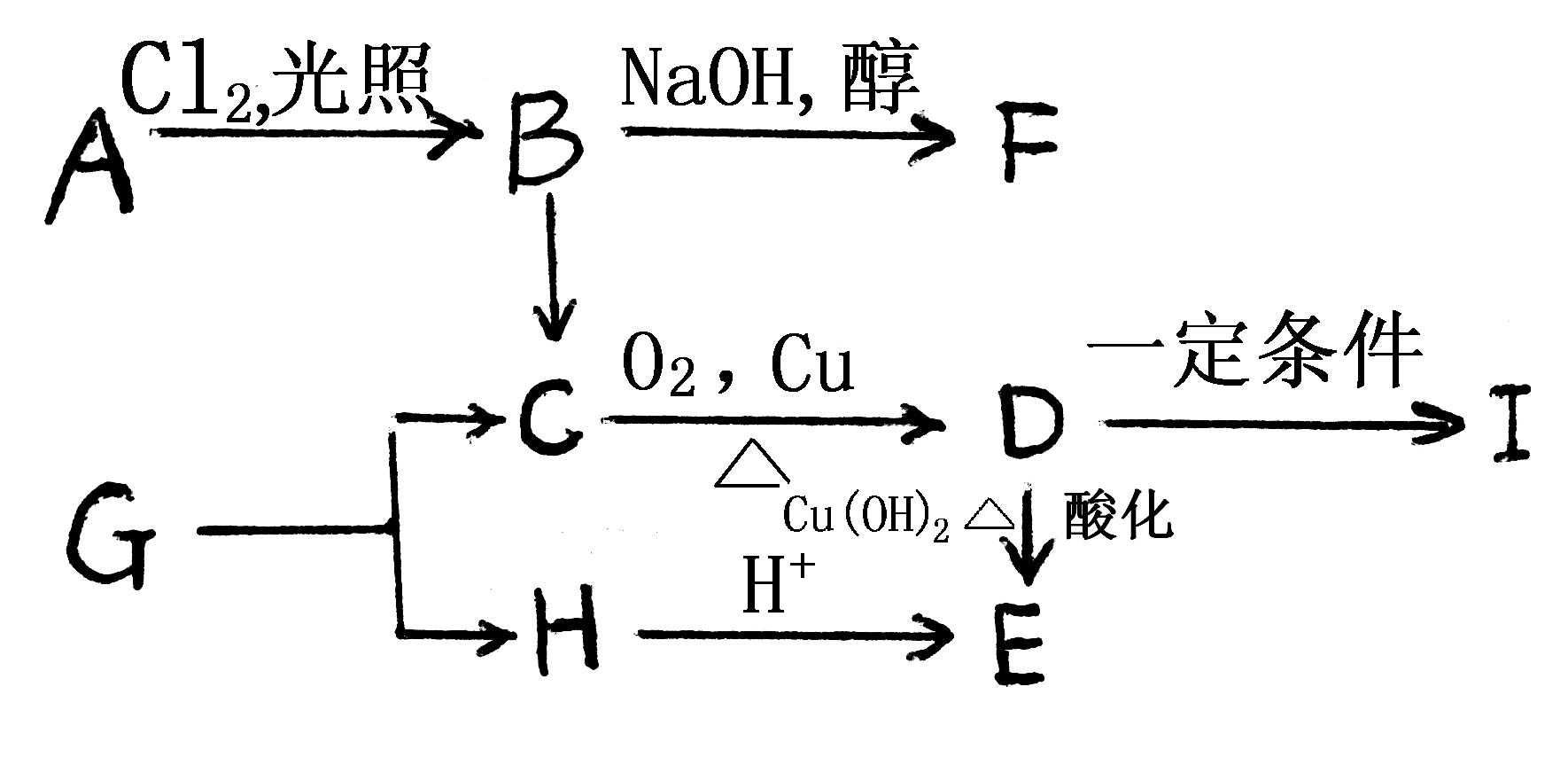
已知:①—CHO +-C-CHO![]() -CH-C-CHO
-CH-C-CHO
②A的分子式是C6H14,核磁共振氢谱有3种峰。
请回答下列问题:
(1)A的名称(系统命名)是___________________________.
![]() B中官能团名称是 _____________________
B中官能团名称是 _____________________
(2) 的反应类型是___________________________,
B→C反应所需试剂和条件是_________________________________
(3)B→F反应的化学方程式是______________________________
F在一定条件下可合成一种高分子材料,其结构简式是_____________
(4)写出同时满足下列条件的E的同分异构体
①能发生水解反应,②能发生银镜反应,③核磁共振氢谱有5个峰
__________________________________________________________
11.(14分)某地有丰富的铝土矿和石灰石资源,拟用铝土矿(主要成分Al2O3,还有少量的Fe2O3、SiO2)为原料冶炼铝,主要工艺流程如图所示(B溶液焰色反应火焰呈黄色):
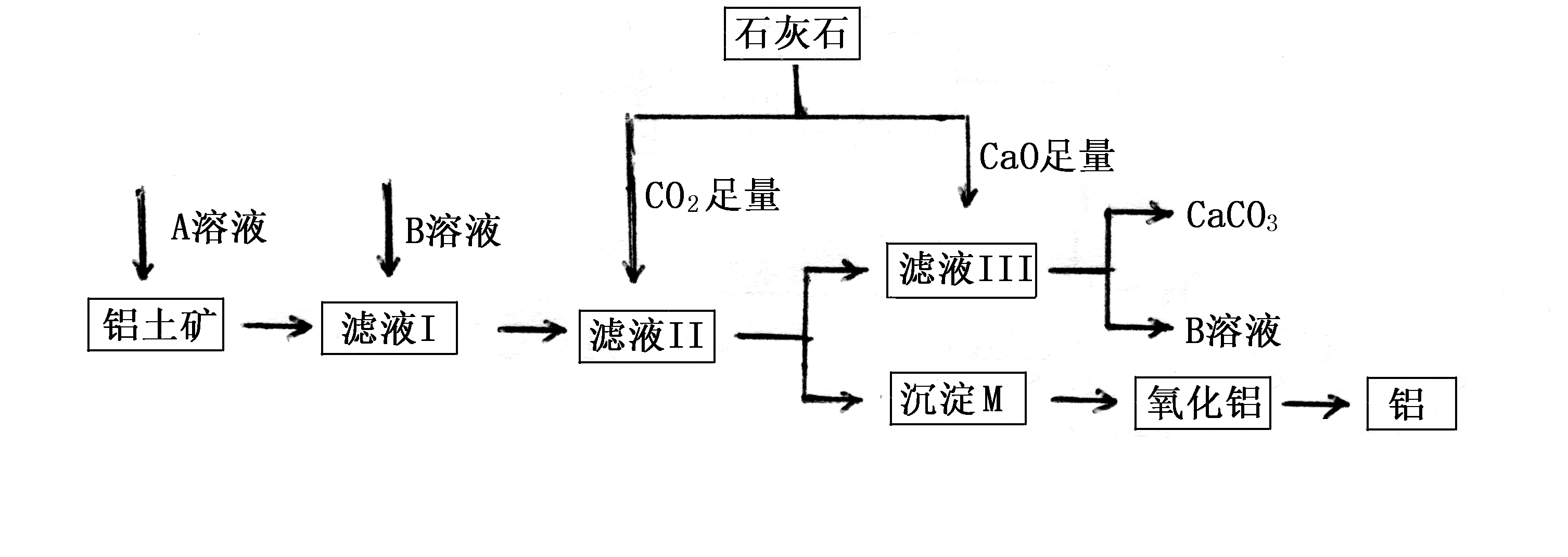
请回答下列问题:
(1)可循环使用的物质是_________________(填化学式).
(2)若不加A溶液而直接向铝土矿中加入B溶液,则过程中制得的沉淀M中含有杂质___________(填化学式)。
(3)以Al和NiOOH为电极,KOH溶液为电解质溶液,组成一种电池,放电时NiOOH转化为Ni(OH)2,该电池放电时的总反应是______________________
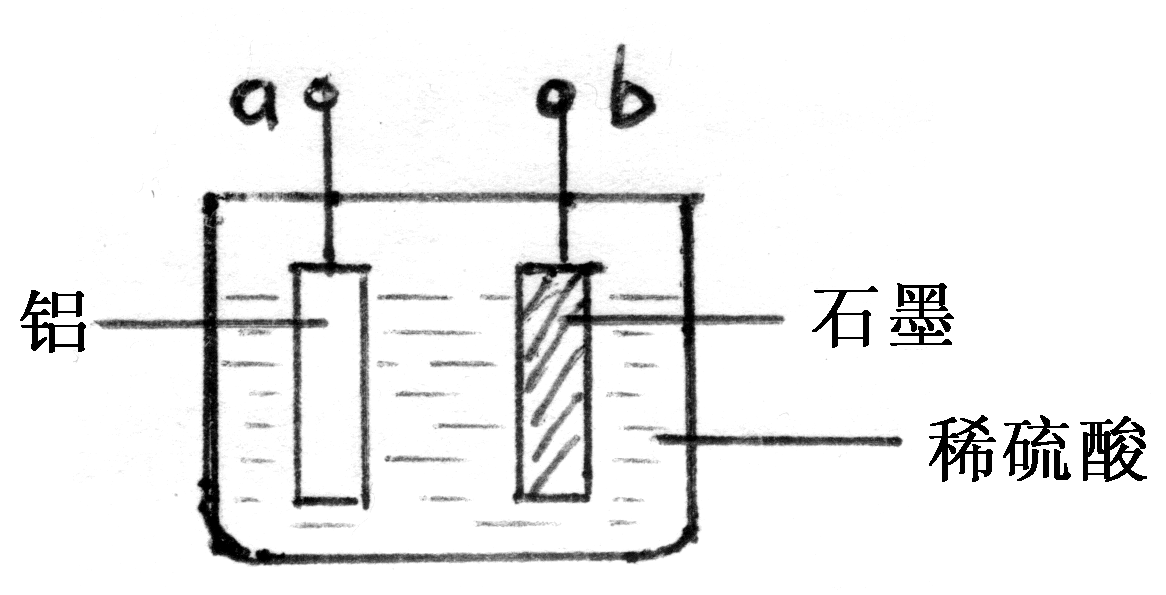 (4)为提高铝的抗腐蚀能力,工业上经常使铝的表面生成致密的氧化膜,其主要装置简单表示如下:
(4)为提高铝的抗腐蚀能力,工业上经常使铝的表面生成致密的氧化膜,其主要装置简单表示如下:
则a端接电源__________极,铝表面生成氧化膜的反应原理是(写电极反应)____________________________________________________________________。
(5)在上述流程中,如果有铝土矿a kg,含氧化铝的质量分数为b,生成沉淀M之前铝元素损失率为20%,由沉淀M生产铝的产率为90%,那么生产出的铝相当于________kg纯氧化铝中的铝元素。
高2015级化学高考模拟试题
参考答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 答案 | C | A | B | C | D | B | D |
:
每空1分 [Ar]3d5O>S>Al(2)每空1分 SP2平面三角形
(3)3分 Fe2O3+3KNO3+4KOH=2K2FeO4+3KNO2+2H2O
(4)3分 CH4(g)+H2O(l)==CO(g)+3H2(g) △H=(b-3a-c)kJ/mol
(5)2分 8
9.(16分)每空2分
:
关闭左端导管和分液漏斗开关,右端导管连接橡皮管末端插入水中,加热烧瓶,产生气泡,停止加热,导管末端形成一段稳定的水柱,证明装置不漏气(2)吸收尾气
(3)4NH3+5O2==4NO+6H2O 或4NH3+7O2==4NO2+6H2O 装置D中有红棕色气体产生
(4)bcdghef
(5)既有NO2-又有NO3-
(6)加入稀硫酸酸化,再加入少量酸性高锰酸钾溶液,如果溶液紫色褪去
4NO+O2+4OH-==4NO2-+2H2O 或 2NO2+2OH-==NO3-+NO2-+H2O 或NO2+NO+2OH-==2NO2-+H2O
10.(16分)
(1)2,2-二甲基丁烷(2分) 氯原子(2分)
(2)取代(2分) NaOH、H2O,加热(2分)
(3)(各2分)
醇 醇
△
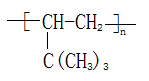
(4)HCOOCH(CH3)CH(CH3)2、HCOO(CH2)2CH(CH3)2(各2分,共4分)
11.(14分)
(1)CaCO3NaOH(2分)
(2)H2SiO3(2分)
(3)Al+3NiOOH+KOH+H2O==KAlO2+3Ni(OH)2(3分)
(4)正(1分) 2Al-6e![]() +3H2O=Al2O3+6H+(3分)
+3H2O=Al2O3+6H+(3分)
(5)0.72ab(3分)