
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
浙江省严州中学高三年级第一次模拟考试
化学学科试题
可能用到的相对原子质量:
C-12 O-16 Na-23 Mg-24 Al-27 S-32 Fe-56 K-39 Cu-64 Ag-108 Cl-35.5 Ba-137
一、选择题(每小题2分,共16分,每小题只有一个正确答案)
1.下列说法正确的是 ( )
A.人造纤维、合成橡胶和光导纤维都属于有机高分子化合物
B.道尔顿、汤姆生、卢瑟福和门捷列夫等对原子结构模型的建立均作出了卓越的贡献
C.化学反应能制造出新的物质,也能制造出新的元素,并伴有能量变化
D.感染MERS致死率较高,为防止感染,要加强环境、个人的卫生和消毒,其中消毒剂常选用
含氯消毒剂、双氧水、酒精等适宜的物质
2.下列有关物质的性质及其解释都正确的是 ( )
A.在漂白粉中滴入70%的硫酸,立刻产生黄绿色气体,在反应中体现硫酸的还原性
B.向一定体积的稀硫酸中加入一定量的Cu、Fe和Fe2O3混合物,反应后有固体剩余,其可能只含铁
C.氢氧化镁和氢氧化铝是常见的阻燃剂,它们分解时发生吸热反应
 D.铝在空气中表现为良好的抗腐蚀性,说明铝极难与氧气反应
D.铝在空气中表现为良好的抗腐蚀性,说明铝极难与氧气反应
3.下列说法正确的是 ( )
A.氯化钠固体不导电,所以氯化钠是非电解质
B.向纯水中加入碳酸钠能使水的电离平衡正向移动,水的离子积增大
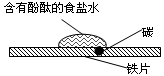
C.如右图研究的是铁的吸氧腐蚀,实验中红色首先在食盐水滴的中心出现题3图
D.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) 的△H<0 △S<0
4.下列有关说法正确的是 ( )
A.原子最外层电子数为2的元素一定是ⅡA元素
B.第三周期元素对应的离子半径从左往右依次减小
C.第ⅦA族元素从上到下,其氢化物的酸性逐渐减弱
D.第三周期的主族元素的最高正价一定等于其最外层电子数
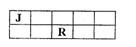
5.J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表。已知:
J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素。下列
说法错误的是 ( )
 A.J和氢组成的化合物分子有多种
A.J和氢组成的化合物分子有多种
B.工业上不用电解M和T组成的化合物来制备M
C.R、T两元素的气态氢化物中,R的气态氢化物更稳定
D.J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是HTO4
6.设NA为阿伏伽德罗常数的值,下列叙述一定正确的是 ( )
A.1 L 2 mol·L-1的NH4Cl溶液中含有的NH4+数目为2NA
B.标况下,0.1mol苯中含有C=C键数目为0.3NA
C.常温常压下,5.2g乙炔和苯的混合气体中含有的碳原子数为0.4NA
D.7.8g过氧化钠与足量CO2反应,转移电子数为0.2NA,CO2为还原剂
7.下列关于有机物的说法或表述中不正确的是 ( )
A.等质量的乙烷、乙烯、乙炔在氧气中完全燃烧,消耗的氧气乙烷最多
B.可借助于核磁共振氢谱区分乙醇和二甲醚这两种物质
C.CH3CH(CH3)CH(CH3)CH(C2H5)CH2CH3的名称:2,3-二甲基-4-乙基己烷
![]() D.石油裂解和油脂的皂化都是高分子生成小分子的过程
D.石油裂解和油脂的皂化都是高分子生成小分子的过程
8.微粒甲与离子乙在溶液中的转化关系如图所示: ,则微粒甲是( )
A.Al2O3B.NH4+ C. Fe3+D.CO2
二、选择题(每小题3分,共24分,每小题只有一个正确答案)
9.下列有关实验操作或原理正确的是 ( )
A.用到金属钠时,要用镊子取、再用小刀切下所需量,剩余的钠不能放回原试剂瓶中
B.测氯水的pH,可用玻璃棒蘸取氯水点在pH试纸上,待其变色后和标准比色卡比较
C.比较不同浓度硫酸与Na2S2O3反应的速率不能通过观察气泡逸出快慢比较,因为SO2易溶于水
D.通过测定等物质的量浓度的NaCl、Na2S溶液的pH,比较硫、氯两种元素的非金属性强弱
10.现有两瓶温度分别为15℃和45℃,pH均为l的硫酸溶液,下列有关说法不正确的是( )
A.两溶液中的c(OH-)相等 B.两溶液中的c(H+)相同
C.等体积两种溶液中和碱的能力相同 D.两溶液中的c(H2SO4)基本相同
11.一定温度下,l mol X和n mol Y在体积为2L的密闭容器中发生如下反应:
X(g)+Y(g)![]() 2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是( )
2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是( )
A.用M表示此反应的反应速率γ(M)=0.1a mol·(L·min)-1
B.当混合气体的质量不再发生变化时,说明反应达到平衡状态
C.向平衡后的体系中加入l mol M,平衡向逆反应方向移动
D.向上述平衡体系中再充入l mol X,平衡正向移动,因为此时γ正增大,γ逆减小
12.下列离子反应中,表达正确的是 ( )
A.向AlCl3溶液中加入过量氨水:Al3+ + 4 NH3·H2O = AlO2- + 4 NH4+ + 2 H2O
B.用FeCl3溶液溶解废铜中的铜:2Fe3+ + 3Cu = 3Cu2+ +2 Fe
C.NaHCO3溶液中滴入过量的Ba(OH)2溶液:HCO3-+Ba2++OH- = BaCO3↓+ H2O
D.铝片溶于过量的氢氧化钠溶液中:Al + 4OH- = AlO2- + 2H2O
13.某含Na+的溶液中可能含有Al3+、NH4+、Fe3+、CO32-、 I-、SO32-。取样,滴加足量氯水,有气泡产生;继续向溶液中加BaCl2溶液或淀粉均无现象。为确定该溶液的组成,还需进行的实验有( )
A.取样,滴加硫氰化钾溶液
B.取样,加足量的浓NaOH溶液加热,用湿润的红色石蕊试纸检验气体
C.取样,逐滴滴入氢氧化钠溶液直至足量
D.取样,加足量盐酸加热,湿润的品红试纸检验气体
14.某废水中含有的NH4+在一定条件下可被O2氧化,反应过程如下:
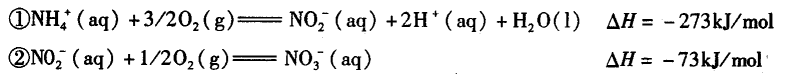
下列说法正确的是( )
A.1mol的NH3和1mol的NH4+都有10×6.02 ×1023个质子
B.室温下,NH4NO2溶液呈酸性,则说明Ka(HNO2)< Kb(NH3·H2O)
C.NH4+(aq)+2O2(g) NO3—(aq)+2H+(aq)+H2O(l);△H= - 346kJ/mol
D.在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
15.普通锌锰干电池的简图(如右下图所示),它是用锌皮制成的锌筒作电极兼做容器,中央插一根碳棒,碳棒顶端加一铜帽。在石墨碳棒周围填满二氧化锰和炭黑的混合物,并用离子可以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解质溶液;该电池工作时的总反应为:
Zn+2NH4++2MnO2=[Zn(NH3)2]2++Mn2O3+H2O
关于锌锰干电池的下列说法中正确的是
A.当该电池电压逐渐下降后,利用电解原理能重新充电复原
B.电池负极的电极反应式为:
2MnO2+2NH4++2e- = Mn2O3+2NH3+H2O
C.该电池碳棒可用铜棒代替,但是工作电压会下降
D.外电路中每通过0.1 mol电子,锌的质量理论上减小6.5g
16.苯乙烯(C6H5CH=CH2)是生产各种塑料的重要单体,其制备
 原理是:C6H5C2H5(g)
原理是:C6H5C2H5(g)![]() C6H5CH=CH2(g)+H2(g),
C6H5CH=CH2(g)+H2(g),
实际生产中常以高温水蒸气作为反应体系的稀释剂(水蒸气不
参加反应),右图为乙苯的平衡转化率与水蒸气的用量、体系
总压强的关系。下列说法正确的是
A.a、b两点转化率不等,但是化学平衡常数相等
B.b点转化率为50%,则混合气体中苯乙烯的体积分数为1/3
C.恒容时加入稀释剂(水蒸气)能减小C6H5C2H5平衡转化率
D.b点和c点温度和压强相同,故其反应速率也相等
三、(本题共4小题,共28分)
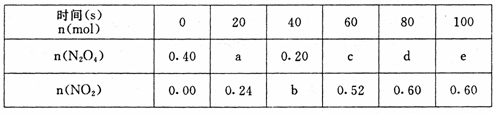
17.(6分)80℃时,将0.40mol的N2O4气体充入2 L已经抽空的固定容积的密闭容器中,发生
 如下反应:N2O4
如下反应:N2O4![]() 2NO2,△H>0隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2,△H>0隔一段时间对该容器内的物质进行分析,得到如下数据:
(1)计算0s—20s内用N2O4表示的平均反应速率为▲mol·L-1·s-1
 (2)要增大N2O4的转化率,同时增大该反应的K值,可采取的措施有(填序号)▲
(2)要增大N2O4的转化率,同时增大该反应的K值,可采取的措施有(填序号)▲
A.通入一定量的NO2气体
B.通入一定量的氦气以增大压强
C.使用高效催化剂
D.升高温度
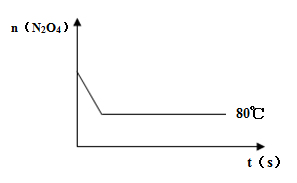
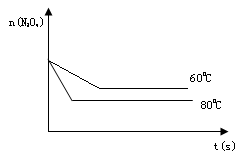
(3)如右图是80℃时容器中N2O4物质的量的变化曲
线,请在该图中补画出该反应在60℃时N2O4物
质的量的变化曲线。
18.(6分)现有反应CO(g)+2H2(g)![]() CH3OH(g)过程中
CH3OH(g)过程中
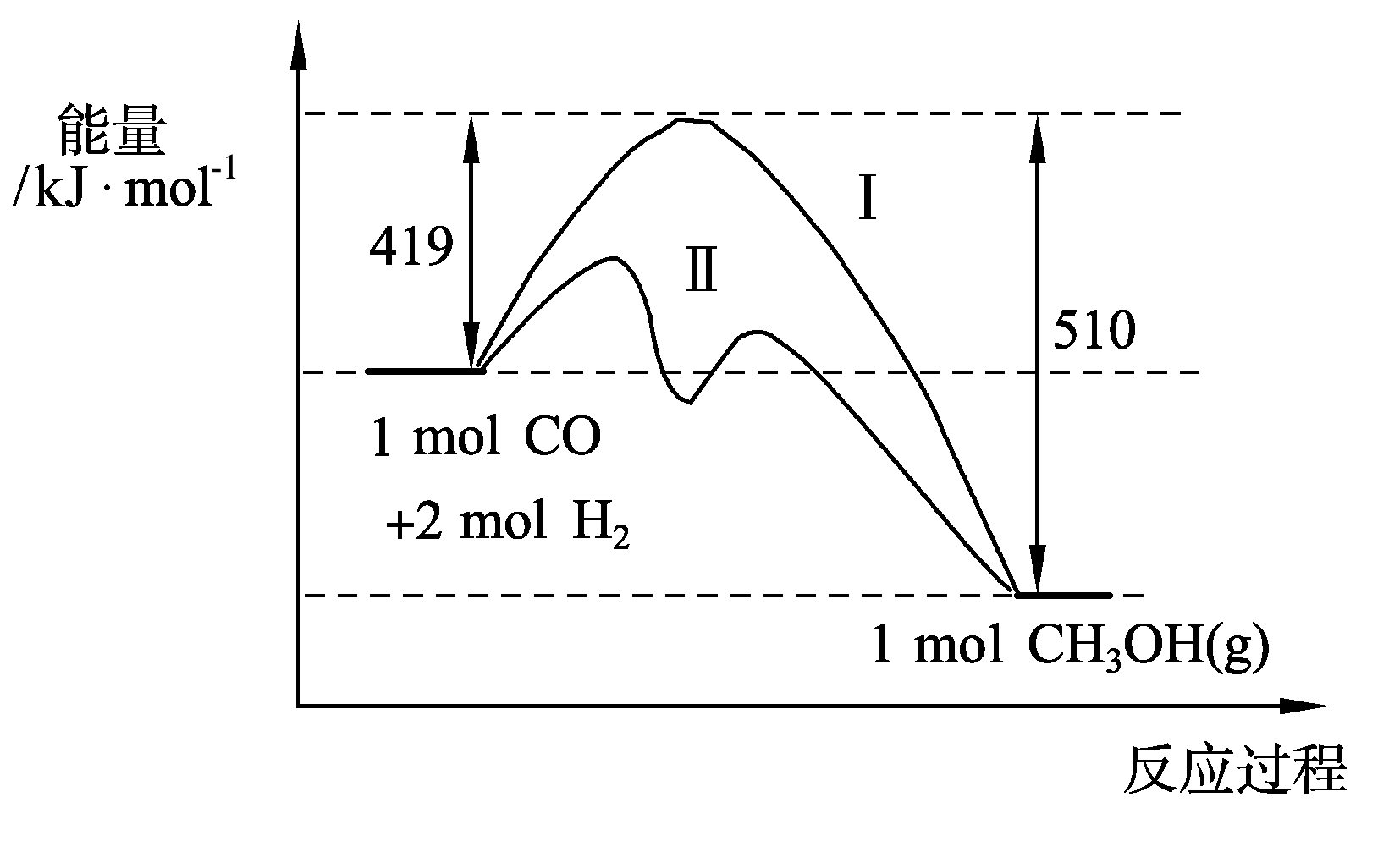 能量变化如右下图所示,写出该反应的热化学方程式▲;
能量变化如右下图所示,写出该反应的热化学方程式▲;
已知该反应中相关的化学键键能数据如下:
| 化学键 | H—H | C—O | H—O | C—H |
| E/(kJ·mol-1) | 436 | 343 | 465 | 413 |
则C≡O中的键能为▲KJ·mol-1;
图中曲线Ⅱ表示▲(填反应条件)的能量变化。
19.(10分)四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题。
| W | X | Y | Z | |
| 结构 或性质 | 最高价氧化物对应的水 化物与其气态氢化物反 应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小 | 最高正价与最 低负价之和为6 |
(1)W元素和氢可形成离子化合物,其电子式为▲。
(2)Y元素和Z元素可形成YZ3化合物,可用于净水剂,净水原理▲(用离子方程式表示)。
(3)①下列可作为比较X和Y金属性强弱的依据是▲(填序号)。
a.最高价氧化物的水化物能反应 b.相应硫酸盐水溶液的pH
c.单质与水反应的难易程度 d.单质与酸反应时失去的电子数
②由X、Y、氢、氧四种元素所组成的化合物,能与盐酸以1:4反应生成两种常见盐和水,则该化合物的化学式为▲。
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X
的最高价氧化物对应的水化物混合,混合后溶液中离子浓度由大到小的顺序是▲。
20.(6分)净水丸能对饮用水进行快速的杀菌消毒,药丸通常分内外两层。外层的优氯净[Cl2Na(NCO)3,氯元素为+1价]先与水反应,生成次氯酸(HClO)起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸)除去。
(1)优氯净中氮元素的化合价为▲。
(2)亚硫酸钠将水中多余次氯酸除去的离子反应方程式为▲。
(3)亚硫酸钠溶液在空气中易变质,请写出检验亚硫酸钠溶液是否变质的方法▲。
四、(本题共2小题,共14分)
21.(6分)用天然气、煤、石油可获得多种有机产品。
(1)从天然气获得的CH4可用于制备CHFCl2(氟利昂的一种主要成分),制备方法如下:
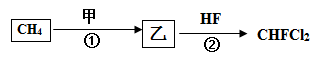
甲为Cl2,反应①的条件是▲,写出乙的结构式▲。
(2)石油通过一定方法可获取汽油,用于获取汽油的方法▲和▲。
(3)煤干馏可获得煤焦油,煤焦油中可分离出苯,写出由苯制备硝基苯的化学方程式▲。
22.(8分)丙烯是重要的化工原料,一定条件下可发生下列转化:
H2O,H+
B
CH3-CH-CH3
CN
KCN
A
HBr
CH3-CH=CH2
③ ② ①
Br2 ④
P
KCN H2O,H+ C2H5OH,浓硫酸 E D C
⑦ ⑥ ⑤
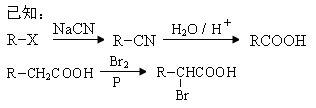
回答下列问题:
(1)以下化合物中含有羧基的是▲。
A.化合物B B.化合物C C.化合物D D.化合物E
(2)上述反应中未涉及的反应类型是▲。
A.取代反应 B.加成反应 C.还原反应 D.加聚反应
(3)写出含碳数最少且与D互为同系物的有机物的结构简式______▲_____;写出D与足量乙醇发生
反应的化学方程式▲。
五、(本题共2小题,共14分)
23.(8分)(1)已知反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O。甲同学通过测定该反应发生时溶液
变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下:
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol·L-1 | V(Na2S2O3)/mL | c(H2SO4)/mol·L-1 | V(H2SO4)/mL | V(H2O)/mL |
| ① | 25 | 0.1 | 5.0 | 0.1 | 10.0 | a |
| ② | 25 | 0.1 | 10.0 | 0.1 | 10.0 | 0 |
| ③ | 25 | 0.2 | 5.0 | 0.1 | 5.0 | b |
| ④ | 50 | 0.2 | 5.0 | 0.1 | 10.0 | 5.0 |
其他条件不变时:探究温度对化学反应速率的影响,应选择实验▲(填实验编号);
若同时选择实验①②、实验②③,测定混合液变浑浊的时间,可分别探究Na2S2O3浓度和H2SO4
的浓度对化学反应速率的影响,则表中a和b分别为▲和▲。
(2)某同学设计如下实验流程探究Na2S2O3的化学性质。
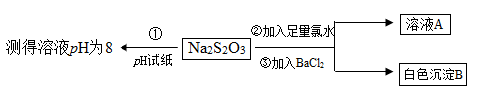
实验操作①中测试时pH试纸的颜色应该接近▲。
A.红色 B.黄色 C.深蓝色 D.绿色
上述流程中实验②、③的目的是为了探究Na2S2O3某种化学性质,你认为是探究了Na2S2O3的▲性。
24.(6分)某同学欲在实验室中对Fe3+与I-的反应进行探究,实现Fe2+与Fe3+的相互转化。
(1)该同学最初的实验操作和现象如下:
| 编号 | 操作 | 现象 |
| I | 先向2 mL 0.1 mol/L FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 | |
| II | 先向2 mL 0.1 mol/L FeCl3溶液中滴加KSCN溶液,再滴加0.1 mol/L KI溶液 |
①实验II的预期现象为▲。
②FeCl2溶液与新制氯水反应的离子方程式为▲。
(2)该同学在进行实验I时,加入的氯水过多,导致出现的红色又褪去,则可能的原因是▲。
六、(本题共1小题,共4分)
25.(4分)某种盐可表示为[xFeSO4·y(NH4)2SO4·6H2O](其摩尔质量为392g·mol-1),可用作标定重铬
酸钾、高锰酸钾等溶液的标准物质,也可用于冶金、电镀。为测定其组成,进行下列实验:
①取一定质量的上述盐样品,准确配制100mL的溶液X;
②量取20.00mL的溶液X,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤,烘干至恒重,得到
白色固体Y 4.660g
③另取20.00mL的X溶液,滴加适量硫酸,用0.1000mol·L-1的KMnO4溶液滴定至终点,生成Mn2+,
消耗KMnO4溶液20.00mL。
(1)在25.00mL试样溶液中c(SO42-)= mol·L-1,n(Fe2+)= mol;
(2)该盐的化学式为 。
浙江省严州中学高三年级第一次模拟考试
化学学科答题卷
一、选择题(每小题2分,共16分,每小题只有一个正确答案)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 选项 |
班级 姓名 考号 座位号
二、选择题(每小题3分,共24分,每小题只有一个正确答案)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 选项 | 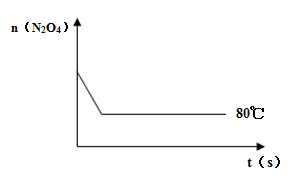 |
三、(本题共4小题,共28分)
17.(6分)(1) ;(2) ;(3)
18.(6分) ;
________________; 。
19.(10分) (1) ;
(2) ;
(3)① ;② ;(4) 。
20.(6分)(1) ;
(2) ;
(3) 。
四、(本题共2小题,共14分)
21.(6分)(1) , ;(2) , ;
(3) 。
22.(8分)(1) ;(2) ;
(3) , 。
五、(本题共2小题,共14分)
23.(8分)(1) ; , ;
(2) , 。
24.(6分)(1)① ;
② 。
(2) 。
六、(本题共1小题,共4分)
25.(4分)(1) ; ; (2) 。
浙江省严州中学高三年级第一次模拟考试
化学学科试题参考答案
一、选择题(每小题2分,共16分,每小题只有一个正确答案)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| D | C | D | D | C | C | D | D |
二、选择题(每小题3分,共24分,每小题只有一个正确答案)
| 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| C | A | B | C | B | C | C | A |
三、(本题共4小题,共28分)
17.(6分)(1)0.003;(2)D;(3) 各2分
18.(6分)
CO(g)+2H2(g)![]() CH3OH(g) △H= -91KJ·mol-1;1084;提供催化剂 各2分
CH3OH(g) △H= -91KJ·mol-1;1084;提供催化剂 各2分
19.(10分) 每空2分
(1)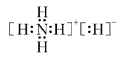 ;(2)Al3++3H2O = Al(OH)3胶体+3H+;
;(2)Al3++3H2O = Al(OH)3胶体+3H+;
(3)①abc;②NaAl(OH)4;(4)c(Na+)>c(N3-)>c(OH-)>c(H+)
20.(6分)每空2分
(1)-3价;(2)SO32-+HClO = SO42-+Cl-+H+
(3)取适量固体于试管,加水溶解,滴加过量盐酸至无气体放出,再滴加BaCl2,有白色沉淀生成证明
试样已经变质。(先加BaCl2,后加盐酸也可)
四、(本题共2小题,共14分)
21.(6分)(1)光照,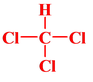 (各1分);(2)分馏,裂化;(各1分)
(各1分);(2)分馏,裂化;(各1分)
(2)![]() (2分)
(2分)
22.(8分)(1)ABC(2分);(2)CD(2分);
(3)HOOC-COOH,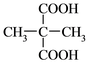 +2C2H5OH
+2C2H5OH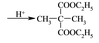 +2H2O (各2分)
+2H2O (各2分)
五、(本题共2小题,共14分)
23.(8分)(1)②④(2分);5.0,10.0 (各1分); (2)D,还原(每空2分)
24.(6分)(1)①滴加KSCN溶液显(血)红色,滴入KI后(血)红色褪去(2分);
②2Fe2++ Cl2= 2Fe3++ 2Cl-(2分)
(2)过量氯水将KSCN(Fe3+)氧化,其他合理答案均可(2分)
六、(本题共1小题,共4分)
25.(4分)(1)1;0.01(每空1分); (2)FeSO4·(NH4)2SO4·6H2O (2分)