
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
![]()
![]() 河北省衡水中学2018届高三上学期九模考试
河北省衡水中学2018届高三上学期九模考试
理综化学
10、下表为元素周期表的部分,其中A、C、D、E 为短周期元素,最外层电子数之和为23,下列说法正确的是
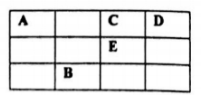
A .元素A 对应的氢化物,常温下一定是气态
B.元素B、E 的原子序数相差19
C.与金属钠的反应中,1molC 原子和1molE 原子得电子数目一定相等
D.A、C、D均可形成18e-分子
11、 NA为阿伏加德罗常数,下列叙述正确的是
A .1molBrCl与H2O完全反应生成氧化氢和次溴酸。转移的电子数为NA
B.锌与一定浓度的浓疏酸反应。产生标准状况下SO2和H2的淝合气体2.4L,锌失去电子数为2NA
C. 标准状况下,6.72LNO2与水充分反应转移的电子数目为0.4NA
D.18gC与1molO2完全反应后。得到CO2的分子个数为NA
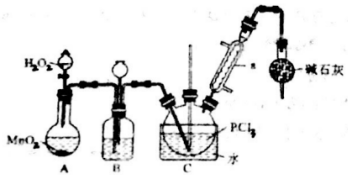
| 物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
| PCl3 | ―112.0 | 76.0 | 137.5 | 均为无色液体,遇水均剧烈 水解为含氧酸和氯化氢,两者互溶 |
| POCl3 | 2.0 | 106.0 | 153.5 |
(3)实验中需控制通入O2的速率,对此采取的操作是_________________________________;
(4)装置B的作用除观察O2的流速之外,还有___________________________________;
(5)反应温度应控制在60~65℃,原因是__________________________________;
II.测定POCl3产品含量的实验步骤:
①实验I结束后,待三颈烧瓶中液体冷却到室温,准确称取16.725g POCl3产品,置于盛有60.00 mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00mL溶液
②取10.00mL溶液于锥形瓶中,加入10.00mL 3.5mol/L AgNO3标准溶液(Ag++Cl-=AgCl↓)
③加入少量硝基苯(硝基苯密度比水大,且难溶于水)
④以硫酸铁溶液为指示剂,用0.2mol/L KSCN溶液滴定过量的AgNO3溶液(Ag++SCN-=AgSCN↓),到达终点时共用去10.00mL KSCN溶液。
(6)达到终点时的现象是_________________________________________;
(7)测得产品中n(POCl3)= ___________________________;
(8)已知Ksp(AgCl)>Ksp(AgSCN),据此判断,若取消步骤③,滴定结果将_______。(填偏高,偏低,或不变)
27、(14分) 碲(Te)为第VIA元素,其单质凭借优良的性能成为制作合金添加剂、半导体、光电元件的主体材料,并被广泛应用于冶金、航空航天、电子等领域。可从精炼铜的阳极泥(主要成分为Cu2Te)中回收碲,
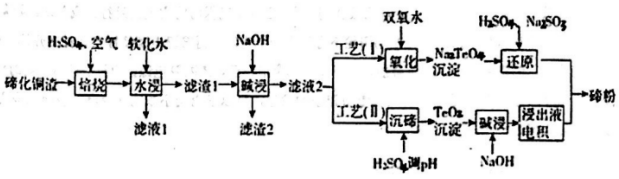
(1)“培烧”后,确主要以TeO2 形式存在,写出相应反应的离子方程式:________________________。
(2)为了选择最佳的培烧工艺进行了温度和硫酸加入量的条件试验,结果如下表所示:
| 温度/℃ | 硫酸加入量 (理论量倍数) | 浸出率/% | |
| Cu | Te | ||
| 450 | 1.25 | 77.3 | 2.63 |
| 460 | 1.00 | 80.29 | 2.81 |
| 1.25 | 89.86 | 2.87 | |
| 1.50 | 92.31 | 7.70 | |
| 500 | 1.25 | 59.83 | 5.48 |
| 550 | 1.25 | 11.65 | 10.63 |
则实验中应选择的条件为_________________,原因为______________________________。
(3) 滤渣1在碱浸时发生的化学方程式为_____________________________。
(4) 工艺( I)中,“还原”时发生的总的化学方程式为____________________________。
(5)由于工艺(1)中“氧化”对溶液和物料条件要求高。有研究者采用工艺(II)获得磅.则“电积”过程中,
阴极的电极反应式为____________________________________。
(6)工业生产中,滤渣2经硫酸酸浸后得滤液3和滤渣3。
①滤液3 与滤液1合井。进入铜电积系统。该处理措施的优点为_____________________________。
②滤渣3中若含Au和Ag,可用_____将二者分离。(填字母)
A.王水 B.稀硝酸 C.浓氢氧化钠溶液 D.浓盐酸
28、(15分) 由H、C、N、O、S等元素形成多种化合物在生产生活中有着重要应用。
I.化工生产中用甲烷和水蒸气反应得到以CO和H2为主的混合气体,这种混合气体可用于生产甲醇,回答下列问题:
(1) 对甲烷而言,有如下两个主要反应:
①CH4(g) +1/2O2(g) =CO(g) +2H2(g)△H1=-36kJ·mol-1
2CH4(g) +H2O(g) =CO(g) +3H2(g) △H2=+216kJ·mol-1
若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO、H2,为维持热平衡,年生产lmolCO,转移电子的数目为______________________。
(2) 甲醇催化脱氢可制得重要的化工产品一甲醛,制备过程中能量的转化关系如图所示。
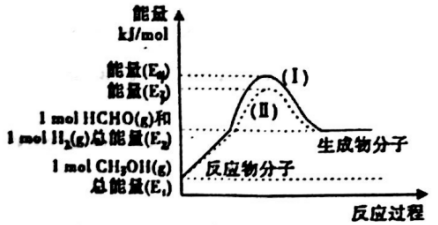
①写出上述反应的热化学方程式________________________________。
②反应热大小比较:过程I________过程II (填“大 于”、“小于”或“等于”)。
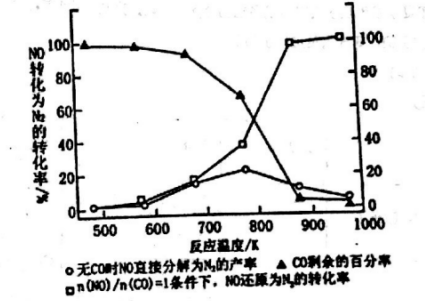
II.(3) 汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领城的重要课题。某研究性小组在实验室以Ag-ZSM-5为催化剂,删得NO转化为N2的转化率随温度变化情况如图所示。若不使用CO,温度超过775K,发现NO的分解率降低。其可能的原因为_____________________________________,
在n(NO)/n(CO)=1的条件下,为更好的除去NOx物质,应控制的最佳温度在_______K左右。
(4) 车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”。活性炭可处理大气污染物NO。在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F。当温度分别在T1℃ 和T2℃时,测得各物质平衡时物质的量(n/mol) 如下表:
| 温度℃ 物质 | 活性炭 | NO | E | F |
| 初始 | 3.000 | 0.10 | 0 | 0 |
| T1 | 2.960 | 0.020 | 0.040 | 0.040 |
| T2 | 2.975 | 0.050 | 0.025 | 0.025 |
①写出NO与活性炭反应的化学方程式_________________________________________;②若T1
③上述反应T1℃时达到化学平衡后再通入0.1mol NO气体,则达到新化学平衡时NO的转化率为______。
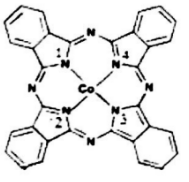
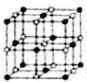 ),在该晶体中与一个钴原子等距离且最近的钴原子有_____个;与一个钴原子等距离且次近的氧原子有______个; 若该钴的氧化物晶体中钴原子与跟它最近邻的氧原子之间的距离为r,该钴原子与跟它次近邻的氧原子之间的距离为______;已知在该钴的氧化物晶体中钴原子的半径为apm,氧原子的半径为bpm,它们在晶体中是紧密接触的,则在该钴的氧化物晶体中原子的空间利用率为____(用含a、b的式子表示)。
),在该晶体中与一个钴原子等距离且最近的钴原子有_____个;与一个钴原子等距离且次近的氧原子有______个; 若该钴的氧化物晶体中钴原子与跟它最近邻的氧原子之间的距离为r,该钴原子与跟它次近邻的氧原子之间的距离为______;已知在该钴的氧化物晶体中钴原子的半径为apm,氧原子的半径为bpm,它们在晶体中是紧密接触的,则在该钴的氧化物晶体中原子的空间利用率为____(用含a、b的式子表示)。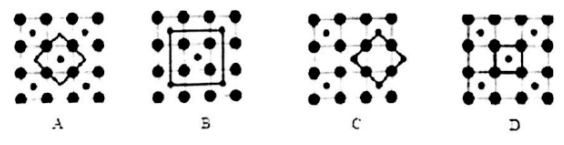
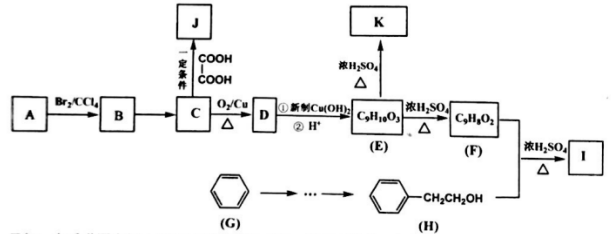
已知: 在质谱图中烃A的最大质荷比为118,其苯环上的一氯代物共三种,核磁共振氢谱显示峰面积比为3:2:2:2:1。
根据以上信息回答下列问题:
(1)A的官能团名称为_________________,B→C 的 反应条件为___________,E→F的反应 类 型为______。(2) I的结构简式为__________,若K分子中含有三个六元环状结构,则其分子式为__________________。
(3) D与新制氢氧化铜悬浊液反应的离子方程式为______________________________________。
(4)H的同分异构体W能与浓溴水反应产生白色沉淀,1molW参与反应最多消耗3molBr2,请写出所有符合条件的W的结构简式_____________________________。
(5) J是一种高分子化合物。则由C生成J的化学方程式为________________________。
(6) 已知:![]() ++RC1
++RC1![]()
![]() +HCl(R为烃基)
+HCl(R为烃基)
设计以苯和乙烯为起始原料制备H的合成路线(无机试剂任选)。
[合成路线示例: CH3CH2OH![]() CH2=CH2
CH2=CH2![]() BrCH2CH2Br]
BrCH2CH2Br]
7-13:CBDDBAB
27、(14 分)(1)Cu2Te+4H++2O2![]() 2Cu2++TeO2+2H2O (2 分)
2Cu2++TeO2+2H2O (2 分)
(2)460℃、硫酸用量为理论量的1.25倍(2分) 该条件下,铜的浸出率高且碲的损失较低(2分)
(3)ToO2+2NaOH=Na2TeO3+H2O (2 分)
(4)Na2TeO4+3Na2SO3+H2SO4==4Na2SO4+Te+H2O (2 分)
(5)TeO32-+ 4e-+3H2O=Te+6OH- (2 分)
(6)CuSO4溶液回收利用,提高经济效益(1分) B (1分)
28、(15 分)
(1)6NA(2 分) (2)CH3OH(g)==HCHO(g)+H2(g) ΔH=+(E2-E1)kJ/mol (2 分) 等于(1分)
(3)NO分解反应是放热反应,升高温度不利于反应进行(只写升高温度不利于反应进行也得满分,其他合理说法也得分) (2分) 870(接近即可给分) (2分)
(4)①C(s)+2NO(g) CO2(g)+N2(g) (没有可逆号扣1分) (2 分) ②<(2分) ③80%(2分)
35、(15 分)( 1) 1s22s22p63s23p63d74s2; (1分)
(2)①N>C>H(1分); sp2(1分) ②2(1分),4(1分);
(3)CN-(1分) N (1分)
(4)12(1分);8(1分)![]() r (2分) 2π/3× (a2+b2)/(a+b)3 (2 分) (5)D(2分)
r (2分) 2π/3× (a2+b2)/(a+b)3 (2 分) (5)D(2分)
36、(15分)
(1)碳碳双键(1分);氢氧化钠水溶液,加热(1分) 消去反应(1分)
(2)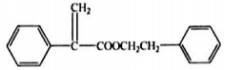 (1分);C18H16O4(1分)
(1分);C18H16O4(1分)
(3)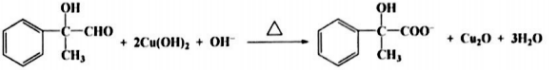 (2分)
(2分)
(4)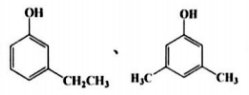 (2 分)
(2 分)
(5)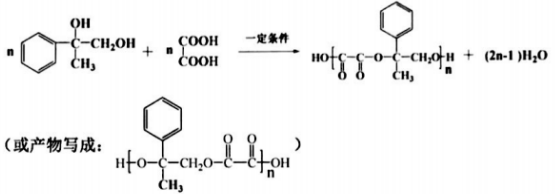 (2分)
(2分)
(6)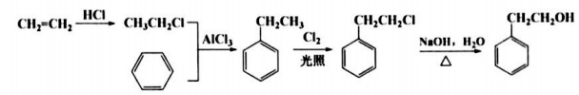
(每步1分,共4分)
欢迎访问“”——