
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
![]() 洛阳市2017—2018学年高中三年级第二次统一考试
洛阳市2017—2018学年高中三年级第二次统一考试
理科综合试题(化学部分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Cu-64 Zn-65 Cl-35.5 Ag-108
一、选择题:本题共13小题,每小题6分。在每小题给出的四个选项中,只有一项是符合题目要求的。
7.化学与人类生产、生活密切相关,下列有关说法不正确的是
A.“海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化
B.将“地沟油”变废为宝,可制成生物柴油和肥皂
C.水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质
D.用活性炭为糖浆脱色和用SO2漂白纸浆的原理不同
8.某有机物的结构简式见图,下列说法正确的是

A.不能发生消去反应
B.分子式为C14H15O6NBr
C.不能使酸性高锰酸钾溶液褪色
D.在一定条件下与氢氧化钠溶液反应,1mol该有机物最多消耗4 mol NaOH
9短周期元素R、T、Q、W在元素周期表中的相对位置如右下图所示,其中T所处的周期序数与族序数相等。下列判断正确的是

A.元素R和Q可以形成一种新型复合材料
B.最高价氧化物对应水化物的酸性:Q
C.W的最低价简单离子核外每个电子层都已排满电子
D.含T的盐溶液一定显酸性
10.下列实验装置能达到实验目的的是
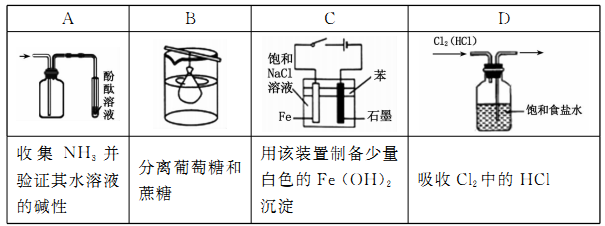
11.NA为阿伏伽德罗常数的值,下列说法正确的是
A.向FeI2溶液中通入适量Cl2,当有2 mol fe2+被氧化时,消耗Cl2的分子数为NA
B.25°C,pH=13的NaOH溶液中OH-的数目为0.1NA
C.2.0gH218O与D2O的混合物中所含中子数为NA
D.235g核素U发生裂变反应:![]() U+
U+![]() n
n![]()
![]() Sr+
Sr+![]() U+10
U+10![]() n,净产生的中子(
n,净产生的中子(![]() n)数为10NA
n)数为10NA
12.连二亚硫酸钠(Na2S2O4)俗称保险粉,还原性比 Naso3更强,工业上广泛用于纺织品漂白及作脱氧剂等。工业上可用惰性电极电解 NaHSO3溶液得到连二亚硫酸钠(Na2S2O4),如下图所示。下列说法不正确的是
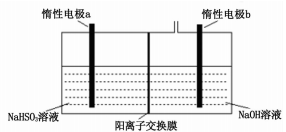
A.得到连二亚硫酸钠产品电极反应式为2HSO3-+2e-=S2O42-+2OH-
B.a为阳极
C.连二亚硫酸钠产品在阴极得到
D.若不加隔膜,则得不到连二亚硫酸钠
13.25℃时,H2CO3的Ka=4.2×10-7,K2=5.6×10-11。室温下向10mL0.1mo1·L-1Na2CO3中逐滴加入0.1mol·L-1HCl。右图是溶液中含C微粒物质的量分数随pH降低而变化的图像(CO2因有逸出未画出)。下列说法错误的是
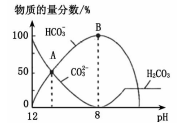
A.A→B的过程中,离子反应方程式为CO32-+H+=HCO3-
B.A点溶液的pH<11
C.分步加入酚酞和甲基橙,用中和滴定法可测定Na2CO3与 NaHCO3混合物组成
D.B点溶液:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
26.(14分)亚硫酰氯(SOCl2)又名氯化亚砜,其熔点-105℃,沸点79℃,140℃以上时易分解。是一种无色或淡黄色发烟液体,遇水剧烈水解生成两种酸性气体,常用作脱水剂,广泛应用于医药、农药、染料工业及有机合成工业。
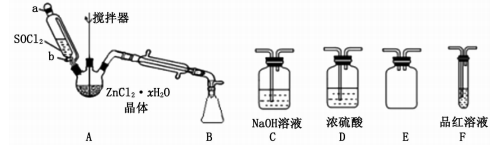
取少量FeCl3·6H2O于试管中,加入过量SOCl2,振荡使两种物质充分反应;再往试管屮加水溶解,滴加KSCN溶液,若___________,则证明脱水过程屮发生了氧化还原反应,按照戊同学的思路方法,还可以选择验证__________或__________(填离子符号)是否存在让明该过程是否发生了氧化还原反应。
27.(15分)印刷铜制电路板的蚀刻液选取和回收再利用一直是研究的热点。

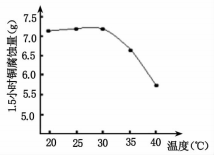
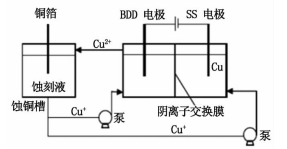
28.(11分)汽车尾气中NOx的排放是造成空气污染的重要因素之一,研究NOx的有效消除成为环保领域的重要课题。
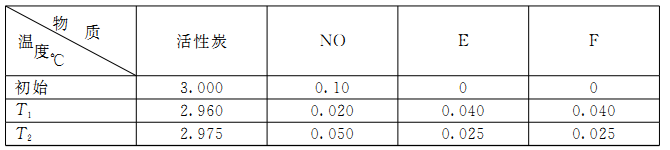
一定条件下,已知:N2(g)+O2(g)=2NO(g) △H=+180.6kJ·mol-1
C(s)+O2(g)=CO2(g) △H=-393.5kJ·mo1-1
①请写出NO(g)与C(s)反应的热化学方程式________________________________;
②根据上述信息判断,温度T1和T2的关系是_______(填序号);
③上述反应T1℃时达到化学平衡后再通入0.1 mol NO气体,则达到新化学平衡时NO的转化率为_______________。
(2)催化氧化法去除NO是在一定条件下,用NH3消除NO污染,其反应原理为![]() 不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图所示:
不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图所示:

①由图可知,无论以何种比例反应,在温度超过900℃时NO脱除率都会骤然下降,这是因为在有氧条件下氦发生了副反应,请写出反应的化学方程式_____________________。
②曲线c对应NH3与NO的物质的量之比是____________。
③曲线a中NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为__________mg/(m3·s)。
(3)NSR技术可实现NOx的储存还原,NOx的储存和还原在不同时段交替进行,工作原理如图a所示。
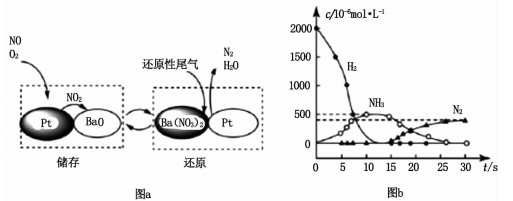
①通过BaO和Ba(NO3)的相互转化实现NOx的储存和还原。储存NOx的物质是___________。
②用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是___________。
③还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有氧条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。将该反应的化学方程式补充完整:___________![]()
(二)选考题:共45分。请考生从给出的2道物理题、2道化学题、2道生物题中每科任选一道作答。如果多做,则每科按所做的第一题计分。
35.【化学——选修3:物质结构与性质】(15分)
2018年2月27H,科技部发布2017年度中国科学十大进展。北京大学化学与分子工程学院马丁研究组与中国科学院山西煤化硏究所温晓东以及大连理工大学石川等合作的研究,实现氢气的低温制备和存储位列其中之—。使得科学研究的热点储氢材料又一次进入人们的视野。

①CO能形成Ni(CO)4,沸点为42.2℃,Ni(CO)4的晶体类型为_______________,标准状况下,VLCO分子形成Ni(CO)4中含σ键数目为_____________。
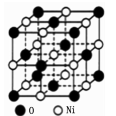
②如图所示为NiO晶体的晶胞示意图。在NiO晶体中Ni2+的半径为a pm,O2-的半径为b pm,假设它们在晶休中是紧密接触的,则在NiO晶体中原子的空间利川率为_____________。(用含字母a、b的计算式表达)
36.【化学——选修5:有机化学】(15分)
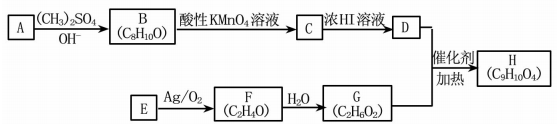
化合物H属于酯类化合物,是一种医药中间体。实验室由化合物A和E制备H的一种合成路线如下图:
已知:
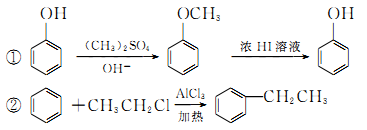
回答下列问题:
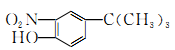 的合成路线(其它试剂任选):
的合成路线(其它试剂任选):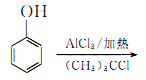

欢迎访问“”——